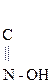Фенолокислоты вступают в р-ции SЕ по бензольному кольцу.
При бромировании, нитрировании, сульфировании салициловой к-ты заместители поступают в орто- и пара- положения по отношению к –ОН группе и в мета- положение по отношению –СООН гр., т.о. действие двух функциональных групп согласованное.
Оксокислоты
Это карбоновые к-ты, содержащие карбонильную группу. Различают кето- и альдегидок-ты.
Номенклатура
Тривиальная, рациональная, международная:
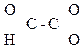 СН3–
СН3– 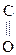 –СООН СН3–
–СООН СН3– 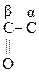 Н2–СООН
Н2–СООН
Глиоксалевая Пировиноградная Ацетоуксусная к-та (АУК),
к-та к-та (ПВК), b-кетомасляная к-та,
a-кетопропионовая, 3-оксобутановая к-та
2-оксопропановая
к-та
Изомерия кеток-т – это изомерия цепи и положения гр. 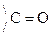 .
.
Оксок-ты могут быть одно-, двух- и многоосновные.
НООС–(СН2)2–  –СООН, НООС–СН2–
–СООН, НООС–СН2–  –СООН
–СООН
a-Кетоглутаровая к-та Щавелевоуксусная к-та (ЩУК),
2-кетоянтарная к-та
Все указанные к-ты являются естественными продуктами обмена веществ.
Оксок-ты, имея в молекуле гр. –СООН и 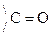 , обладают св-вами, характерными для к-т, альдегидов и кетонов.
, обладают св-вами, характерными для к-т, альдегидов и кетонов.
Р-ции по гр. –СООН – смотрите р-ции в разделе оксик-т; оксок-ты диссоциируют, образуют соли, сложные эфиры, ангидриды, хлорангидриды, амиды.
По карбонильной гр. идут р-ции АN, при этом образуются оксимы, гидразоны, оксинитрилы и т.д., т.е. проходят р-ции с Н2, РС15, NH2OH, NH2– NH2, NH2–NH–С6Н5, НСN, НОR, р-ции окисления.
|
|
|
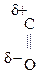 –СООН
–СООН 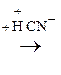
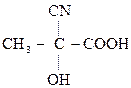 ,
,
|
|
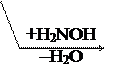
В этом случае р-ции протекают легче, чем для обычных кетонов.
2-оксо-ты окисляются даже такими слабыми окислителями как Сu(ОН)2, при этом образуются две к-ты как и для типичных кетонов:
Н2О + СО2
|
|
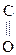 –СООН + О + НОН ® СН3СООН + НО–СООН
–СООН + О + НОН ® СН3СООН + НО–СООН Пировиноградная к-та
Это результат увеличения d+ заряда атома С гр. 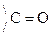 и объясняет также способность кеток-т легко декарбоксилироваться. Пировиноградная к-та при нагревании или действии фермента декарбоксилазы разлагается:
и объясняет также способность кеток-т легко декарбоксилироваться. Пировиноградная к-та при нагревании или действии фермента декарбоксилазы разлагается:
|
 –СООН ® СН3–
–СООН ® СН3– 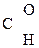 + СО2
+ СО2
Ацетоуксусная к-та легко декарбоксилируется как и все b-кеток-ты даже при слабом нагревании:
СН3–  –СН2–СООН
–СН2–СООН 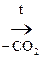 СН3–
СН3–  –СН3
–СН3
АУК Ацетон
В свою очередь 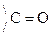 группа, оказывая влияние на гр. –СООН, увеличивает ее кислотность. ПВК в 500 раз сильнее пропионовой к-ты.
группа, оказывая влияние на гр. –СООН, увеличивает ее кислотность. ПВК в 500 раз сильнее пропионовой к-ты.
Для оксок-т характерно существование двух изомерных форм: кетонной и енольной, легко переходящих друг в друга и находящихся в динамическом равновесии. Напомним, что явление существования вещ-ва в виде нескольких изомерных формах, легко переходящих друг в друга и находящихся в подвижном равновесии, наз-ся таутомерией. В зависимости от возникающих групп таутомерия наз-ся по-разному: кето-енольная, лактим-лактаимная, прототропная. Для кеток-т характерна кето-енольная таутомерия:
|
|
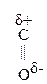
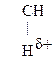 –
– 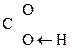 Û R–
Û R– 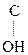 =CH–
=CH– 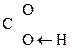 .
.
Кето-енольная таутомерия встречается и в обычных альдегидах и кетонах, однако енола содержится в таких системах очень мало (~ 2,5 ×10-5%), т.е. равновесие практически сдвинуто в сторону кетонной формы:
СН3–  –СН3 СН3–
–СН3 СН3– 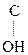 =CH2
=CH2
Ацетон
Введение ЭА заместителя у енолизированного атома С, например гр. –СООН, смещает равновесие в сторону енола:
|
|
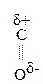 –
– 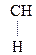 –
– 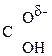 Û СН3–
Û СН3– 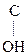 =CH–СООН
=CH–СООН
Енольная форма стабилизируется, если двойная С=С связь сопряжена со второй p-системой или гр. –ОН участвует в образовании внутримолекулярной Н-связи. Так, этиловый эфир ацетоуксусной к-ты существует уже на 7,5% в енольной форме, т.к. стабилизирован Н-связью:
СН3– 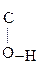 СН–
СН–  –ОС2Н5 Û СН3–
–ОС2Н5 Û СН3–  –CH2–
–CH2– 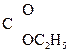 .
.
Смещение равновесия зависит от природы растворителя, температуры (с ее увеличением уменьшается содержание енольной формы) и др. факторов.
Доказательством наличия енольной формы являются р-ции: с Вr2 (водой) – на двойную связь (обесцвечивание), с FeC13 р-ция на –ОН гр. (фиолетовое окрашивание); наличие 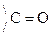 гр. – р-ции с NH2OH, NH2– NH2, NH2–NH–С6Н5 (образование осадков).
гр. – р-ции с NH2OH, NH2– NH2, NH2–NH–С6Н5 (образование осадков).
Многие р-ции в живых организмах проходят через енольную форму. Так, фосфорный эфир пировиноградной к-ты является важным фосфолирующим и ацилирующим агентом обмена вещ-в:
CH2= 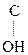 –
– 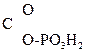 .
.
Тесты для самостоятельной работы студентов
Вариант 1
1. В процессе углеводного обмена в организме образуется щавелевоуксусная кислота, имеющее строение:
НООС – С – СН2 – СООН.
ﺍﺍ
О
Укажите название ее по Международной номенклатуре:
а) бутандиовая кислота; б) 2-оксобутандиовая кислота;
в) 3-оксобутандиовая кислота; г) α- оксоянтарная кислота.
2. Укажите соединение с хиральным атомом углерода:
а) НООС – СН2 – СН – СН2 – СООН; б) НООС – СН2 – СН2 – СN;
ﺍ
OH
в) НООС – СН2 – СН – СООН; г) НООС – СН2 – СН2 – NН2.
ﺍ
OH
3. Укажите соединение, для которого возможна изомерия положения функциональной группы:
а) 2-гидроксибутандиовая кислота;
б) 2-оксобутандиовая кислота;
в) 3-гидроксибутановая кислота;
г) 2-гидроксиэтановая кислота.
4. Образование изоамилового эфира 3-оксобутановой кислоты происходит по механизму:
а) AN; б) SN; в) SE; г) AE.
5. Фенилгидразон щавелевоуксусной кислоты образуется из:
а) фенола; б) фенолфталеина;
в) фенилгидразина; г) фенилсалицилата.
Вариант 2
1. Укажите соединение, у которого имеется хиральный атом углерода:
а) 2-метилпропановая кислота;
б) пропанол – 2;
в) 2-гидроксипропановая кислота;
г) 2-гидрокси, 2-метилпропановая кислота.
2. Качественной реакцией на α-, β-, γ- оксикислоты является:
а) окисление; б) галогенирование;
в) дегидратация; г) дегидрирование.
3. Кето – енольная таутомерия характерна для:
а) оксикислот; б) оксокислот;
в) фенолокислот; г) аминокислот.
4. При окислении 3-оксобутановой кислоты образуются:
а) Н – СООН и СН3 – СООН;
б) СН3 – СООН и НООС – СООН;
в) СН3 – СН2 – СООН и Н – СООН;
г) СН3 – СН2 – СН2 – СООН и Н2О.
5. По какому механизму протекает реакция образования оксинитрила из пировиноградной кислоты:
а) Е; б) АN; в) SE; г) AE.
Вариант 3
1. Известно, что аспирин получают из:
а) карболовой кислоты; б) бензойной кислоты;
в) салициловой кислоты; г) лимонной кислоты.
2. Фенилгидразон ацетоуксусной кислоты образуется из:
а) фенола; б) фенолфталеина;
в) фенилгидразина; г) фенилсалицилата.
3. В процессе углеводного обмена в организме образуется ацетоуксусная кислота, имеющее строение Н3С – С – СН2 – СООН.
ﺍﺍ
О
Укажите название ее по Международной номенклатуре:
а) бутандиовая кислота; б) 2-оксобутандиовая кислота;
в) 3-оксобутандиовая кислота; г) 3-оксобутановая кислота.
4. Метилсалицилат образуется по механизму:
а) AN + Е; б) SN; в) SE; г) AE.
5. Укажите соединение, у которого возможна изомерия:
а) фенол;
б) бензойная кислота;
г) анилин.
Вариант 4
1. Амид салициловой кислоты образуется в результате реакции:
а) кислоты со спиртом; б) кислоты с амином;
в) кислоты с аммиаком; г) кислоты с кислотой.
2. Образование лактида характерно для:
а) оксикислот; б) оксокислот;
в) фенолокислот; г) аминокислот.
3. Известно, что цитраты получают из:
а) карболовой кислоты; б) бензойной кислоты;
в) салициловой кислоты; г) лимонной кислоты.
4. Сложный эфир оксокислоты образуется при взаимодействии оксокислоты и:
а) спирта; б) метана; в) аммиака; г) кетона
5. Укажите соединение, для которого возможна оптическая изомерия:
а) 2,3-дигидроксибутандиовая кислота;
б) 2-оксобутандиовая кислота;
в) 3-оксобутановая кислота;
г) 2-гидроксиэтановая кислота.
Вариант 5
1. В процессе углеводного обмена в организме образуется пировиноградная кислота, имеющее строение:
Н3С – С – СООН.
ﺍﺍ
О
Укажите название ее по Международной номенклатуре:
а) 2-оксобутановая кислота; б) 2-оксопропановая кислота;
в) 2-оксипропановая кислота; г) α - кетопропионовая кислота.
2. Укажите соединение, для которого возможна оптическая изомерия:
а) 3-гидрокси,3-карбоксипентандиовая кислота;
б) 2-оксобутандиовая кислота;
в) 3-оксобутановая кислота;
г) 2-гидроксипропановая кислота.
3. Известно, что малаты получают из:
а) яблочной кислоты; б) молочной кислоты;
в) салициловой кислоты; г) лимонной кислоты.
4. Образование лактона характерно для:
а) оксикислот; б) оксокислот;
в) фенолокислот; г) аминокислот.
5. Гидразон пировиноградной кислоты образуется по механизму:
а) AN + Е; б) SN; в) SE; г) AE.
Ответы к тестам “ Окси-, оксокислоты ”
| вариант вопрос | 1 | 2 | 3 | 4 | 5 |
| 1 | б | в | в | в | б |
| 2 | в | в | в | а | г |
| 3 | в | б | г | г | а |
| 4 | б | б | б | а | а |
| 5 | в | б | в | а | а |
 2020-04-12
2020-04-12 1542
1542