Для анализа работы паросиловых установок существенное значение имеют изохорный, изобарный, изотермический и адиабатный процессы. Расчет этих процессов можно выполнить либо с помощью таблиц воды и водяного пара, либо с помощью h, s -диаграммы. Первый способ более точен, но второй более прост и нагляден.
Общий метод расчета по h, s - диаграмме состоит в следующем. По известным параметрам наносится начальное состояние рабочего тела, затем проводится линия процесса и определяются его параметры в конечном состоянии. Далее вычисляется изменение внутренней энергии, определяются количества теплоты и работы в заданном процессе.
Изохорный процесс (рис. 4.9). При нагревании пара при постоянном объеме влажный пар можно перевести в сухой насыщенный и перегретый. Охлаждением его можно сконденсировать, но не до конца, так как при каком угодно низком давлении над жидкостью всегда находится некоторое количество насыщенного пара. Это означает, что изохора не пересекает нижнюю пограничную кривую.
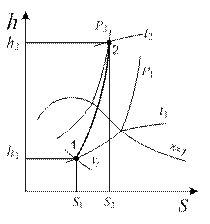
Рис. 4.9. Изохорный процесс водяного пара
Изменение внутренней энергии водяного пара при
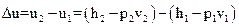 .
.
Данная формула справедлива и для всех без исключения остальных термодинамических процессов.
В изохорном процессе внешняя работа l=0, поэтому подведенная теплота расходуется (в соответствии с первым законом термодинамики) на увеличение внутренней энергии пара:
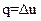 .
.
Изобарный процесс (рис. 4.10). При подводе теплоты к влажному насыщенному пару его степень сухости увеличивается и он (при постоянной температуре) переходит в сухой, а при дальнейшем подводе теплоты – в перегретый пар (температура пара при этом растет). При отводе теплоты влажный пар конденсируется при Ts=соnst.
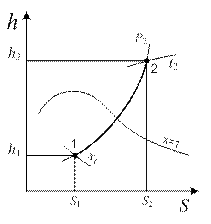
Рис. 4.10. Изобарный процесс водяного пара
Участвующая в процессе теплота равна разности энтальпий:
q=h2–h1.
Работа процесса подсчитывается по формуле
l=p(v2–v1).
Изотермический процесс (рис. 4.11). Внутренняя энергия водяного пара в процессе T=соnst не остается постоянной (как у идеального газа), так как изменяется ее потенциальная составляющая.
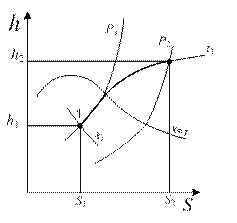
Рис. 4.11. Изотермический процесс водяного пара
Величина Du находится по формуле
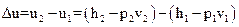 .
.
Количество участвующей в изотермическом процессе теплоты равно:
q=T(s2–s1).
Внешняя работа определяется из первого закона термодинамики:
l=q–Du.
Адиабатный процесс (рис. 4.12). При адиабатном расширении давление и температура пара уменьшаются, и перегретый пар становится сначала сухим, а затем влажным.
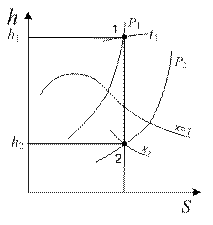
Рис. 4.12. Адиабатный процесс водяного пара
Работа адиабатного процесса определяется выражением
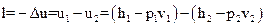 .
.
Влажный воздух
Влажный воздух представляет собой смесь сухого воздуха и водяного пара.
Смесь сухого воздуха и насыщенного водяного пара называется насыщен-ным влажным воздухом.
Смесь сухого воздуха и перегретого водяного пара называется ненасыщенным влажным воздухом.
Температура, до которой необходимо охлаждать ненасыщенный влажный воздух, чтобы, содержащийся в нем перегретый пар стал насыщенным, называется температурой точки росы. При дальнейшем охлаждении влажного воздуха (ниже температуры точки росы) происходит конденсация водяного пара.
Влагосодержание, абсолютная и относительная влажность.
Масса пара в 1 м3 влажного воздуха, численно равная плотности пара rп при парциальном давлении рп, называется абсолютной влажностью.
Отношение действительной абсолютной влажности воздуха rп к максимально возможной абсолютной влажности rs при той же температуре называют относительной влажностью и обозначают через j:
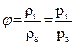 ,
,
где рп – парциальное давление водяного пара во влажном воздухе;
рs – максимально возможное парциальное давление водяного пара при данной температуре.
Для сухого воздуха j=0, для насыщенного воздуха j=100%.
Величина относительной влажности сама по себе полностью не характеризует содержание пара во влажном воздухе, для этого еще нужно знать температуру влажного воздуха, однозначно определяющую величину рs.
Отношение массы водяного пара Мп, содержащегося во влажном воздухе, к массе сухого воздуха Мв называется влагосодержанием воздуха и измеряется в килограммах на килограмм:
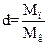 .
.
Определяя массы сухого воздуха и водяного пара из уравнения состояния идеального газа, и учитывая что рп=jрs, mп=18,06 кг/моль и mв=28,95 кг/кмоль, то
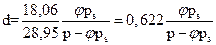 ,
,
где р – внешнее давление.
 2020-04-12
2020-04-12 150
150








