Нормальные условия: p = … мм рт. ст.= … Па; T = … К
1. Плотность воздуха: r = … кг/м3
2. Средняя арифметическая скорость молекул воздуха: 
3. Средняя длина свободного пробега молекул воздуха: 
4. Концентрация молекул воздуха: n =… 1/м3
5. Среднее число столкновений молекул воздуха 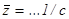
6. Эффективный диаметр молекул воздуха: d = … м



Цель работы:
Углубление теоретических представлений об энтропии, экспериментальное наблюдение процесса плавления и кристаллизации и получение навыков измерения изменения энтропии.
1. Теоретическая часть
Термодинамический процесс обратим, если, протекая в обратном направлении, он возвращает систему в исходное состояние без затрат энергии (упругий удар, колебания маятника в отсутствии сопротивления, идеализированный цикл Карно). Большинство процессов в технике – необратимы или, по крайней мере, содержат этапы, являющиеся необратимыми (неупругий удар, процессы с трением, диффузия, теплообмен). Энтропия является количественной мерой степени необратимости процесса.
Из равенства КПД тепловых двигателей и термического КПД обратимого цикла Карно
 (1)
(1)
можно получить выражение
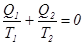 (2)
(2)
 |
Это выражение означает, что количество теплоты, полученное или отданное телом при обратимом процессе, пропорционально температуре. Отношение Q/T называется приведенным количеством теплоты. Сумма приведенных количеств теплоты при любом обратимом процессе равна нулю, что в дифференциальной форме имеет вид
 ,
,  (3)
(3)
причем интеграл берется по замкнутому контуру (круговой процесс). В каждом цикле кругового процесса все термодинамические параметры принимают исходные значения, т.е. их изменение равно нулю. В этом случае равна нулю и сумма приведенных количеств теплоты, что позволяет ввести термодинамический параметр состояния энтропию S, как некоторую функцию состояния, дифференциал которой
 (4)
(4)
Если некоторая термодинамическая система обратимо переходит из состояния 1, характеризующегося параметрами р1, V1, Т1, в состояние 2 с параметрами р2, V2, Т2, то изменение энтропии системы при таком переходе может быть вычислено по формуле
 , (5)
, (5)
где dQ — элементарный приток теплоты в систему, Т - термодинамическая температура всей системы. Интеграл берется вдоль «траектории» процесса, например абс при нагревании и плавлении, как показано на рисунке 1.
Возможны следующие три случая:
а) DS=0 – процесс обратим, может протекать как в прямом, так и в обратном направлениях;
б) DS>0 - процесс необратим, самопроизвольно протекает только в одном направлении
в) DS<0 - процесс самопроизвольно протекать не может, необходим подвод энергии извне.
2-й закон термодинамики с использованием понятия энтропии формулируется так:
Все процессы в природе протекают в направлении увеличения энтропии, энтропия замкнутой системы не может самопроизвольно уменьшаться.
В статистической физике энтропию связывают с термодинамической вероятностью состояния системы – с числом способов, которыми может быть реализовано данное состояние макроскопической системы. Согласно Больцману энтропия системы и термодинамическая вероятность связаны между собой следующим соотношением
S=klnW, (6)
 |
где k – постоянная Больцмана. Энтропия является мерой неупорядоченности системы.
 2020-04-20
2020-04-20 134
134








