Тема: Химия и производство
Многие химические реакции, с которыми вы познакомились в лабораторных условиях, или аналогичные им осуществляют в промышленных условиях при производстве важнейшей для повседневной жизни химической продукции.
Пластмассы, синтетические волокна, фармацевтические препараты, удобрения, мыла и моющие средства, красители, пестициды, косметика и парфюмерные изделия и даже компоненты пищи — все это только некоторые виды продукции, выпуск которой полностью или частично зависит от химической промышленности.
Одиннадцать первых мест по объему производства принадлежит веществам, формулы которых: H 2 SO 4, NH 3, N 2, СаО, O 2, С 2 Н 4, NaOH, Cl 2, НСl, H 3 PO 4, HNO 3. Эти-то вещества и используют в больших количествах далее для получения столь необходимых видов продукции, как названные выше.
Даже если речь идет о «100%-м природном продукте», это означает лишь то, что в нем нет синтетических добавок, и совсем не означает, что при получении не использовались какие-либо химические технологии.
| Химическая промышленность — это отрасль народного хозяйства, производящая продукцию на основе химической переработки сырья. Основой ее является химическая технология — наука о наиболее экономичных методах и средствах массовой химической переработки природных материалов (сырья) в продукты потребления и промежуточные продукты, применяемые в различных отраслях народного хозяйства. |
Главная задача химии и химической технологии — производство разнообразных веществ и материалов с определенным комплексом механических, физических, химических и биологических свойств.
Любое химическое производство создается на основе общих научных принципов:
| Общие принципы | Частные принципы |
| 1. Создание оптимальных условий проведения химических реакций | Противоток веществ, прямоток веществ, увеличение площади поверхности соприкосновения реагирующих веществ, использование катализатора, повышение давления, повышение концентраций реагирующих веществ |
| 2. Полное и комплексное использование сырья | Циркуляция, создание смежных производств (по переработке отходов) |
| 3. Использование теплоты химических реакций | Теплообмен, утилизация теплоты реакций |
| 4. Принцип непрерывности | Механизация и автоматизация производства |
| 5. Защита окружающей среды и человека | Автоматизация вредных производств, герметизация аппаратов, утилизация отходов, нейтрализация выбросов в атмосферу |
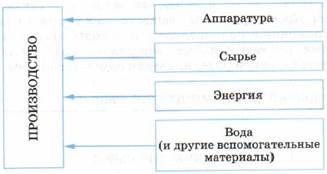
Несмотря на огромное многообразие химических производств веществ и материалов, все они включают составляющие, указанные на схеме.
Важнейшие составляющие химического производства
Сырье
Сырьем называют природные материалы (природные ресурсы), используемые в промышленности для получения различных продуктов и еще не прошедшие промышленной переработки. Иногда используют вторичное сырье — это изделия, отслужившие свой срок, или отходы каких-либо производств, которые экономически выгодно снова переработать в химические продукты.
Сырье химической промышленности классифицируют по различным признакам.
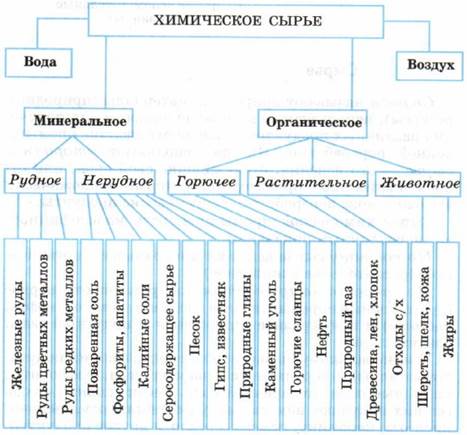
По составу сырье делят на минеральное и органическое (растительное и животное).
По агрегатному состоянию различают твердое (руды, горные породы, твердое топливо), жидкое (нефть, рассолы) и газообразное (природный и попутный газы, воздух) сырье.
Классификация химического сырья
Вода
Особое место среди природных ресурсов занимает вода. Она играет важную роль в химической промышленности.
· В ряде производств это сырье и реагент, непосредственно участвующий в основных химических реакциях, например при получении водорода, серной, азотной и фосфорной кислот, щелочей; в реакциях гидратации и гидролиза.
· Будучи универсальным растворителем и одним из наиболее распространенных катализаторов, вода дает возможность осуществлять многие химические реакции с большой скоростью в растворах или в присутствии ее следов. В химической, металлургической, пищевой и легкой промышленности воду используют как растворитель твердых, жидких, газообразных веществ. Часто ее применяют для перекристаллизации, для очистки различных продуктов производства от примесей.
· Вода используется как теплоноситель из-за ее большой теплоемкости, доступности и безопасности в применении. Ею охлаждают реагирующие массы, нагретые в результате экзотермических реакций. Водяным паром или горячей водой подогревают взаимодействующие вещества для ускорения реакций или проведения эндотермических процессов.
Энергия
Вы знаете, что большинство химических процессов требует затраты энергии. В химическом производстве энергию также расходуют на проведение вспомогательных операций: транспортировку сырья и готовой продукции, сжатие газов, дробление твердых веществ, контрольно-измерительное обслуживание и др. Химическая промышленность относится к одной из самых энергоемких. Средний расход только электрической энергии на производство 1 т аммиачной селитры NH 4 NO 3 равен 11 000 кВт•ч; 1т синтетического аммиака — 3200; 1 т фосфора — 16 500; 1 т алюминия — 19 000.
В химической промышленности используют различные виды энергии: электрическую, тепловую, ядерную, химическую и световую.
Электрическую энергию используют для проведения электролиза расплавов и растворов веществ, нагревания, в операциях, связанных с электростатическими явлениями, например, в электрофильтрах при производстве серной кислоты для очистки оксида серы (IV). Электроэнергию вырабатывают тепловые (ТЭС), атомные (АЭС) электростанции и гидроэлектростанции (ГЭС).
Тепловая энергия в химической промышленности необходима для нагревания реагирующих веществ при проведении химических реакций, а также для сушки, плавления, дистилляции, выпаривания и других операций. Ее источником в производстве цемента, стекла, керамики служат различные виды топлива (твердого, жидкого, газообразного).
Ядерную энергию используют главным образом для получения электроэнергии. Но такие реакции, как полимеризация, синтезы фенола и анилина, отверждение полимеров, проводят с помощью радиоактивного излучения.
Ученые разрабатывают способы использования солнечной энергии, например фотохимическое разложение воды.
 2020-05-11
2020-05-11 361
361







