B – источник; D 1 - зеркало осветителя; D 2 - зеркало конденсора; E – кювета; D – монохроматор; F1 - входная щель; F2 - выходная щель; G – приёмник; H - усилитель; I – регистратор.
Источником ИК-излучения обычно служит стержень из карбида кремния -глобар, который нагревается свыше тысячи градусов Цельсия, а также штифт Нернста, состоящий из оксидов лантаноидов. Однако в более новых версиях прибора на смену старым источникам пришли лазеры. Источник света проходит через кювету с анализируемым веществом и через раствор сравнения.
После прохождения излучения через кювету оно попадает на монохроматор, который представляет собой оптическую систему прибора. Главная его функция – направлять источник излучения по необходимому пути при помощи задания необходимого диапазона раскрытия щели и изменения положения зеркала. Внутри монохроматора располагается зеркало Литтрова и призма. Свет отражается от зеркала и проходит через призму, что способствует его лучшей фокусировке.
Оптическая часть прибора должна хорошо пропускать инфракрасные лучи, поэтому изготавливается из соответствующего материала. Это соли галогенидов щелочных и щелочноземельных металлов (CaF2, KBr, CsI, LiF, NaCl).
Для интервала 4000-1700 см-1 применяются призмы из LiF. Нижу 1700 см-1 LiF непрозрачен, а выше 4000 см-1 дисперсия его меньше, чем у стекла. Призма из NaCl может быть использована в диапазоне 4000 – 660 см-1. Призмы из KBr применяются в области от 400 до 650 см-1, а призмы из CsI - в области 400-180 см-1 [7].
Различают два типа приёмников: тепловые (бломеры и теплопары) и фотоэлектронные. Первые используют для средней ИК-области, а вторые в более высокой. Таким образом, выбирать приёмник следует, исходя из исследуемого материала.
В качестве регистрирующего устройства во многих современных устройствах используют компьютер, оснащенный специальной программой.
Глава 3
Пробоподготовка
Способ пробоподготовки выбирают в соответствии с агрегатным состоянием вещества.
Сложнее всего снимать спектры из мелкокристаллических сыпучих веществ, т.к. свет неупорядоченно отражается от каждой песчинки, частично преломляется и рассеивается. Чтобы снизить вероятность появления таких нежелательных искажений, свободные полости заполняют жидкостью со схожим показателем преломления. Эти жидкости получили название иммерсионные.
Вещества в жидком агрегатном состоянии наносят в виде тонкой плёнки толщиной от 0,005 до 0,1 мм на прозрачные в данной области пластины из хлорида натрия или бромида калия. Также можно снимать спектры и из растворов в узких областях. Для такого метода обычно берутся кюветы из нерастворимых в воде материалов.
Из твёрдых веществ делают коллоидный раствор в вазелиновом масле, используемый, как иммерсионное вещество. Твёрдые соединение тщательно перемешивают в ступке, а затем добавляют несколько капель иммерсионной жидкости. Получившуюся суспензию выкладывают на пластины из хлорида натрия или бромида калия и плотно сжимают (следят, чтобы внутри не образовывались пузырьки воздуха).
Другим способом исследования твёрдого образца является его прессовка с галогенидом щелочного металла. В результате получается небольшая полупрозрачная таблетка. Такой метод отличается удобством хранения исследуемого вещества и отсутствием мешающих полос поглощения. Однако есть вероятность реакции между таблеткой и атмосферными газами, что приводит к засорению исходного продукта, а в следствии неточным показаниям. Поэтому такой метод лучше применять с нерастворимыми в обычных растворителях веществами, либо образцами имеющим прочную кристаллическую решётку.
Глава 4
Общие понятия о биологически активных веществах.
Для дальнейшего рассмотрения ИК-спектров биологически активных соединений рассмотрим, что представляет класс этих сложных органических соединений.
Биологически активные вещества – это очень важный класс органических соединений, отвечающий за правильное регулирование жизнедеятельности всех систем организма. Биохимия изучает свойства веществ и механизмы функциональных групп, входящих в их состав, а также какое действие оказывают биологически активные вещества на синтез ДНК, строение клеток и органов.
Живой организм постоянно обменивается энергией с окружающей средой и при этом должен сохранять постоянство химического состава. Эти процессы регулируются разными параметрами, однако главную роль занимают биологически активные компоненты. Часть из них поступает с пищей – витамины, другая синтезируется железами внутренней и внешней секреции – гормоны.
К биологически активным веществам относятся: витамины, ферменты, гормоны, лекарства.
Витамины
Витамины – низкомолекулярные органические соединения различной химической природы, необходимые для осуществления важнейших процессов, протекающих в живом организме. [8] При этом витамины не участвуют в пластическом и энергетическом обмене.
Ещё с древних времён людям было известно, что отсутствие определённых продуктов вызывает заболевания. Однако до 1880 г. никто не предполагал, что в пищевых продуктах содержатся маленькие компоненты, оказывающие большое влияние на организм. Своё название витамины получили от латинского слова vita – жизнь. В настоящее время известно более 30 таких соединений. [9]
Для нормального развития человеку необходимо ежедневное поступление 100-120 мг витаминов.
На сегодняшний день принято обозначать витамины латинскими буквами: A, B, C, D и т.д.. Классифицируются они на растворимые в воде (B1, B2, B3, B6, B12, H, C, P), растворимые в жирах (A, D, E, K), витаминоподобные вещества (B15, U, ПАБК). [10]
Необходимость изучения витаминов вызвана тем, что они влияют практически на все сферы жизни:
· Улучшают сопротивляемость заболеваниям
· Поддерживают развитие (особенно подрастающего организма)
· Способствует усвоению микро- и макроэлементов
· Регулируют обмен веществ
Ферменты
Ферменты – это органические катализаторы белковой природы, которые ускоряют реакции, необходимые для функционирования живых организмов. [11] Благодаря их действию скорости многих реакций проходят в миллион раз быстрее, чем в отсутствие ферментов. Действуя, как катализаторы, они уменьшают энергию активации (энергия необходимая для протекания реакции между веществами), тем самым позволяют взаимодействовать многим важным соединениям. Таким образом, становятся возможны реакции, без дополнительных затрат и повышения температуры.
Изначально считалось, что ферменты это небольшие вещества, сорбированные на белках, однако позднее выяснили, что они по своей природе являются белками и делятся на анаболические и катаболические. Первые применяются для синтеза органических веществ, вторые для распада. Как и все белки, ферменты образуют компактные структуры – глобулы.
Несмотря на то, что ферменты проявляют свойства присущие всем белкам, они также имеют и специфические особенности: зависимость от интервала температур и pH.
Многие ферменты работают только при нормальной температуре человеческого тела. Поэтому во время болезни превышение отметки 37° замедляет обменные процессы, связанные с действием ферментов, и ведёт к гибели.
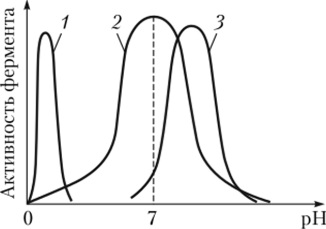 В основном, ферменты проявляют своё действие при pH 7. Изменение этого значения приводит к нарушению соотношения катионильных и анионильных групп. В сильнощелочной и сильнокислой среде ферменты теряют свою активность. На рис. 7 показана активность некоторых ферментов в разных средах.
В основном, ферменты проявляют своё действие при pH 7. Изменение этого значения приводит к нарушению соотношения катионильных и анионильных групп. В сильнощелочной и сильнокислой среде ферменты теряют свою активность. На рис. 7 показана активность некоторых ферментов в разных средах.
 2020-05-21
2020-05-21 94
94








