Рассмотрим механизм образования ионной связи на примере взаимодействия натрия и хлора.
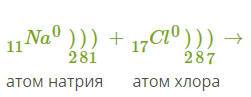
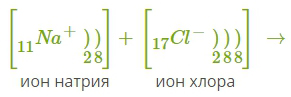

Na0+Cl0→Na++Cl−→Na+Cl−
Такое превращение атомов в ионы происходит всегда при взаимодействии атомов типичных металлов и типичных неметаллов, электроотрицательности которых резко различаются.
Ионная связь образуется в сложных веществах, состоящих из атомов металлов и неметаллов.
Пример: Взаимодействие кальция и фтора
1. Кальций — элемент главной подгруппы второй группы. Ему легче отдать два внешних электрона, чем принять недостающие.
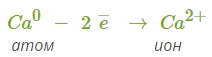
2. Фтор — элемент главной подгруппы седьмой группы. Ему легче принять один электрон, чем отдать семь.
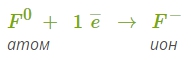
3. Найдём наименьшее общее кратное между зарядами образующихся ионов. Оно равно 2. Определим число атомов фтора, которые примут два электрона от атома кальция: 2:1=2.
4. Составим схему образования ионной связи:
Ca0+2F0→Ca2+F−2.
Пример: Взаимодействие натрия и кислорода
1. Натрий — элемент главной подгруппы первой группы. Он легко отдаёт один внешний электрон.

2. Кислород — элемент главной подгруппы шестой группы. Ему легче принять два электрона, чем отдать шесть.
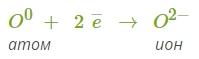
3. Найдём наименьшее общее кратное между зарядами образующихся ионов. Оно равно 2:1=2. Определим число атомов натрия, которые отдадут два электрона атому кислорода: 2.
4. Составим схему образования ионной связи:
2Na0+O0→Na+2O2−.
С помощью ионной связи образуются также соединения, в которых имеются сложные ионы:
NH+4,NO−3,OH−,SO2−4,PO3−4,CO2−3.
Значит, ионная связь существует также в солях и основаниях.
Соли аммония NH4NO3,NH4Cl,(NH4)SO42 не содержат металла, но образованы ионной связью.
Ионы создают вокруг себя электрическое поле, действующее во всех направлениях. Поэтому каждый ион окружён ионами противоположного знака. Такое соединение представляет собой огромную группу положительных и отрицательных частиц, расположенных в определённом порядке.
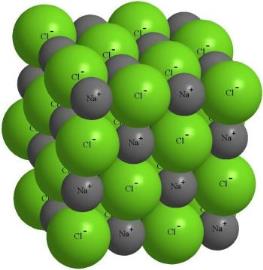
Притяжение между ионами довольно сильное, поэтому ионные вещества имеют высокие температуры кипения и плавления.
Все ионные соединения при обычных условиях — твёрдые вещества.
Примеры веществ с ионной связью:

Питьевая сода

Железный купорос

Поваренная соль
 2020-06-12
2020-06-12 213
213