Форма работы: индивидуальная, электронное обучение.
Урок повторения и обобщения знаний.
Цель: повторить основные сведения по разделу циклические предельные и непредельные углеводороды.
Основные понятия: циклогексан, бензол, бензольное кольцо.
Используемая литература:
Учебник Химия 10 класс О.С. Габриелян И.Г. Остроумов, С.А. Сладков Москва, «Просвещение». 2018 г
Интернет-ресурсы: https://obrazovaka.ru/himiya/predelnye-i-nepredelnye-uglevodorody-tablica.html
Ход урока.
1. Организационная часть.
2. Основная часть.
1. В зависимости от строения углеродной цепи углеводороды подразделяют на две группы:
- ациклические или алифатические,т.е. "жирные" (от греческого слова "алейфар" – "жир", т.к. впервые структуры с длинными углеродными цепями были обнаружены в составе жиров);
- циклические.
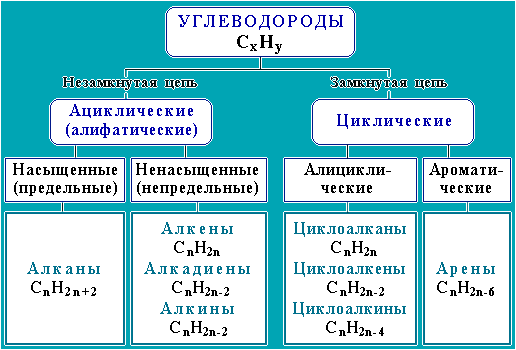
Открытая (незамкнутая) цепь алифатических углеводородов может быть неразветвленной или разветвленной. Углеводороды с неразветвленной углеродной цепью называют нормальными (н -) углеводородами.
Среди циклических углеводородов выделяют:
· алициклические (т.е. алифатические циклические);
· ароматические (арены).
В этом случае классификационным признаком служит строение цикла.
К ароматическим углеводородам относят соединения, содержащие один или несколько циклов С6Н6 (структура бензола).
2. По степени насыщенности различают:
- насыщенные (предельные) углеводороды (алканы и циклоалканы), в которых имеются только простые связи С-С и отсутствуют кратные связи;
- ненасыщенные (непредельные), содержащие наряду с одинарными связями С-С двойные и/или тройные связи (алкены, алкадиены, алкины, циклоалкены, циклоалкины).
Следует заметить, что хотя по составу бензол С6Н6 формально соответствует ненасыщенным циклическим углеводородам (его молекулу часто изображают как шестичленный цикл с тремя двойными связями), по свойствам это соединение
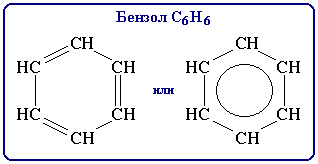
резко отличается от ненасыщенных веществ из-за делокализации кратных связей. Поэтому соединения ряда бензола относят к самостоятельной группе ароматических углеводородов (аренов).
Бензол – бесцветная, летучая, огнеопасная жидкость с неприятным запахом. Он легче воды (=0,88 г/см3) и с ней не смешивается, но растворим в органических растворителях, и сам хорошо растворяет многие вещества. Бензол кипит при 80,1 С, при охлаждении легко застывает в белую кристаллическую массу. Бензол и его пары ядовиты. Систематическое вдыхание его паров вызывает анемию и лейкемию.
– Видеоматериал (физические свойства бензола).
2. Химические свойства бензола.
1) Химические свойства бензола определяется строением его молекулы.
2) Ароматическая 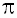 -система обладает повышенной устойчивостью.
-система обладает повышенной устойчивостью.
3) Поэтому хотя бензол является непредельным углеводородом, он проявляет свойства, характерные для предельных (склонность к реакциям замещения, устойчивость к действию окислителей).
Реакции замещения.

 2020-06-08
2020-06-08 191
191







