Практическая работа
Свойства растворов неэлектролитов
Цель: научиться рассчитывать температуры кристаллизации и кипения растворов, константы криоскопическую и эбуллиоскопическую, применять закон Рауля для расчета молекулярной массы вещества.
ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
Пример 1. Определите температуру кипения раствора, содержащего 1,84г нитробензола C6N5NO2 в 10 г бензола. Эбуллиоскопическая постоянная бензола 2,53. Температура кипения чистого бензола 80,20С.
Решение
По закону Рауля 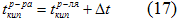 ,
,
 Температура кипения раствора:
Температура кипения раствора: 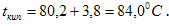
Пример 2. Раствор, содержащий 1,22 г бензойной кислоты C6H5COOH в 100 г сероуглерода, кипит при 46,529 0С, температура кипения сероуглерода 46,3 0С. Вычислите эбуллиоскопическую константу сероуглерода.
Решение
Повышение температуры кипения ∆t = 46,529 – 46,3 = 0,2290.
Молярная масса бензойной кислоты 122 г/моль. Из формулы (1) находим эбуллиоскопическую константу:

Пример 3. Раствор, содержащий 11,04 г глицерина в 800 г воды, кристаллизуется при –0,2790C. Вычислить молярную массу глицерина.
Решение
Температура кристаллизации чистой воды 00С, следовательно, понижение температуры кристаллизации ∆t = 0 – (– 0,279) = 0,2790.
Подставляя в уравнение (1) данные вычисляем молярную массу глицерина:

КОНТРОЛЬНЫЕ ВОПРОСЫ
Задание для первой погруппы
1. Раствор, содержащий 0,512 г неэлектролита в 100 г бензола, кристаллизуется при 5,296оС. Температура кристаллизации бензола 5,5оС. Криоскопическая константа 5,1о. Вычислите молярную массу растворенного вещества.
2. Вычислите температуру кристаллизации раствора мочевины (NH2)2CO, содержащего 5 г мочевины в 150 г воды. Криоскопическая константа воды 1,86о.
3. Раствор, содержащий 3,04 г камфоры C10H16O в 100 г бензола, кипит при 80,714 оС. Температура кипения бензола 80,2оС. Вычислите эбуллиоскопическую константу бензола.
4. Вычислите молярную массу неэлектролита, зная, что раствор, содержащий 2,25 г этого вещества в 250 г воды, кристаллизуется при –0,279 оС. Криоскопическая константа воды 1,86о.
5. Вычислите молярную массу вещества, если внесение 39 г этого вещества в 1000 г бензола привело к снижению температуры кристаллизации на 1,3˚С? Криоскопическая константа бензола 5,1˚.
6. Раствор, содержащий 25,65 г некоторого неэлектролита в 300 г воды, кристаллизуется при –0,465 оС. Вычислите молярную массу растворенного вещества. Криоскопическая константа воды 1,86о.
7. Вычислите криоскопическую константу уксусной кислоты, зная, что раствор, содержащий 4,25 г антрацена С14Н10 в 100 г уксусной кислоты, кристаллизуется при 15,718 оС. Температура кристаллизации уксусной кислоты 16,05 оС.
8. Температура кристаллизации раствора, содержащего 66,3 г некоторого неэлектролита в 500 г воды, равно –0,558 оС. Вычислите молярную массу растворенного вещества. Криоскопическая константа воды 1,86о.
9. Какую массу анилина C6H5NH2 следует растворить в 50 г этилового эфира, чтобы температура кипения раствора была выше температуры кипения этилового эфира на 0,53о. Эбуллиоскопическая константа этилового эфира 2,12о.
 2020-06-29
2020-06-29 145
145







