Тема: Химические свойства металлов. Электрохимический ряд напряжений металлов.
Основные понятия и термины по теме:металлы, электрохимический ряд напряжений металлов,химические свойства,
План изучения темы (перечень вопросов, обязательных к изучению):
1. Электрохимический ряд напряжений металлов.
2. Химические свойства металлов.
Краткое изложение теоретических вопросов:
По своим химическим свойствам все металлы являются восстановителями, все они сравнительно легко отдают валентные электроны, переходят в положительно заряженные ионы, то есть окисляются. Восстановительную активность металла в химических реакциях, протекающих в водных растворах, отражает его положение в электрохимическом ряду напряжений металлов, или ряду стандартных электродных потенциалов металлов.
Чем левее стоит металл в ряду стандартных электродных потенциалов, тем более сильным восстановителем он является, самый сильный восстановитель – металлический литий, золото – самый слабый, и, наоборот, ион золото (III) – самый сильный окислитель, литий (I) – самый слабый.
Металлы, стоящее в ряду напряжений левее водорода, способны вытеснять его из растворов разбавленных кислот, при этом растворяться в них.
Химические свойства
Взаимодействие с простыми веществами
- С кислородом большинство металлов образует оксиды – амфотерные и основные:
4Li + O2 = 2Li2O,
4Al + 3O2 = 2Al2O3.
- С галогенами металлы образуют соли галогеноводородных кислот, например,
Cu + Cl2 = CuCl2.
- С водородом самые активные металлы образуют ионные гидриды – солеподобные вещества, в которых водород имеет степень окисления -
2Na + H2 = 2NaH.
- С серой металлы образуют сульфиды – соли сероводородной кислоты:
Zn + S = ZnS.
- С азотом некоторые металлы образуют нитриды, реакция практически всегда протекает при нагревании:
3Mg + N2 = Mg3N2.
- С углеродом образуются карбиды:
4Al + 3C = Al4C3.
Взаимодействие с кислотами
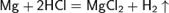
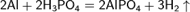
Взаимодействие с концентрированной серной кислотой
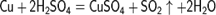
 2020-06-29
2020-06-29 84
84






