Задания на 12-16 мая по химии по теме; «Углеводы»
1 Изучив тему «Углеводы» заполните таблицу:
| Углевод | Определение, формула | Физические свойства | Химические свойства | Биологическая роль | Применение углеводов |
| глюкоза | |||||
| сахароза | |||||
| целлюлоза |
2. Напишите схематично уравнение реакций фотосинтеза и гидролиза крахмала
3. Напишите схему классификации углеводов
Углеводы
Углеводы - кислородсодержащие органические вещества, в которых водород и кислород находятся, как правило, в соотношении 2:1 (как и в молекуле воды).
Общая формула большинства углеводов - C n (H2O) m. Но этой общей формуле отвечают и некоторые другие соединения, не являющиеся углеводами, например: C(H2O) то есть HCHO или C2(H2O)2 то есть CH3COOH.
В линейных формах молекул углеводов всегда присутствует карбонильная группа (как таковая, или в составе альдегидной группы). И в линейной, и в циклической формах молекул углеводов присутствуют несколько гидроксильных групп. Поэтому углеводы относят к двуфункциональным соединениям.
Углеводы по их способности гидролизоваться делятся на три основных группы: моносахариды, дисахариды и полисахариды.
Углеводы
Моносахариды Дисахариды Полисахариды
Глюкоза Сахароза Крахмал
С6Н12О6 С12Н22О11 (С6Н10О5)n
Фруктоза Лактоза Целлюлоза
С6Н12О6 С12Н22О11 (С6Н10О5)n
Рибоза
С5Н10О5
Дезоксирибоза
С5Н10О4
Моносахариды
Если в линейной форме молекулы моносахарида есть альдегидная группа, то такой углевод относится к альдозам, т. е. представляет собой альдегидоспирт (альдозу), если же карбонильная группа в линейной форме молекулы не связана с атомом водорода, то это кетоноспирт (кетоза)
По числу атомов углерода в молекуле моносахариды делятся на триозы (n = 3), тетрозы (n = 4), пентозы (n =5), гексозы (n = 6) и т. д. В природе чаще всего встречаются пентозы и гексозы.
Если в линейной форме молекулы гексозы есть альдегидная группа, то такой углевод относится к альдогексозам (например, глюкоза), а если только карбонильная, то - к кетогексозам (например, фруктоза)
| Глюкоза (пример альдогексозы) | Фруктоза (пример кетогексозы) | Рибоза (пример альдопентозы) |
 Структурные формулы циклической формы Структурные формулы циклической формы
|  Структурные формулы циклической формы Структурные формулы циклической формы
|  Структурные формулы циклической формы Структурные формулы циклической формы
|
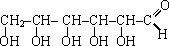 Структурные формулы линейной формы Структурные формулы линейной формы
|  Структурные формулы линейной формы Структурные формулы линейной формы
|  Структурные формулы линейной формы Структурные формулы линейной формы
|
Сложность химического и пространственного строения моносахаридов приводит к тому, что у них существует множество изомеров, так, например, существует несколько десятков изомерных гексоз.
Картина осложняется еще и тем, что при растворении моносахаридов у части молекул происходит обратимое раскрытие цикла, а обратная циклизация может привести к образованию другого изомера. Для  -глюкозы (обычной кристаллической формы глюкозы) этот процесс выражается следующим уравнением:
-глюкозы (обычной кристаллической формы глюкозы) этот процесс выражается следующим уравнением:

| 
| 
| 
| 
|
 -форма -форма
| альдегидная (линейная)форма | 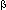 -форма -форма
|
Физические свойства моносахаридов: бесцветные кристаллические вещества, растворимые в воде, на вкус сладкие.
Химические свойства глюкозы
Являясь двуфункциональным соединением, глюкоза проявляет свойства многоатомного спирта и альдегида (в растворе) - качественная реакция.
1. Горение (а также полное окисление в живом организме):
C6H12O6 + 6O2  6CO2 +6H2O
6CO2 +6H2O
а) Как многоатомный спирт при комнатной температуре реагирует с Cu(OH)2, образуя раствор синего цвета.
б) Как альдегид окисляется аммиачным раствором оксида серебра (реакция серебряного зеркала) или гидроксидом меди(II) (качественные реакции):
| HOCH2—(CHOH)4—CHO | + Ag2O 
| HOCH2—(CHOH)4—COOH | + 2Ag |
| глюкоза | глюконовая кислота |
2.
HOCH2—(CHOH)4—CHO + Cu(OH)2  HOCH2—(CHOH)4—COOH + Cu2O + 2H2O
HOCH2—(CHOH)4—COOH + Cu2O + 2H2O
3.
в) Как альдегид вступает в реакции присоединения (восстанавливается):
| HOCH2—(CHOH)4—CHO | + H2 
| HOCH2—(CHOH)4—CH2OH |
| глюкоза | сорбит (гексангексаол-1,2,3,4,5,6) |
4. Спиртовое брожение: C6H12O6  2C2H5OH + 2CO2
2C2H5OH + 2CO2 
5. Молочнокислое брожение: C6H12O6  2CH3—CH(OH)—COOH
2CH3—CH(OH)—COOH
Дисахариды
Из дисахаридов наибольшее значение имеет сахароза C12H22O11:
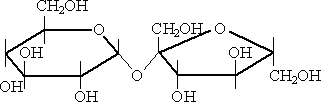
Молекула сахарозы состоит из остатков молекул глюкозы и фруктозы.
Физические свойства: бесцветное кристаллическое вещество, очень хорошо растворимое в воде, сладкое на вкус.
Химические свойства
В растворе сахарозы не происходит раскрытие циклов, поэтому она не обладает свойствами альдегидов.
1. Гидролиз (в кислотной среде):
| C12H22O11 | + H2O | C6H12O6 | + | C6H12O6 |
| сахароза | глюкоза | фруктоза |
2.
3. Являясь многоатомным спиртом, сахароза дает синее окрашивание раствора при реакции с Cu(OH)2.
Полисахариды
Целлюлоза - полимер (—C6H10O5—) n с элементарным звеном, представляющим собой остаток 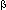 -глюкозы
-глюкозы

Молекулы целлюлозы имеют линейное строение и большую молекулярную массу. Между молекулами - прочные водородные связи. Целлюлоза нерастворима в воде и других растворителях.
Крахмал - полимер такого же состава, что и целлюлоза, но с элементарным звеном, представляющим собой остаток  -глюкозы
-глюкозы

Молекулы крахмала свернуты в спираль, большая часть молекул разветвлена. Молекулярная масса крахмала меньше молекулярной массы целлюлозы. Физические свойства -Крахмал - аморфное вещество, нерастворимое в холодной воде, но частично растворимое в горячей.
Химические свойства
1. Горение (практическое значение имеет для целлюлозы):
(C6H10O5) n + 6O2  6 n CO2 + 5 n H2O
6 n CO2 + 5 n H2O
2. Гидролиз:
(C6H10O5) n + n H2O n C6H12O6
При гидролизе крахмала образуется  -глюкоза, а при гидролизе целлюлозы -
-глюкоза, а при гидролизе целлюлозы - 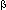 -глюкоза.
-глюкоза.
3. Качественная реакция на крахмал: с йодом возникает синее окрашивание.
4. Термическое разложение целлюлозы без доступа воздуха приводит к образованию метанола, уксусной кислоты, ацетона и др. продуктов.
5. С уксусной и азотной кислотой целлюлоза образует сложные эфиры [C6H7O2(ONO2)3] n и [C6H7O2(OCOCH3)3] n.
6. уравнения реакций фотосинтеза и гидролиза крахмала
свет
6СО2 + 6Н2О → С6Н12О6 + 6О2 – Q;
(С6Н10О5)n + nН2О → n С6Н12О6
 2020-06-29
2020-06-29 141
141






