ПЛАН ЗАНЯТИЯ № 35
Дисциплина: Химия
Тема: Белки
Цель занятия: изучить структуру белков; химические свойства белков: горение, денатурация, гидролиз, цветные реакции: биологические функции белков; белки как биополимеры.
Планируемые результаты
предметные: развитие и обобщение знаний обучающихся об органических веществах, углубление представлений обучающихся о важнейших теоретических понятиях органической химии;
сформировать представление о строении и свойствах нового класса органических соединений: изучить состав, строение, химические свойства белков;
расширить сведения о зависимости свойств органических соединений от строения. метапредметные: использование различных видов познавательной деятельности и основных интеллектуальных операций (постановки задачи, формулирования гипотез, анализа и синтеза, сравнения, обобщения, систематизации, выявления причинно-следственных связей, поиска аналогов, формулирования выводов) для решения поставленной задачи, применение основных методов познания (наблюдения, научного эксперимента) для изучения различных сторон химических объектов и процессов, с которыми возникает необходимость сталкиваться в профессиональной сфере личностные: умение использовать достижения современной химической науки и химических технологий для повышения собственного интеллектуального развития в выбранной профессиональной деятельности
Норма времени: 2 часа
Вид занятия: Лекция
План занятия:
1.Структура белков.
2.Химические свойства белков: горение, денатурация, гидролиз, цветные реакции.
3.Биологические функции белков.
4.Белки как биополимеры.
3. Выводы по занятию
Оснащение: доска, мультимедийный комплекс, презентация, химическая посуда, хим.реактивы
Литература:
Основные источники:
1. Рудзитис Г.Е., Фельдман Ф.Г., Химия. 11 класс. – М.: Просвещение, 2014
2. Рудзитис Г.Е., Фельдман Ф.Г., Химия. 10 класс. – М.: Просвещение, 2014
Дополнительные источники:
1. Габриелян О. С., Остроумов И. Г. Химия для профессий и специальностей технического профиля: учебник для студ. учреждений сред. проф. образования. — М., 2014.
2. Габриелян О. С., Остроумов И. Г., Остроумова Е. Е. и др. Химия для профессий и специальностей естественно-научного профиля: учебник для студ. учреждений сред. проф. образования. — М., 2014.
3. Габриелян О. С., Остроумов И. Г. Химия для профессий и специальностей социально-экономического и гуманитарного профилей: учебник для студ. учреждений сред. проф. образования. — М., 2014.
4. Габриелян О. С., Остроумов И. Г., Сладков С. А., Дорофеева Н.М. Практикум: учеб. Пособие для студ. учреждений сред. проф. образования. — М., 2014.
Преподаватель: Корниенко Т.В.
Тема: Белки
План занятия:
Ход урока
"Жизнь, есть способ существования белковых тел"
Ф. Энгельса.
Роль белков в организме человека
Мы сегодня с вами говорим о самых сложных молекулах, входящих в состав живых организмов. Давайте назовем их:
· кератин (состоят волосы, ногти, перья, кожа, рога, шерсть) – выполняют строительную функцию;
· пепсин (содержится в желудочном соке) – способен разрушать другие белки при пищеварении;
· антитела белковой природы находятся в крови: б-тромбин участвует в свертывании крови;
· инсулин (гормон поджелудочной железы) – регулирует обмен глюкозы;
· коллаген – компонент соединительной ткани;
· гемоглобин – транспортирует кислород ко всем клеткам и тканям организма;
· альбумин – яичный белок;
· фибрин, фибриноген – кровь;
· трипсин – поджелудочный сок;
· миозин – мышцы;
· глобулин – вакцина;
· родопсин – зрительный пурпур;
· лиозин – слюна.
2.Функции, выполняемые белками:
•защищают организм от микробов и вирусов, участвуя в выработке антител;
•регулируют энергобаланс, особенно при больших нагрузках или при дефиците в пище жиров и углеводов.
•обеспечивают рост, размножение и полноценное развитие организма, особенно нервной системы, регулируя раздражимость и реакции на внешние раздражители;
•входят в состав гормонов, мышц и других тканей;
•в связи с витаминами и микроэлементами являются биологическими катализаторами — ферментами;
•формируют способность высшей формы движения материи — мышление;
Состав белков
Откуда же берется это бесконечное многообразие белковых молекул, многообразие их функций и их особая роль в жизненных процессах? Для того, чтобы ответить на этот вопрос обратимся к составу и строению белков.
В состав белков входят атомы?...
Чтобы ответить на этот вопрос проведем разминку. Отгадайте загадки
Загадки: (ответы записать в конспект)
1. Он повсюду и везде:
В камне, в воздухе, в воде.
Он и в утренней росе
И в небес голубизне.
2. Я – самый легкий элемент,
В природе без меня ни шагу.
И с кислородом я в момент
Даю живительную влагу.
3. В воздухе он главный газ,
Окружает всюду нас.
Угасает жизнь растений
Без него, без удобрений.
В наших клеточках живет
Важный элемент …
4. Отправились школьники как – то в поход
(К задаче химической это подход).
Ночью костер развели при луне,
Песенки пели о ярком огне.
Отбросьте в сторонку свои сантименты:
Какие горели в огне элементы?
Да, правильно, это главные химические элементы, входящие в состав белка.
Об этих четырех элементах можно сказать словами Шиллера «Четыре элемента, сливаясь вместе, дают жизнь и строят мир».
Итак: Белки – это природные биополимеры, мономерами которых являются аминокислоты.
Известно много аминокислот, но в качестве мономеров любых природных белков известно только 20 аминокислот. В организме человека насчитывается до 100 000 белков.
4.Получение белков:
Как связаны аминокислоты в белке?
При помощи пептидной связи (амидная)
 (запись в тетради!)
(запись в тетради!)
Белки получают в результате реакции конденсации
Конденсацией называется реакция, приводящая к усложнению углеродного скелета и возникновению новой углеродной связи, причем из двух или более относительно простых молекул образуется новая, более сложная молекула. Обычно в результате реакции конденсации выделяется молекула воды.
Образование дипептида (запись в тетради!) 
Образование трипептида (записывать в тетрадь не надо)

5.По происхождению белки подразделяют на:
1) Животные – им богаты мясо, рыба, птица (20%), яйца, молоко и молочные продукты – сыр, творог (15-20%).
2) Растительные – они содержатся в зерновых: рис, пшеница, овес, рожь, гречиха, пшено, кукуруза (10%); в бобовых: фасоль, соя, горох, орехи – более 15%.
6.Физические свойства белков:
Есть твердые – это белки костей и хрящей и жидкие – яичный белок.
Одни хорошо растворимые в воде образуя коллоидные растворы (желатин, белок молока), а другие нерастворимые (белки сухожилий, хрящей, мышечные волокна, клейковина злаков).
Структуры белка
Давайте рассмотрим на экране модели первичной, вторичной, третичной и четвертичной структуры белка.
Первичная – прямая цепочка из аминокислот, удерживается пептидными связями.
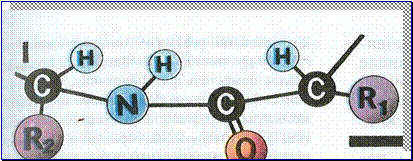
Вторичная – скрученная в спираль первичная цепочка, удерживается водородными связями. Такую структуру имеют фибриллярные белки (коллаген, белок кожи; фибриноген, белок крови; миозин, белок мышц)).

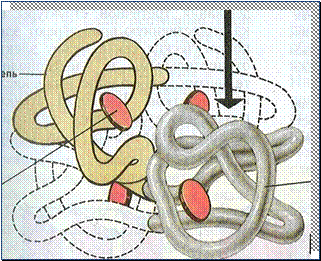
Третичная – многократно скрученная спираль, глобула, удерживается слабыми дисульфидными связями. Такую структуру имеют глобулярные белки (альбумины, глобулины).

Некоторые белки имеют четвертичную структуру – объединение нескольких глобул. Четыре глобулы связаны атомом железа имеет белок гемоглобин.
Химические свойства
1. Денатурация – необратимое свертывание белка под влиянием различных факторов: температуры, кислоты, щелочи, солей и т.д.
Давайте выясним влияние соляной кислоты и солей тяжелых металлов на белок куриного яйца.
а) денатурация белка соляной кислотой;
б) осаждение белка сульфатом меди.
в) горение шерстяной ткани – ощущается запах паленых перьев, этой реакцией можно отличить шерсть от тканей других видов.
Почему опасно отравление тяжелыми металлами?
При денатурации происходит как полное разрушение структур белка, так и частичное.
Если первичная структура не разрушена, то может произойти восстановление остальных структур - этот процесс называется ренатурация.
Процесс денатурации легче пронаблюдать у белков, растворимых в воде.
Где ежедневно вы с этим явлением встречаетесь? (мытье рук, головы, действие пепсина желудочного сока, прием препаратов, содержащих ферменты).
2. Цветные реакции белков
Опыт 1: Биуретовая реакция (распознавание пептидных связей).
К 2 мл раствора белка добавьте 2 мл 10% раствора NaOH, а затем 2–3 капли CuSO4.
Наблюдение: красно-фиолетовое окрашивание.
(ссылка https://www.youtube.com/watch?v=geyz_MDx4UE)
Вывод: содержатся пептидные группы.
Опыт 2: Ксантопротеиновая реакция (обнаружение бензольных ядер в аминокислотных остатках). К 2 мл раствора белка добавьте 0,5 мл конц. HNO3 и нагрейте.
Наблюдение: желтое окрашивание.
(ссылка https://www.youtube.com/watch?v=geyz_MDx4UE)
Вывод: в состав белков входят остатки ароматических аминокислот.
9.Выводы по занятию:
· белки – это высокомолекулярные органические соединения, биополимеры, состоящие из мономеров
α -аминокислот
· аминокислоты соединяются в полипептидную цепочку за счёт пептидной связи
· аминокислоты заменимые и незаменимые
· белки могут быть простыми и сложными
· четыре структуры белка ( первичная, вторичная, третичная и четвертичная)
· денатурация – это утрата белковой молекулой своей структурной организации, обеспечивающей функциональные свойства белка
· ренатурация - процесс восстановления структуры белка
10. Домашнее задание: §38, тест стр.183.
 2020-06-30
2020-06-30 313
313






