Заключение
Приложения
Список литературы
Введение.
В данной работе будут рассмотрены методы получения и свойства карбоната марганца (II).
Карбонат марганца — сложное вещество, химическая формула — MnCO3. Представляет собой бледно розовые кристаллы, в присутствии кислорода и воды приобретает бурую окраску.
Марганец самый активный элемент VII-B группы. Однако, он устойчив на воздухе, т.к. покрыт оксидной пленкой, которая препятствует дальнейшему окислению. Сам марганец ядовит, но его соединения не ядовиты и широко используются, активно реагируют мо многими кислотами. Оксиды и гидроксиды марганца в зависимости от его степени окисления проявляют разный кислотно-основный характер:
MnO - основный характер оксида;
Mn2O3 – преобладает основный характер (слабые кислотные св-ва);
MnO2 – амфотерный оксид.
В окислительно-восстановительных процессах соединения марганца проявляют различные св-ва в зависимости от его степени окисления и среды. Соли марганца со степенью окисления +2 подвергаются гидролизу по катионному типу. При этом рН<7. При нормальных условиях гидролиз заканчивается на первой ступени.
Большинство карбонатов хорошо растворимы в воде (Na2CO3, (NH4)2CO3, K2CO3). Карбонаты термически нестойки, кроме щелочных металлов – при нагревании они плавятся без разложения. Кислые соли (гидрокарбонаты) можно получить по реакции:
CaCO3 + CO2 + H2O = Ca(HCO3)2
Карбонаты кальция, магния, бария и др. применяют в строительном деле, в химической промышленности, оптике и др. В технике, промышленности и быту широко применяется сода (Na2CO3 и NaHCO3): при производстве стекла, мыла, бумаги, как моющее средство, при заправке огнетушителей, в кондитерском деле. Кислые карбонаты выполняют важную физиологическую роль, являясь буферными веществами, регулирующими постоянство реакции крови.
Теоретическая часть.
Нахождение в природе.
В природе карбонат марганца чаще встречается в виде минерала родохрозита (марганцевый шпат). 
На месторождении выделяются три типа руд: марганцевые карбонатные, марганцевые окисленные, магнетитовые. В распределении марганцевых руд намечается зональность: первично-оксидные руды отлагаются в прибрежной зоне среди осадков песчано-алеврито-глинистого состава; по мере удаления от берега оксидные руды постепенно сменяются карбонатными (родохрозит, манганокальцит, кальциевый родохрозит), ассоциирующими с глинами, кремнистыми глинами и опоками. Метаморфизованные месторождения возникли в результате многоэтапного регионального метаморфизма. Как известно, они широко распространены в Индии. При низкой ступени метаморфизма оксиды и, возможно карбонаты марганца были превращены в брауниты, а кремнистые породы — в кварциты.. Марганцевые карбонатные руды бурого и кремового цвета являются первичными; они состоят в основном из родохрозита, манганокальцита, родонита. Среднее содержание марганца в них составляет 24%. На верхних горизонтах месторождения, до глубины 30–70 м, под действием процессов выветривания карбонатные руды преобразованы в черные окисленные руды, состоящие из псиломелана, гаусманита, пиролюзита.
2) Строение кристаллической решетки карбоната марганца и химическая связь в ионе CO32-.
Карбонат марганца обладает гексагональной кристаллической решеткой (а = 0,4771 нм, с = 1,5664 нм, z = 6, пространств. группа R3с).
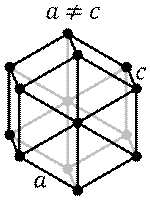
В ионе CO32- Центральный углеродный атом имеет sp²-гибридизацию. Длина связи C—O в карбонат-ионе составляет 129 пм.
 2020-07-01
2020-07-01 310
310







