- Окисление этанола.
С2Н5ОН + О2 → СН3СООН + H2O
- Окисление ацеталъдегида.
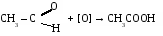
3. Окисление бутана.
2С4Н10 + 5О2 → 4СН3СООН + 2H2O
Основная часть получаемой уксусной кислоты используется для производства искусственных волокон и пластмасс на основе целлюлозы, для производства красителей, ядохимикатов.
ВЫСШИЕ КАРБОНОВЫЕ КИСЛОТЫ
С15Н31СООН – пальмитиновая кислота
С17Н35СООН – стеариновая кислота
С17Н33СООН – олеиновая кислота
С17Н31СООН – линолевая кислота
Высшие карбоновые кислоты вступают в те же реакции, чтои другие кислоты.
Соли высших карбоновых кислот называются мылами.
Мыла.
Мыла - соли высших карбоновых кислот.
1. Моющие мыла.
С17Н35СООNa – твердое мыло
С17Н35СООK –жидкое мыло
Мыла проявляют свойства солей, то есть реагируют с кислотами, щелочами и растворами других солей, а также подвергаются гидролизу.
2C17H35COONa + BaCl2 → (C17H35COO)2Ba↓ + 2NaCl
2C17H35COO- + 2Na+ + Ba2+ + 2Cl- → (C17H35COO)2Ba↓ + 2Na+ + 2Cl-
2C17H35COO- + Ba2+ → (C17H35COO)2Ba↓
C17H35COONa + H2O → C17H35COOH↓ + NaOH
C17H35COO- + Na+ + H2O → C17H35COOH↓ + Na+ + OH-
C17H35COO- + H2O → C17H35COOH↓ + OH-
2. Немоющие мыла.
(C17H35COO)2Сa, (C17H35COO)3Al
Немоющие мылаиспользуются для изготовления консистентных смазок (солидол) и для получения напалма.
Домашнее задание:
Упражнение.
1.Составьте уравнения реакций посхеме
СH4 → С2Н2 → С6Н6 → С6H5Cl → С6H5OH
2. Составьте уравнения реакций по схеме:
С2Н6 → С2Н4 → С2H5OH → С2H5 – O – С4H9
1. Составьте уравнения реакций по схеме:
С2Н6 → С2Н4 → С2H5Cl → С2H5OH → С2H5 – O – СH3
2. Составьте уравнения реакций, подтверждающих химические свойства метаналя
3. Написать уравнение плучения метилэтилового эфира
 2020-07-01
2020-07-01 80
80







