Алгоритм вычисления количества вещества продукта реакции по массовой доле исходного вещества в растворе
| ПОСЛЕДОВАТЕЛЬНОСТЬ ДЕЙСТВИЙ | ПРИМЕР ВЫПОЛНЕНИЯ ДЕЙСТВИЙ |
| 1.Прочитайте текст задачи. | Рассчитайте количество водорода, выделившегося при взаимодействии 730 г 30%-ого раствора соляной кислоты с цинком. |
| 2.Запишите условие и требование задачи с помощью общепринятых обозначений. |  2.Дано:
mраствора = 730 г 2.Дано:
mраствора = 730 г
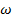 = 30% или 0,3 = 30% или 0,3
  ν (Н2) =?
ν (Н2) =?
|
| 3.Запишите уравнение реакции | 3.Решение: Zn + 2HCl = ZnCl2 + H2↑ |
| 4. Пользуясь формулой, рассчитайте массу чистого вещества. | mвещ. = mраствора · ω m (HCl) = 730 г · 0,3 = 219 г |
| метод пропорций | |
| 5. Над формулами записать, что известно по условию задачи | 219 г Х моль Zn + 2HCl = ZnCl2 + H2↑ |
| 6. Под уравнением записываем то, что следует из уравнения реакции с учётом условий задачи (находим массу соляной кислоты и количество водорода, которое равно коэффициенту перед формулой водорода). | Mr (HCl) = Ar(H) + Ar(Cl) = 1 + 35,5 = 36,5 M (HCl) = 36,5 г/моль m (HCl) = 2 моль · 36,5 г/моль = 73 г 219 г Х моль Zn + 2HCl = ZnCl2 + H2↑ 73 г 1моль |
| 7. Составьте пропорции и определите количество водорода . | 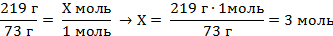
|
| количественный метод | |
| выполняем пункты 1 - 4 | |
| 5. Рассчитать молярную массу соляной кислоты | Mr (HCl) = Ar(H) + Ar(Cl) = 1 + 35,5 = 36,5 M (HCl) = 36,5 г/моль |
| 6. Рассчитать количество соляной кислоты | 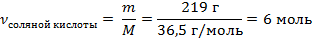
|
| 7. Над формулами записать, что известно по условию задачи и произведённых расчётов | 6 моль Х моль Zn + 2HCl = ZnCl2 + H2↑ |
| 8. Под формулами записываем, что следует из уравнения реакции (количество соляной кислоты и водорода, которые равны коэффициентам перед соответствующими формулами); составляем пропорцию | 6 моль Х моль
Zn + 2HCl = ZnCl2 + H2↑
2 моль 1 моль
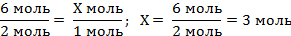
|
| алгебраический способ | |
| выполняем пункты 1 - 3 | |
| 4. По формуле находим количество водорода | Zn + 2HCl = ZnCl2 + H2↑
2 моль 1 моль
ν (HCl) = 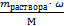 2 моль HCl – 1 моль H2, следовательно ν (H2) =
2 моль HCl – 1 моль H2, следовательно ν (H2) =  ν (HCl) ν (HCl)
|
| 5. Находим молярную массу соляной кислоты | Mr (HCl) = Ar(H) + Ar(Cl) = 1 + 35,5 = 36,5 M (HCl) = 36,5 г/моль |
| 6. Подставляем в формулу величины, производим расчёт | ν (H2) =  ν (HCl) = ν (HCl) = 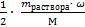
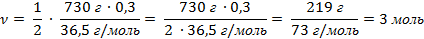
|
| Запишите ответ. | Ответ: ν (Н2) = 3 моль |
Алгоритм решения задач на концентрацию растворов
| ПОСЛЕДОВАТЕЛЬНОСТЬ ДЕЙСТВИЙ | ПРИМЕР ВЫПОЛНЕНИЯ ДЕЙСТВИЙ |
| расчёт массовой доли растворённого вещества | |
| 1.Прочитайте текст задачи. | Рассчитать массовую долю хлорида натрия в растворе, полученном при смешивании 28г соли и 252г воды. |
| 2.Запишите условие и требование задачи с помощью общепринятых обозначений. |  2.Дано:
mсоли = 28 г
mводы = 252 г 2.Дано:
mсоли = 28 г
mводы = 252 г
  ω (NaCl) =?
ω (NaCl) =?
|
| 3. Рассчитать массу раствора | 3.Решение: mраствора = mсоли + mводы mраствора = 28 г + 252 г = 280 г |
| 4. По формуле рассчитать массовую долю растворённого вещества | 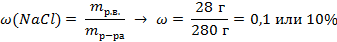
|
| 5 Записать ответ | Ответ: 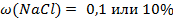
|
| вычисление массы вещества в растворе по массе раствора и массовой доле растворенного вещества (приготовление растворов) | |
| 1.Прочитайте текст задачи. | Вычислите массы гидроксида натрия и воды, необходимых для приготовления 400 г 20%-го раствора гидроксида натрия |
| 2.Запишите условие и требование задачи с помощью общепринятых обозначений. |  2.Дано:
mр-ра = 400 г
ω (NaОН) = 20% = 0,2 2.Дано:
mр-ра = 400 г
ω (NaОН) = 20% = 0,2
  m(NaOH) =?
mводы =?
m(NaOH) =?
mводы =?
|
| 3. Рассчитать массу гидроксида натрия в растворе (растворённое вещество) | 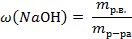
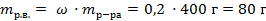
|
| 4. Рассчитайте массу воды | mраствора = mсоли + mводы mводы = mраствора - mсоли mводы = 400 – 80 = 320 г |
| Записать ответ | Ответ: mводы = 320 г; m(NaOH) = 80 г |
| решение задач на упаривание раствора | |
| при упаривании испаряется растворитель, а масса растворённого вещества остаётся неизменной; концентрация раствора увеличивается | |
| 1.Прочитайте текст задачи. | 100 г 25%-ного раствора соли упарили до 80 г. Вычислите массовую долю растворённого вещества в полученном растворе |
| 2.Запишите условие и требование задачи с помощью общепринятых обозначений. |  2.Дано:
mр-ра 1 = 100 г
mр-ра 2 = 80 г
ω1 = 25% или 0,25 2.Дано:
mр-ра 1 = 100 г
mр-ра 2 = 80 г
ω1 = 25% или 0,25
  ω2 =?
ω2 =?
|
| 3. Вычислить массу растворённого вещества в первом растворе по формуле | 
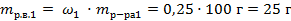
|
| 4. Вычислить массовую долю вещества во втором растворе | 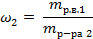
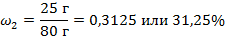
|
| 5.Записать ответ | Ответ: ω2 = 0,3125 или 31,25% |
| решение задач на концентрирование раствора | |
| при концентрировании в раствор добавляется дополнительная масса растворённого вещества; концентрация повышается | |
| 1.Прочитайте текст задачи. | К 250 г 5%-ного раствора соли добавили 23 г соли. Вычислите массовую долю полученного раствора |
| 2.Запишите условие и требование задачи с помощью общепринятых обозначений. |  2.Дано:
mр-ра 1 = 250 г
mсоли = 23 г
ω1 = 5% или 0,05 2.Дано:
mр-ра 1 = 250 г
mсоли = 23 г
ω1 = 5% или 0,05
  ω2 =?
ω2 =?
|
| 3. Вычислить массу растворённого вещества в первом растворе по формуле | 
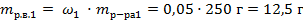
|
| 4. Вычислить массу растворённого вещества по формуле | 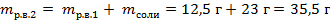
|
| 5. Вычислить массу полученного раствора по формуле | 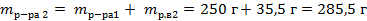
|
| 6. Вычислить массовую долю вещества во втором растворе | 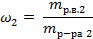
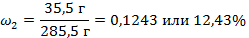
|
| 7.Записать ответ | Ответ: ω2 = 0,1243 или 12,43% |
| решение задач на разбавление раствора | |
| к раствору добавляется определённая масса растворителя; концентрация уменьшается | |
| 1.Прочитайте текст задачи. | К 180 г 10% - ного раствора кислоты добавили 20 г воды. Вычислите массовую долю полученного раствора |
| 2.Запишите условие и требование задачи с помощью общепринятых обозначений. |  2.Дано:
mр-ра 1 = 180 г
mводы = 20 г
ω1 = 10% или 0,1 2.Дано:
mр-ра 1 = 180 г
mводы = 20 г
ω1 = 10% или 0,1
  ω2 =?
ω2 =?
|
| 3. Вычислить массу растворённого вещества в первом растворе по формуле | 
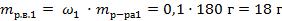
|
| 4. Вычислить массу полученного раствора по формуле | 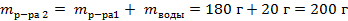
|
| 5. Вычислить массовую долю вещества во втором растворе | 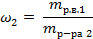
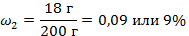
|
| 6. Записать ответ | Ответ: ω2 = 0,09 или 9% |
| решение задач на смешивание растворов | |
| 1.Прочитайте текст задачи. | К 230 г 30%-ного раствора щёлочи добавили 100 г 6%- ного раствора щёлочи. Вычислите массовую долю полученного раствора |
| 2.Запишите условие и требование задачи с помощью общепринятых обозначений. |  2.Дано:
mр-ра 1 = 230 г
ω1 = 30% или 0,3
m р-ра 2 = 100 г
ω2 = 6% или 0,06 2.Дано:
mр-ра 1 = 230 г
ω1 = 30% или 0,3
m р-ра 2 = 100 г
ω2 = 6% или 0,06
  ω3 =?
ω3 =?
|
| 3. Вычислить массы растворённого вещества в растворах по формуле | 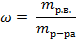
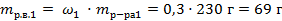
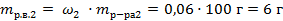
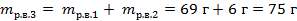
|
| 4. Вычислить массу полученного раствора по формуле | 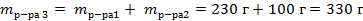
|
| 5. Вычислить массовую долю вещества в полученном растворе | 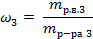
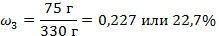
|
| 6. Записать ответ | Ответ: ω3 = 0,227 или 22,7% |
 2020-08-05
2020-08-05 505
505






