ГОСУДАРСТВЕННОЕ ПРОФЕССИОНАЛЬНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ТУЛЬСКОЙ ОБЛАСТИ
«ЕФРЕМОВСКИЙ ХИМИКО-ТЕХНОЛОГИЧЕСКИЙ ТЕХНИКУМ»
| Рассмотрено на заседании предметно-цикловой комиссии Протокол №___ от 2020г Председатель ПЦК ____________Л.В.Прасолова | СОГЛАСОВАНО Заместитель директора по УР _______________Е.Е. Саратова «____» _____________ 2020 г. |
ЭКЗАМЕНАЦИОННЫЙ ТЕСТ
ПМ. 01 Подготовка рабочего места, лабораторных условий, средств измерений, испытательного оборудования, проб и растворов к проведению анализа в соответствии с требованиями нормативно-технической документации, требования охраны труда и экологической безопасности
для профессии
18.01.33 Лаборант по контролю качества сырья, реактивов, промежуточных продуктов, готовой продукции, отходов производства (по отраслям)
Период обучения 2019-2020г.г.
Ефремов 2020 г.
| Номер варианта |
Номер вопроса | |||||||||
| Вариант 1 | 1 | 5 | 9 | 13 | 17 | 21 | 25 | 29 | 33 | |
| Вариант 2 | 2 | 6 | 10 | 14 | 18 | 22 | 26 | 30 | 34 | |
| Вариант 3 | 3 | 7 | 11 | 15 | 19 | 23 | 27 | 31 | 35 | |
| Вариант 4 | 4 | 8 | 12 | 16 | 20 | 24 | 28 | 32 | 36 | |
Шкала оценивания вопросов:
с1по28 вопрос -1 балл;
задачи №29-36 -2 балла
Оценки:
«5» - 11 баллов;
«4» -10 – баллов;
«3» -9-7 баллов;
«2» - 6 – 0 баллов.
1. Что такое титриметрическое определение?
2. Что называется титрованием?
3. Напишите формулу зависимости объемов количественно реагирующих растворов и их нормальных концентраций.
4. Правильное положение глаз при определении объема раствора в бюретке...
1 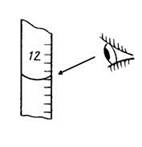 2
2 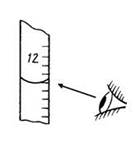 3
3 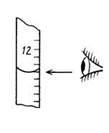
5. Расчеты результатов определений в титриметрии основаны на законе
A. кратных отношений
B. действующих масс
C. Авогадро
D. эквивалентов
6. Аликвотная часть – это количество...
A. миллилитров добавленного из бюретки раствора
B. капель добавленного из капельницы индикатора
C. миллилитров отобранного пипеткой раствора для анализа
D. миллилитров отобранного мензуркой раствора для анализа
7. Какая мерная посуда применяется при титриметрических определениях?
8. Что такое рабочий раствор?
9. Как выражается концентрация рабочего раствора?
10. Чем измеряют объем рабочего раствора?
11. Как устанавливают точную концентрацию рабочего раствора?
12. Раствор с точно известной концентрацией, приготовленный по точной навеске вещества - …
A. вторичный стандарт
B. стандарт – титр
C. определяемый раствор
D. первичный стандарт
13. Точка эквивалентности – это…
A. раствор вещества с точно известной концентрацией
B. постепенное смешивание веществ
C. момент, наступающий в ходе титрования, когда реагирующие вещества полностью прореагировали
D. вещество, меняющее окраску в определенных условиях
14. Как приготовить точный раствор по точно взятой навеске?
15. Как приготовить раствор из фиксанала?
16. Что такое точка эквивалентности?
17. Для какой цели при титровании применяются индикаторы?
18. Что такое точка конца титрования?
19. Что такое титрование с применением «свидетеля»?
20. Как подготовить бюретку к титрованию?
21. Расскажите, как выполняется титрование?
22. Что такое поправочный коэффициент?
23 Чем измеряют объем аликвоты?
24. Какое расхождение допускается при титровании параллельных образцов?
25.Формулы, используемые для расчетов в титриметрическом анализе:
A. Cн(В) = Cн(А)* V(А)
V(В)
B. V(В) = m/ρ
C. ρ=m/V(А)
D. Cн(А)*V(А)=Cн(B)*V(B)
26. Напишите формулу, по которой можно рассчитать титр раствора, зная его точную нормальную концентрацию.
27. Напишите формулу, по которой можно рассчитать титр рабочего раствора по определяемому веществу, если известна нормальная концентрация рабочего раствора.
28. Какой формулой рассчитать титр раствора? Что такое титр раствора?
29.Сколько граммов хлорида калия требуется для приготовления раствора массой 600 г с массовой долей 20% КСl?
30.В 500 г воды растворили 20г сульфата калия. Определите массовую долю К2SO4 в растворе.
31.Сколько граммов нитрата натрия потребуется для приготовления 200мл 0,2М раствора?
32. Определите молярность и нормальность серной кислоты в 450 мл которой содержится 10г Н2SO4.
33.Поправочный коэффициент 200мл 0,1 Н раствора натрия гидроксида равен 1,15. Приведите расчет доведения поправочного коэффициента (К) до нормы.
34.2000 мл 0,1 М раствора натрия гидроксида (Mr 40,0) приготовлены из навески массой 8,0 г (m). Поправочный коэффициент полученного раствора равен 0,85 (К). Приведите расчет доведения поправочного коэффициента (К) до нормы.
35.Для приготовления титрованного раствора 0.1 М раствора соляной кислоты в объеме 1000мл взяли кислоту в объеме 9мл. Поправочный коэффициент полученного раствора равен 1,25 (К). Приведите расчет доведения поправочного коэффициента (К) до нормы.
36.Поправочный коэффициент 800мл 0,1 Н раствора натрия гидроксида равен 0,75. Приведите расчет доведения поправочного коэффициента (К) до нормы.
 2020-08-05
2020-08-05 319
319






