1. В раскалённом состоянии реагирует с парами воды:
2Cr + 3H2O 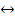 Cr2O3 + 3H2
Cr2O3 + 3H2
2. Хром растворяется в разбавленных сильных кислотах (HCl, H2SO4). В отсутствии воздуха образуются соли Cr2+, а на воздухе – соли Cr3+.
Cr + 2HCl → CrCl2 + H2
2Cr + 6HCl + O2 → 2CrCl3 + 2H2O + H2
3. Наличие защитной окисной плёнки на поверхности металла объясняет его пассивность по отношению к холодным концентрированным кислотам – окислителям. Однако при сильном нагревании эти кислоты растворяют хром:
2 Сr + 6 Н2SО4(конц) 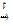 Сr2(SО4)3 + 3 SО2↑ + 6 Н2О
Сr2(SО4)3 + 3 SО2↑ + 6 Н2О
Сr + 6 НNО3(конц) 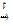 Сr(NО3)3 + 3 NO2↑ + 3 Н2О
Сr(NО3)3 + 3 NO2↑ + 3 Н2О
д) Получение
Получение меди
1. Восстановлением из оксидов углём или оксидом углерода (II): CuO + C 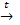 Cu + CO
Cu + CO
CuO + CO 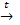 Cu + CO2
Cu + CO2
2. При электролизе солей меди: 2CuSO4 + 2H2O → 2Cu + O2 + 2H2SO4
Получение железа
1. Восстановлением из оксидов углём или оксидом углерода (II)
FeO + C 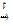 Fe + CO
Fe + CO
Fe2O3 + 3CO 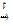 2Fe + 3CO2
2Fe + 3CO2
Получение хрома
1. Алюминотермия: Cr2O3 + 2Al 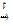 Al2O3 + 2Cr
Al2O3 + 2Cr
2. Восстановлением оксидов хрома оксидом углерода (II), водородом:
CrO + Н2 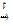 Cr + H2O
Cr + H2O
е) Применение меди, железа, хрома
– Напишите электронное строение атома меди
– Допишите уравнения реакций:
а) Fe + O2 б) Cr + H2SO4 в) Cu + Cl2
Тест по теме
1) Электронная формула 1s 2 2s2 2p6 3s2 3p6 3d2 4s2 принадлежит:
а) Zn б) Ti в) Cu г) Fe
Определите металл по следующим данным: светло-розовый цвет, тягучий, вязкий, легко прокатывается. Температура плавления 1083С. По проводимости электрического тока уступает лишь серебру.
а) Zn б) Ti в) Cu г) Fe
3) Степень окисления железа в формуле Fe2O3:
а) –2 б) + 4 в) + 2 г) + 3
4) Металлические свойства в ряду Ti Cr Fe:
а) уменьшаются б) увеличиваются в) не изменяются г) изменяются периодически
5) В схеме превращений Cr → CrCl3 → Cr(OH)3
Веществами x и y могут быть соответственно
а) Cl2, H2O б) Cl2, NaOH в) NaCl, KOH г) HCl, KOH
Выполните одно из трех заданий по своим возможностям
«3» - Допишите уравнения: а) Fe+ Cl2 б) Ti(IV) + O2 в) Zn + HNO3
«4» – Напишите уравнения реакций по схеме: Zn ZnO ZnSO4 Zn(NO3)2
«5» – Напишите уравнения реакций по схеме, заменив «X» и «Y» соответствующей формулой: Fe(III) «X» «Y» Fe2O3
Прочитать внимательно и сделать конспект.
Выполнить тест
 2020-08-05
2020-08-05 242
242







