Сборник задач
Для самостоятельного решения
по радиационной безопасности
УЧЕБНО-МЕТОДИЧЕСКОЕ ПОСОБИЕ
(для выполнения самостоятельных работ)
для студентов сельскохозяйственных специальностей
Гродно 2009
УДК 539.16(076)
ББК 22.383 Я73
С-23
Авторы: С.НСоколовская, Н.Н Забелин.
Рецензенты:доцент, доктор биологических наук И.Б. Заводник;
доцент, кандидат физико-математических наук
А.А. Денисковец.
Сборник задач для самостоятельного решения по радиа-
С-23 ционной безопасности: учебно-методическое пособие для
студентов сельскохозяйственных специальностей /
С.Н.Соколовская, Н.Н. Забелин.– Гродно: ГГАУ, 2009.– 58 c.
Учебно-методические пособие для выполнения контролируемых самостоятельных работ для студентов зооинженерного, агрономического, экономического, инженерно-технического факультетов, факультета ветеринарной медицины и факультета защиты растений.
УДК 539.16(076)
ББК 22.383 Я73
Рекомендовано учебно-методической комиссией факультета защиты растений УО «Гродненский государственный аграрный университет» (Протокол №4 от 23.06.2009)
© С.Н. Соколовская, Н.Н. Забелин, 2009
© УО «ГГАУ», 2009
ПРЕДИСЛОВИЕ
По своим масштабам и последствиям авария на Чернобыльской АЭС (ЧАЭС) представляет собой глобальную экологическую катастрофу. В результате катастрофы на ЧАЭС в атмосферу было выброшено большое количество радиоактивных веществ, суммарная активность которых – десятки миллионов Кюри (~  Ки), а также несколько тонн ядерного топлива. Из шести областей Беларуси пять загрязнено долгоживущими радиоизотопами (23% территории, на которой проживало на момент аварии 2,1 млн. человек - пятая часть населения Республики Беларусь).тиор Наибольшее радиоактивное загрязнение сельскохозяйственных угодий имеют Гомельская (45%), Могилевская (23%) и Брестская (23%) области.
Ки), а также несколько тонн ядерного топлива. Из шести областей Беларуси пять загрязнено долгоживущими радиоизотопами (23% территории, на которой проживало на момент аварии 2,1 млн. человек - пятая часть населения Республики Беларусь).тиор Наибольшее радиоактивное загрязнение сельскохозяйственных угодий имеют Гомельская (45%), Могилевская (23%) и Брестская (23%) области.
Поскольку последствия аварии на ЧАЭС многие годы будут влиять на состояние экономики нашей Республики, необходимы определенные знания для выполнения разнообразных работ во всех областях промышленности и сельского хозяйства Республики Беларусь, а также необходимо иметь четкое представление о степени радиационной опасности, которой могут подвергаться люди.
Курс радиационной безопасности введен во всех вузах нашей республики и поэтому уже написано немало учебных пособий для его успешного усвоения. Но имеется недостаточное количество сборников задач для практического закрепления изучаемого материала. Поэтому нами были составлены задачи, некоторые из которых базируются на фактических данных, взятых из опыта работы СЭС г. Гродно и других источников.
В задачнике предлагаются два раздела, содержащие основные формулы и примеры решения задач. Данный сборник задач предлагается использовать для контролируемой самостоятельной работы, решения задач на практических занятиях на зооинженерном, агрономическом, экономическом, инженерно-технологическом факультетах, факультете защиты растений и факультете ветеринарной медицины дневной и заочной форм обучения.
РАЗДЕЛ 1.
Ядерные превращения. Основной закон радиоактивного распада. Активность.
1.1. Энергия связи атомного ядра. Радиоактивность.
Ядерной ("планетарной") моделью атома называется такая модель структуры атома, в которой в центре атома расположено очень плотное ядро диаметром d=10-15м, в котором сосредоточен весь положительный заряд, а вокруг него по орбитам вращаются электроны. Абсолютное значение суммарного отрицательного заряда электронов равно положительному заряду ядра.
Атомное ядро любого химического элемента состоит из положительно заряженных протонов и не имеющих электрического заряда нейтронов. Протон и нейтрон являются двумя зарядовыми состояниями ядерной частицы, которая называется нуклоном. Заряд протона по абсолютной величине равен заряду электрона. Массовым числом А называется общее число нуклонов в ядре. Масса атомного ядра практически совпадает с массой всего атома, ибо масса электронов в атоме мала. Массовые числа нейтрона и протона одинаковы и равны единице. Электроны имеют отрицательный заряд, значение которого, принято считать, условно равным (-1), соответствует элементарному заряду (qe=  ).
).
Строение атома можно представить в виде схемы:
АТОМ


 ЯДРО ЭЛЕКТРОНЫ
ЯДРО ЭЛЕКТРОНЫ 
 qe =
qe = 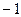
me = 0,00055 а.е.м., A=0
протоны р+ нейтроны n0
q p = +1 q n = 0
 =1,00728 а.е.м., A=1
=1,00728 а.е.м., A=1  = 1,00867 а.е.м., A=1
= 1,00867 а.е.м., A=1
Число протонов в ядре равно числу электронов в отрицательно заряженном oблаке и совпадает с порядковым номером (атомным номером) Z атома данного химического элемента в периодической системе Менделеева:
№пор= Z
или №пор.= Z = число р+ = число е -.
Чтобы определить число нейтронов надо от массового числа A отнять атомный номер Z: число нейтронов = N = A − Z
Дефект массы ядра:
 .
.
Энергия связи ядра выражается формулами:
 ,
,
если дефект массы Δm измеряется в кг или атомных единицах массы, соответственно, где с скорость света в вакууме.
 .
.
Радиоактивность -самопроизвольное превращение атомов одного элемента в атомы других элементов, сопровождающееся испусканием материальных частиц и жесткого электромагнитного излучения.
Альфа-излучение - представляет собой поток ядер гелия, cостоящих из двух протонов и двух нейтронов. Имеет статичеcкий электрический заряд равный +2, массовое число 4. Альфа-излучение обладает малой проникающей способностью (всего несколько сантиметров в воздухе и десятки микрон в биологической ткани). Поток альфа-частиц легко остановит даже лист бумаги. Альфа-частица обознчается симвалом -  .
.
Испускаемые при радиоактивном распаде  - частицы обладают скоростью 20 000 км/с и движутся в веществе прямолинейно, вызывая при этом ионизацию всех атомов на своем пути.
- частицы обладают скоростью 20 000 км/с и движутся в веществе прямолинейно, вызывая при этом ионизацию всех атомов на своем пути.
Бета-излучение является потоком заряженных частиц малой массы - электронов или позитронов. Позитрон - элементарная частица, имеющая массу электрона, но обладающая положительным элементарным зарядом.  - электрон обозначается символом -
- электрон обозначается символом - 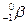 ,
,  - позитрон -
- позитрон -  .
.
Масса  -частицы в 7000 раз меньше массы
-частицы в 7000 раз меньше массы  -частицы, а скорость движения достигает 200000-270000 км/с.
-частицы, а скорость движения достигает 200000-270000 км/с.
Гамма-излучение (  ) было идентифицировано как жесткое (т.е. имеющее очень высокую энергию и короткую длину волны
) было идентифицировано как жесткое (т.е. имеющее очень высокую энергию и короткую длину волны  ) электромагнитное излучение.
) электромагнитное излучение.
Часто ядра атомов, образующиеся в процессе радиоактивных превращений, обладают избыточной энергией. Переходя в основное состояние, они излучают избыток энергии в виде гамма-квантов.
Все радиоактивные превращения всегда сопровождаются испусканием того или иного вида излучения, причем один акт распада дает только одну частицу – либо  , либо
, либо  , в результате чего данное ядро становиться ядром другого элемента. Образовавшееся ядро так же может быть радиоактивным и распадаться по тому или иному типу. Процесс последовательных ядерных превращений всегда заканчивается образованием стабильных изотопов.
, в результате чего данное ядро становиться ядром другого элемента. Образовавшееся ядро так же может быть радиоактивным и распадаться по тому или иному типу. Процесс последовательных ядерных превращений всегда заканчивается образованием стабильных изотопов.
1.2. Правило смещения.
Правило смещения точно указывает, какие именно превращения претерпевает химический элемент, испуская радиоактивное излучение.
Эмиссия альфа- и бета-частиц
Правило смещения можно пояснить с помощью ядерной модели атома, предложенной Резерфордом в 1911. Если неустойчивое ядро испускает бета-частицу (электрон), то заряд ядра увеличивается на единицу, а массовое число не изменяется. Следовательно, химический элемент перемещается на обну клетку вправо в периодической таблице Менделеева. При эмиссии альфа-частицы заряд ядра и массовое число образованного химического элемента уменьшаются на 2 и 4 единицы соответственно, т.е. в таблице Менделеева он перемещается влево на две клетки от исходного элемента.
Различают несколько видов самопроизвольных ядерных превращений, которые иначе называют типами ядерного распада.
а)  - распад – тип распада, связанный с испусканием ядром
- распад – тип распада, связанный с испусканием ядром  - частицы, в результате чего массовое число уменьшается на четыре единицы, а заряд (атомный номер) – на две единицы. Общей схемой
- частицы, в результате чего массовое число уменьшается на четыре единицы, а заряд (атомный номер) – на две единицы. Общей схемой  - распада является следующая:
- распада является следующая:
 ,
,
где Х – символ материнского изотопа, Y - дочернего ядра.
В качестве примера можно привести схему распада изотопа радия – 226 с образованием радона –222:
 .
.
В настоящее время известно около 200 радионуклидов, обладающих 
 - активностью. Почти все они относятся к концу периодической системы элементов и имеют значение Z
- активностью. Почти все они относятся к концу периодической системы элементов и имеют значение Z 
 83.
83.
б)  - распад существует двух видов:
- распад существует двух видов:  - электронный распад и
- электронный распад и  - позитронный распад.
- позитронный распад.
 - электронный распад вызывается самопроизвольным превращением в ядре одного нейтрона
- электронный распад вызывается самопроизвольным превращением в ядре одного нейтрона  в протон
в протон  , с испусканием электрона
, с испусканием электрона  и легчайшей электрически нейтральной частицы, называемой антинейтрино
и легчайшей электрически нейтральной частицы, называемой антинейтрино 
 :
:

Общая схема  - электронного распада следующая:
- электронного распада следующая:

При данном типе распада образуется дочернее ядро Y с таким же массовым числом А, но с атомным номером  на единицу большим, чем у материнского ядра
на единицу большим, чем у материнского ядра  .
.
В качестве примера можно привести схему распада трития:

При  - позитронном распаде происходит превращение в ядре одиночного протона в нейтрон с испусканием позитрона
- позитронном распаде происходит превращение в ядре одиночного протона в нейтрон с испусканием позитрона  и легчайшей электрически нейтральной частицы, называемой нейтрино
и легчайшей электрически нейтральной частицы, называемой нейтрино  :
:
 .
.
Общая схема  - позитронного распада следующая:
- позитронного распада следующая:
 .
.
В данном случае образуется дочернее ядро Y с таким же массовым числом A, но с атомным номером  меньше на единицу.
меньше на единицу.
Позитронный распад наблюдается главным образом для искусственно полученных радиоактивных изотопов. Примером  -позитронного распада является превращение фосфора – 30 в кремний – 30:
-позитронного распада является превращение фосфора – 30 в кремний – 30:
 .
.
в) Электронный захват – это тип распада, считающийся разновидностью  - распада. При электронном захвате ядро атома поглощает один из электронов собственной электронной оболочки (обычно с ближайшей к нему K - оболочки). При этом один из протонов превращается в нейтрон, что сопровождается испусканием нейтрино и образованием дочернего ядра Y с массовым числом A и атомным номером меньше на единицу.
- распада. При электронном захвате ядро атома поглощает один из электронов собственной электронной оболочки (обычно с ближайшей к нему K - оболочки). При этом один из протонов превращается в нейтрон, что сопровождается испусканием нейтрино и образованием дочернего ядра Y с массовым числом A и атомным номером меньше на единицу.
Электронный захват называют иначе K - захватом. Общей для такого распада является следующая схема:
 .
.
Примером K – захвата является превращение радиоактивного бериллия в стабильный литий или превращение калия в аргон:

или 
Электронный захват всегда сопровождается рентгеновским излучением за счет перехода более удаленного от ядра электрона на образовавшиеся свободное место в K слое.
1.3. Основной закон радиоактивного распада.
Основной закон радиоактивного распада утверждает, что за единицу времени распадается всегда одна и та же доля радиоативных ядер для данного вида радиоактивного изотопа:
Δ N = - λ 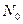 Δ t
Δ t
где Δ N- количество распадающихся атомов за промежуток времени Δ t; 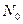 - начальное количество атомов;
- начальное количество атомов;  - постоянная распада. Знак минус указывает на убыль числа ядер в результате радиоактивного распада.
- постоянная распада. Знак минус указывает на убыль числа ядер в результате радиоактивного распада.
Постоянная распада характеризует долю ядер, распадающихся за единицу времени, имеет размерность с-1.
Из основного закона радиоактивного распада следует закон убыли во времени числа радиоактивных ядер:
 , (1)
, (1)
где  - количество радиоактивных ядер спустя время
- количество радиоактивных ядер спустя время  ;
;
 - математическая константа (
- математическая константа ( =2,72).
=2,72).
Для характеристики устойчивости ядер относительно радиактивного распада кроме λ, удобно использовать величину Т, называемую периодом полураспада.
Период полураспада –это время, в течение которого распадается половина начального количества ядер. Для различных радиоактивных изотопов период полураспада составляет от долей секунды до многих миллиардов лет. Причем у одного и того же элемента могут быть изотопы, значительно отличающиеся периодом полураспада. Так, например, радий – 226 имеет период полураспада 1620 лет, а радий – 219 – всего 10-3 с.
В зависимости от периода полураспада радиоактивные изотопы разделяются на долгоживущие (годы и более) и короткоживущие (секунды, дни).
Период полураспада Т и постоянная распада  связаны между собой следующим соотношением:
связаны между собой следующим соотношением:
 . (2)
. (2)
Среднее время жизни радиоактивного атома:
 . (3)
. (3)
Заменив в уравнении (1) величину  ее выражением, содержащим период полураспада, получим:
ее выражением, содержащим период полураспада, получим:
N= N0 · e -  t , (4)
t , (4)
которое также отражает основной закон радиоактивного распада.
Число ядер радиоактивного изотопа уменьшается со временем по экспоненциальному закону. За время  число нераспавшихся ядер уменьшается в 2 раза, за время
число нераспавшихся ядер уменьшается в 2 раза, за время  = 2Т – в 4 раза и т.д. Если общее время наблюдения
= 2Т – в 4 раза и т.д. Если общее время наблюдения  , где k – любое положительное число, то количество нераспавшихся ядер уменьшается в 2k раз, см. рисунок 1.
, где k – любое положительное число, то количество нераспавшихся ядер уменьшается в 2k раз, см. рисунок 1.
Используя данную закономерность можно представить основной закон радиоактивного распада в виде:
 или N =N0 /2- t/Т, (5)
или N =N0 /2- t/Т, (5)
где к =-t/T, т.е. количество периодов полураспада, прошедших с момента наблюдения.
Уравнением (5) удобно пользоваться в том случае, если время наблюдения сравнимо (по порядку величины) с периодом полураспада.
Зная период полураспада, можно легко определить долю оставшихся радиоактивных атомов через любое время.

Рис. 1
Например, если  , то
, то  , т.е. число радиоактивных атомов за это время уменьшилось в 1024 раза.
, т.е. число радиоактивных атомов за это время уменьшилось в 1024 раза.
Кроме того, уравнением (5) можно пользоваться для нахождения времени, через которое останется вполне определенная часть нераспавшихся атомов. Например, требуется рассчитать, через какое время количество атомов цезия – 137 уменьшится в 100 раз, если его период полураспада 30 лет.
Нам дано, что  .
.
Следовательно к = 6,7 и t = 6,7 . 30  200 лет.
200 лет.
1.4. Активность и единицы ее измерения. Удельная, объемная и поверхностная активность.
Активность характеризует интенсивность распада радиоактивного препарата и измеряется количеством распадающихся за одну секунду ядер в данном образце. Чем больше радиоактивных превращений происходит за одну секунду в образце, тем выше его активность и тем более интенсивное излучение он создает. Поэтому, содержание радионуклида в образце, а также уровень его загрязнения радионуклидами удобно измерять не единицами массы, а активностью.
Так, например, если взять N атомов какого-либо радиоактивного изотопа, характеризующегося постоянной распада  , то за время 1с будет распадаться
, то за время 1с будет распадаться  . N радиоактивных ядер. Тогда активность можно рассчитать по формуле:
. N радиоактивных ядер. Тогда активность можно рассчитать по формуле:
 (6)
(6)
т.к. N =  , где
, где  - масса образца,
- масса образца,  - молярная масса радионуклида,
- молярная масса радионуклида,  - число Авогадро, то
- число Авогадро, то
 . (7)
. (7)
Из выражения (7) следует, что активность образца тем выше, чем больше его масса.
С другой стороны, активность может быть определена по формуле:
 , (8)
, (8)
которая указывает, что активность не только зависит от массы изотопа, но и от его периода полураспада Т. Поэтому при равном количестве атомов радиоактивного изотопа в образцах самое интенсивное излучение будет создавать образец с более коротким периодам полураспада.
Международной единицей активности является 1 беккерель (1 Бк = 1  ). Внесистемной единицей измерения активности является 1 кюри (1 Ки = 37 млрд. расп/с или 3,7 . 1010 Бк), что соответствует активности 1г радия – 226.
). Внесистемной единицей измерения активности является 1 кюри (1 Ки = 37 млрд. расп/с или 3,7 . 1010 Бк), что соответствует активности 1г радия – 226.
Так как в результате распада число атомов N0 радионуклида уменьшается в соответствии с основным законом радиоак-тивного распада, то и активность образца также уменьшается со временем по этому закону:
 , (9)
, (9)
где A0 – начальная активность,
A -активность спустя время t.
Если время наблюдения t сравнимо по порядку величины с периодом полураспада Т, то можно использовать выражение:
 , (10)
, (10)
где к = t/T - число периодов полураспада.
Для характеристики уровня загрязнения радионуклидами каких-либо объектов используются следующие величины:
1. Удельная активность (Аm) – активность 1 кг твердых или сыпучих образцов. Аm =  .
.
2. Объемная активность (Аv) – активность 1 л или 1 м3 жидких или газообразных образцов.  .
.
3. Поверхностная активность ( ) – активность единицы площади поверхности.
) – активность единицы площади поверхности.  .
.
4. Молярная активность  - активность 1 моля вещества.
- активность 1 моля вещества.  .
.
Единицы активности и производные от них представлены в таблице 1.
Таблица 1.
 2020-08-05
2020-08-05 128
128







