Это сбраживание сахаристых веществ. Этанол получают брожением в присутствии дрожжей. Сущность брожения заключается том, что получаемая из крахмала глюкоза под действием ферментов распадается на спирт и СО2. результат этого процесса выражается схемой:
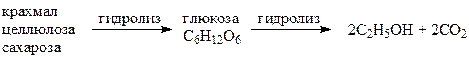
Физические свойства
Низкомолекулярные спирты (С1-С3) являются жидкостями с характерными запахом и вкусом и смешиваются с водой в любых соотношениях.
Температуры кипения спиртов не превышают 100°С, однако они выше чем температуры кипения эфиров или углеводородов, с такой же молекулярной массой.
Причиной этого являются межмолекулярные водородные связи, возникающие между водородными и кислородными атомами гидроксильных групп различных молекул спирта (происходит с участием неподеленных пар электронов кислорода).
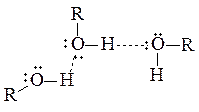
Хорошая растворимость спиртов в воде объясняется образованием водородных связей между молекулами спирта и воды.
Спирты с С11 и выше – твердые вещества.
Химические свойства спиртов.
Химические свойства спиртов обусловлены присутствием гидроксигруппы. Поэтому для спиртов характерны реакции:
1) с разрывом связи –СО-Н
2) с разрывом связи С-ОН
3) реакции окисления
1. Кислотно-основные свойства спиртов.
Спирты являются амфотерными соединениями. Они способны выступать в роли как кислот, так и оснований.
Они проявляют кислотные свойства при взаимодействии со щелочными металлами и щелочами. Водород гидроксила замещается на металл с образованием алкоголятов (которые легко разлагаются водой).
2C2H5OH + 2Na = 2C2H5ONa + H2
этилат натрия
Спирты более слабые кислоты, чем вода. Их кислотные свойства в убывают в следующем порядке: СН3ОН < СН3СН2ОН < (СН3)2СНОН < (СН3)3СОН. Т.е. разветвление углеродного скелета снижает кислотные свойства.
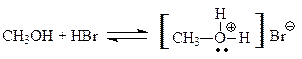
Свойства оснований спирт проявляют по отношению к кислотам. Сильнее минеральные кислоты протонируют атом кислорода ОН-группы:
 2020-09-24
2020-09-24 232
232








