РЕАКЦИИ
Вариант № 1
Дополните:
1. Окислительно-восстановительные реакции – это ______________________
2. Если алгебраическая величина степени окисления увеличивается, то протекает процесс _______, а с электронной точки зрения ________________
3. Окислитель в ходе реакции _______________, поэтому его алгебраическая величина степени окисления _________________________________________
4. Неметаллы (простые вещества) проявляют свойства _____, а с электронной точки зрения _______________________________________________________
5. Чем меньше алгебраическая величина стандартного окислительно-восстановительного потенциала (φоВ), тем сильнее выражены свойства _____
6. ЭДС = __, если ЭДС < 0, то окислительно-восстановительная реакция ____
7. В кислой среде: а) избыток кислорода в частице связываем ___________ с образованием _____________________________________________________
б) недостаток кислорода в частице берём из ________ с образованием _____________________________________________________
8. Для реакции K2Cr2O7 + KCl + H2SO4 → K2SO4 + Cr2(SO4)3 + Cl2 + H2O, если

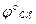 /
/ 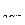 = + 1,36В,
= + 1,36В, 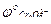 /
/ 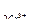 = 1,33В; ЭДС = ____, следовательно ____
= 1,33В; ЭДС = ____, следовательно ____
коэффициент перед восстановителем __________________________________
9. Установите соответствие:
| Окислительно-восстановительная реакция | Тип реакции |
| А. 3H2S + 2HNO3 → 3S + 2NO + 4H2O | 1. Диспропорционирования |
| Б. 5NaI + NaIO3 + 3H2SO4 → 3I2 + 3Na2SO4 +3H2O | 2. Внутримолекулярная |
| В. Cl2 + 2KOH → KCl + KClO + H2O | 3. Межмолекулярная |
| Г. 2KClO3 → 3O2 + 2KCl | 4. Сопропорционирования |
Выберите правильный вариант ответа:
10. Только восстановительные свойства проявляют вещества
1) KIO3 2) KIO2 3) KI 4) I2
11. Окислительно-восстановительную двойственность проявляют (два варианта ответа) ___________________________
1) N2 2) NH3 3) NaNO2 4) NaNO3
12. В уравнении реакции Сu + HNO3 (разб.) → ______________ коэффициент
перед окислителем _____________________________
1) 8 2) 10 3) 6 4) 4
13. В уравнении реакции, схема которой
Cu2S + HNO3 → Cu(NO3)2 + H2SO4 + NO + H2O,
сумма коэффициентов
1) 45 2) 50 3) 60 4) 52
Дайте полное решение задания, используя ионно-электронный метод.
Вариант № 2
Дополните:
1. Cтепень окисления – это ___________________________________________
2. Частица (атом, ион или молекула), отдающая электроны называется ______
3. Окислительно-восстановительные реакции называют сопряженными, так как __
4. Самые активные восстановители – это _______________________________
5. ЭДС рассчитывают по формуле _____________________________________
6. Сложные вещества, содержащие элемент в низкой степени окисления, играют роль _______________________________________________________
7. В щелочной среде: а) недостаток кислорода в частице берём из _____ с образованием _____________________________________________________
б) избыток кислорода в частице связываем _______ с образованием ______________________________________________________
8. Для реакции K2Cr2O7 + KBr + H2SO4 → K2SO4 + Cr2(SO4)3 + Br2 + H2O, если
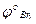 /
/ 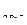 = + 1,06В,
= + 1,06В, 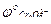 /
/ 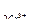 = 1,33В; ЭДС = ___, следовательно ____
= 1,33В; ЭДС = ___, следовательно ____
коэффициент перед восстановителем _________________________________
9. Установите соответствие:
| Окислительно-восстановительная реакция | Тип реакции |
А. 2Cu(NO3)2 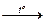 O2 + 4NO2 + 2CuO O2 + 4NO2 + 2CuO
| 1. Межмолекулярная |
| Б. 2NO + H2O → HNO3 + HNO2 | 2. Диспропорционирования |
| В. 4NH3 + 5O2 → 4NO + 6H2O | 3. Внутримолекулярная |
| Г. 2Na2S + Na2SO3 + 3H2SO4 → 3S + 3Na2SO4+3H2O | 4. Сопропорционирования |
 2020-10-10
2020-10-10 218
218








