Укажите номер правильного ответа:
1. Электронная формула 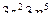 соответствует атому:
соответствует атому:
1) 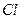 2)
2) 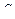 3)
3) 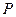 4)
4) 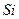
2. Пространственная конфигурация угловая соответствует частицам (два варианта ответа):
1)  2)
2) 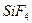 3)
3) 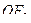 4)
4) 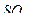
3. Окисление аммиака протекает по уравнению:
4NH3 + 3О2 → 2N2 + 6H2О ∆Н = – 1528 КДж
г г г
∆Н0обр. КДж/Моль 0 0 −285,84
Теплота образования аммиака (∆Н0 обр. NH3) равна:
1) − 92,15 КДж/Моль 3) − 46,76 КДж/Моль
2) 92,15 КДж/Моль 4) + 46,76 КДж/Моль
4. Если энтальпия образования СO2 равна (− 393,5 КДж/моль), то количество теплоты, выделяемое при сгорании 24 г углерода, равно ___ КДж
1) 196,8 2) 305,3 3) 600,2 4) 787,0
5. При проведении обратимой реакции 2NО(г) + О2 (г) ↔ 2NО2 (г)
начальные концентрации NО и О2 были соответственно равны 1,2 и 0,8 моль/л, а в состоянии равновесия концентрация NО2 составила 0,4 моль/л, тогда константа равновесия равна _____________________________________
1) 0,42 2) 0,84 3) 4 4) 8
Часть В. Выполните тестовые задания
Дополните:
1. Атом – это ______________________________________________________
2. Спиновое квантовое число обозначается буквой _____________, принимает значения _________________________, характеризует ___________________
3. В группах (главных подгруппах А) сверху вниз радиус атома ___________, энергия ионизации ______, ОЭО _________, увеличиваются свойства ______
4. Энергия связи – это _______________________________________________
5. Число 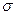 – связей в молекуле
– связей в молекуле 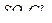 равно ___________________________
равно ___________________________
6. Первый закон термодинамики имеет математическое выражение ________
7. Критерием самопроизвольного протекания реакций (для реальных систем) является величина, называемая _____, рассчитывается по формуле _________
8. Правило Вант Гоффа формулируется ______________. Его математическое выражение имеет вид _______________________________________________
9. Математическое выражение Кр для реакции: 2SO2 (г) + О2 (г) ↔ 2SO3 (г) имеет вид: _________________________________________________________
 2020-10-10
2020-10-10 138
138








