Термодинамические характеристики газа. Эффект Джоуля – Томпсона. Способы определения дифференциального и интегрального дроссель эффекта. Эффект Ранка.
В технологических расчётах добычи и транспорта газа часто пользуются основными термодинамическими характеристиками природного газа: теплоемкостью, энтропией, энтальпией, теплотой сгорания, теплообменом, теплопроводностью.
Теплоёмкость. Теплоёмкостью называют количество теплоты, необходимое для нагревания единицы массы или объёма вещества на 1° С.
Отношение теплоёмкости в массе системы М называется удельной теплоёмкостью: с = С/М, а отношение теплоемкости к количеству вещества – молярной теплоёмкостью:
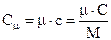 . (1)
. (1)
Единицей количества теплоты, работы, энергии в системе СИ является джоуль (Дж). Джоуль - работа силы 1 Н при перемещении ею тела на расстоянии 1 м в направлении действия силы:
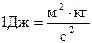
Теплоёмкость выражается в Дж/К, удельная теплоёмкость – в Дж/(кг·K), молярная теплоёмкость – в Дж/(моль К).
Теплоёмкость природных газов зависит от химического состава и состояния, а также от процесса сообщения им теплоты. В адиабатическом процессе С = 0, в изобарическом С = Ср, в изохорическом С = Сv.
Для газов обычно различают теплоёмкости при постоянном объёме Сv и постоянном давлении Ср.
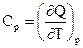
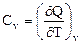 (2)
(2)
где Р = const и V = const.
Теплоёмкости при постоянном объёме Сv связана с процессом, характеризующимся тем, что при неизменности объёма вся энергия, сообщаемая газу в форме теплоты, затрачивается на увеличение внутренней энергии газа. Ср связана с процессом, характеризующимся тем, что, нагревая тело, предоставляют ему возможность расширяться при неизменном давлении. Таким образом, часть сообщенной телу теплоты идет на производство работы расширения. Поэтому Ср > Сv.
Для идеальных газов между Ср и Сv существует следующее соотношение в [кал/моль·°С]:
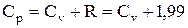 (3)
(3)
где R - газовая постоянная.
В области давлений, где газы считаются идеальными, значения теплоёмкостей постоянны. Однако для реальных газов значения теплоёмкости изменяются в зависимости от давления и температуры.
Для смеси газов теплоёмкость определяется по сумме теплоемкости входящих компонентов по формуле
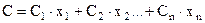 (4)
(4)
где С1, С2…Сn - теплоёмкости отдельных компонентов смеси;
х1, х2…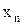 содержание компонентов в долях единицы.
содержание компонентов в долях единицы.
Отношение теплоёмкости 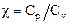 называют показателем адиабаты.
называют показателем адиабаты.
Для практических целей с достаточной точностью можно использовать формулу следующего вида:
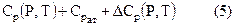
где Ср – изобарная теплоёмкость;
Ср ат – теплоёмкость при атмосферном давлении и заданной температуре, определяемая из рисунка 1 и расчётным путём.
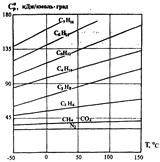
Рисунок 1. Зависимость изобарной молярной теплоёмкости природных газов 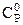 от температуры при давлении Р = 0,1 МПа
от температуры при давлении Р = 0,1 МПа
Аналитически Ср ат определяется по формуле следующего вида
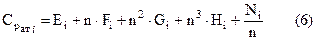
где Еi, Fi, Hi, Ni – коэффициенты, определяемые из таблицы 1;
n = Т/100;
Т – температура, при которой определяется 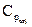 .
.
Изотермическая поправка на давление ΔСр может быть определена как графическим путем, так и расчётным, например, по формуле следующего вида
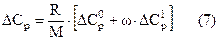
где R – газовая постоянная, равная R = 1,986 ккал/моль;
М – молекулярная масса газа;
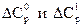 - поправки на теплоёмкость, зависящие от приведенных давления и температуры, определяемые по зависимостям, приведенным на рисунках 2 и 3.
- поправки на теплоёмкость, зависящие от приведенных давления и температуры, определяемые по зависимостям, приведенным на рисунках 2 и 3.
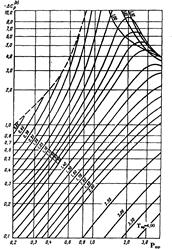
Рисунок 2. Зависимость поправочной 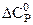 от приведенных давления и температуры
от приведенных давления и температуры
Величина 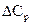 может быть определена и без учёта фактора ацентричности ω по графической зависимости приведенной на рисунке 4.
может быть определена и без учёта фактора ацентричности ω по графической зависимости приведенной на рисунке 4.

Рисунок 3. Зависимость поправочной величины 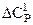
от приведенных давления и температуры
Таблица 1. Значения коэффициентов для зависимости (6)
| Компоненты | Молек. масса 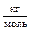 |  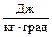 | 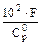 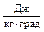 | 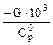 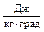 | 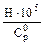 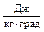 | 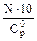  |
| Метан | 16,04 | 58522,25 | 15215,04 | - 2947,67 | 18575,95 | |
| Этан | 30,07 | 62557,49 | 25663,79 | 36001,45 | 3343,11 | |
| Пропан | 44,09 | 66328,12 | 32767,24 | 62295,40 | - 782,07 | |
| Бутан | 58,12 | 65812,73 | 33182,44 | 33182,44 | 3,8610 | |
| Изобутан | - | 68152,31 | 36790,16 | 75903,33 | - 1685,56 | |
| Пентан | 72,15 | 65762,49 | 33814,98 | 66951,12 | - 112,122 | |
| Изопентан | - | 66838,91 | 34687,09 | 69556,98 | - 1530,40 | |
| Гексан | 86,16 | 66060,17 | 34773,68 | 70914,34 | - 456,22 | |
| Гептан | 100,20 | 66040,07 | 35091,50 | 31839,23 | - 503,65 | |
| Октан | 114,22 | 66094,50 | 35466,84 | 73861,01 | - 561,57 | |
| Нонан | 128,26 | 65986,06 | 35489,58 | 74039,37 | - 522,39 | |
| Декан | 142,29 | 65991,50 | - 35677,77 | 74788,39 | - 549,49 | |
| Кислород | 32,00 | 21621,09 | 16458,14 | 49445,62 | 125051,12 | |
| Водород | 2,02 | 330368,33 | 294527,51 | 14165,32 | 200717,79 | |
| Вода | 18,02 | 40147,27 | 27801,52 | 79225,56 | 26409,75 | |
| Гелий | 4,00 | 5191,632 | ||||
| Аргон | 39,95 | 520,712 | ||||
| Криптон | 83,80 | 248,696 | ||||
| Хлористый водород | 36,46 | 741,248 | 1447,19 | 187,48 | 51,33 | 313,63 |
| Сероводород | 64,86 | 19097,88 | 154,95 | 43953,78 | 5109,53 | |
| Двуокись серы | 34,08 | 24379,36 | 16676,57 | 45818,66 | 11682,30 | |
| Азот | 28,01 | 21745,15 | 16129,31 | 45183,53 | 15429,99 | |
| Двуокись углерода | 44,01 | 25745,76 | 19428,01 | 53589,36 | 6924,42 | |
| Окись углерода | 28,01 | 22065,65 | 16193,91 | 44592,35 | 15197,54 |
Фактор ацентричности молекул газа ω определяется аналогично, как и при определении коэффициента сверхсжимаемости Z.
Величину Ср(Р, Т) можно рассчитать по формуле вида
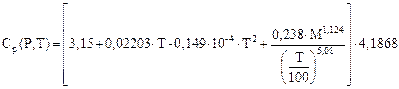 (8)
(8)
где Т - температура газа, 0С;
М – молекулярная масса газа.
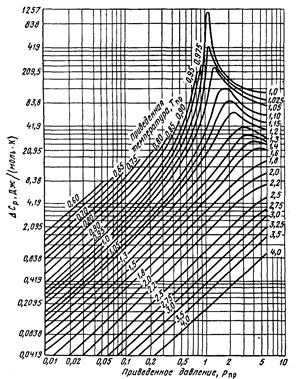
Рисунок 4Зависимость изотермической поправки изобарной молярной теплоёмкости 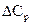 от приведенных абсолютных давления Рпр и температуры Тпр
от приведенных абсолютных давления Рпр и температуры Тпр
Энтропия. Энтропия S тела - величина, изменение которой равно отношению изменения количества теплоты к абсолютной температуре тела:
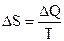 (9)
(9)
где ∆S - изменение энтропии системы, если ей сообщается теплота ∆Q при температуре T.
Единицей измерения энтропии является джоуль на Кельвин (Дж/К).
Удельная энтропия в Дж/К
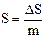 (10)
(10)
где m - масса тела.
Энтальпия. Свойство вещества, которое позволяет судить о количестве теплоты, требующейся для изменения его температуры, называется энтальпией Н.
Иными словами, энтальпия- это функция состояния вещества, определяемая равенством:
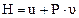 (11)
(11)
где u - внутренняя энергия, рассчитанная на единицу массы вещества;
Р - давление;
ν - удельный объём.
В термодинамике различают два процесса, в которых подведенное тепло равно разности энтальпий:
- расширение при постоянном давлении;
- скорость процесса небольшая, поэтому изменением кинетической энергии можно пренебречь.
Изменение энтальпии от температуры для однофазного состояния вещества выражается удельной теплоёмкостью при постоянном давлении Ср:
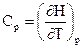 (12).
(12).
Влияние давления выражается следующим образом
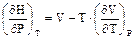 (13)
(13)
гдеV– объём газа.
Для идеальных газов изменение энтальпии с изменением давления выражается как
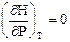 .
.
Для реальных газов изменение энтальпии с изменением давления выражается, как известно через коэффициент сжимаемости z:
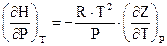 (14)
(14)
Внутренняя энергия идеального газа зависит только от температуры. Зависимость внутренней энергии реального газа от объёма и давления была выяснена Джоулем и Томсоном.
На рисунке 5 приведена графическая зависимость позволяющая оценивать влияние давления и температуры на энтальпию природного газа.

Рисунок 5 - Энтальпийная диаграмма природного газа
 2014-02-05
2014-02-05 3591
3591








