Контрольные вопросы
Задание на СРСП
Сроки выполнения–третья неделя, виды заданий – реферат.
Задание на СРС
1. Метастабильное состояние
2. Метастабильное равновесие
3. Химическое равновесие в гетерогенных реакциях.
Д [2] гл. VII, 220-224с.
Д [2] гл. VIII, 269-272с.
О [2] гл. 11, 313-315с.
1. Вычислить константу равновесия реакции:
NH3(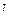 ) + HCl (
) + HCl (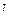 ) = NH4Cl(K)
) = NH4Cl(K)
2. Вывести уравнения изобары и изохоры химической реакции.
Д [2] гл. VIII, 266-268с.
Д [2] гл. VIII, 269-272с.
А. Для письменного контроля:
1. Какое состояние называется равновесным?
2. Что показывает значение абсолютной энтропии?
3. Каков смысл химического потенциала?
4. Каким путем рассчитать химическое равновесие?
5. Что обозначают уравнения изобары и изохоры реакции?
1. Характерная черта химического равновесия:
а) динамичность;
б) постоянность;
в) непостоянность;
г) нединамичность.
2. Определите условия равновесия для обратимых изобарно-изотермических процессов:
а) dG = 0;
б) dF = 0;
в) dV = 0;
г) dG = const.
3. При химическом равновесии:
а) Vnp = Vобр;
б) Vnp > Vобр;
в) Vnp < Vобр;
г) P = const.
4. Укажите энергию Гиббса:
а) dG = VdP – SdT;
б) dF = - pdV – SdT;
в) dV = 0;
г) dH = nCpdT.
5. Определите константу равновесия, выраженную через парциальное давление:
а) КР;
б) КС;
в) Кт;
г) К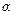 .
.
6. Определите условие равновесия для обратимых изохорно-изотермических процессов:
а) dF = 0;
б) dG = 0;
в) dV = 0;
г) dG = const.
7. Укажите энергию Гельмгольца:
а) dF = - pdV – SdT;
б) dG = VdP – SdT;
в) dV = 0;
г) dH = nCP · dT.
8. Уравнение изобары реакции показывает, что процесс происходит:
а) при постоянном давлении;
б) при постоянном объеме;
в) при постоянной концентрации;
г) при повышении температуры.
9. Определите константу равновесия, выраженную через концентрацию:
а) Кс;
б) КР;
в) Кt;
г) K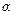 .
.
10. Гомогенная система состоит из веществ:
а) находящихся в одной фазе;
б) находящихся в разных фазах;
в) находящихся в постоянном объеме;
г) находящихся в разных объемах.
 2014-02-02
2014-02-02 691
691








