Например, если в раствор СН3СООН добавить ацетат натрия CH3COONa, то за счет диссоциации соли концентрация ацетат-ионов СН3СОО– резко увеличится. В соответствии с принципом Ле Шателье это приведет к смещению равновесия процесса
СН3СООН 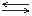 СН3СОО– + Н+
СН3СОО– + Н+
в левую сторону. Аналогичный эффект наблюдается, если в раствор СН3СООН добавить небольшое количество сильной кислоты.
Таким образом, диссоциация слабой кислоты подавляется в присутствии собственной соли или сильной кислоты. То же можно сказать и о слабом основании, диссоциация которого будет подавляться в сильнощелочной среде или в присутствии соли, содержащей одноименный катион.
При добавлении большого количества соответствующего сильного электролита слабый электролит практически не будет диссоциировать.
Существует количественная связь между константой и степенью диссоциации слабого электролита и его концентрацией в растворе, называемая законом разбавления Оствальда .
Для бинарного электролита, молекула которого распадается только на 2 иона, можно показать, что
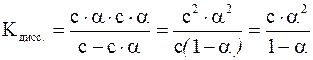
где с – исходная молярная концентрация электролита в растворе; α – степень диссоциации электролита; с ∙ α – концентрация распавшихся молекул электролита и образовавшихся при этом ионов.
 Вильгельм Фридрих Оствальд (1853 – 1932).
Вильгельм Фридрих Оствальд (1853 – 1932).
Родился в Риге. Учился в Дерптском университете, здесь же в 1878 г. получил степень доктора. С 1882 г. был профессором Рижского университета. С 1887 г. перешел на кафедру физической химии в Лейпциге, где работал до 1928 г.
В. Оствальд изучал электрическую проводимость органических кислот. Познакомившись с работами С. Аррениуса, он стал его сторонником. В. Оствальд внес существенный вклад в теорию электролитической диссоциации. В частности, он предложил свой известный закон разбавления, показал, что аналитические реакции в растворах следует рассматривать как ионные, и объяснил цвет растворов многих веществ специфической окраской ионов. В. Освальду принадлежат также исследования по катализу.
Так как степень диссоциации слабых электролитов мала, то можно пренебречь этой величиной в знаменателе. Тогда K» c·a2, откуда 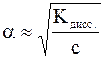 или учитывая, что
или учитывая, что 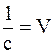 (разведение или разбавление раствора), то
(разведение или разбавление раствора), то 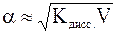 .
.
Для электролитов, молекулы или формульные единицы которых распадаются на большее число ионов, закон разбавления Оствальда носит более сложный характер.
 2014-02-02
2014-02-02 1338
1338
