Основными источниками электрического поля корабля являются электрохимические процессы взаимодействия, разнородных по своим электрохимическим характеристикам, металлических деталей подводной части корпуса; например, возникновение в морской воде тока гальванической пары «стальной корпус корабля – бронзовые гребные винты».
В 1950 году были опубликованы сведения об электрическом поле эскадренного миноносца “Фаренхольм”. Указывалось, что это поле создавалось в результате возникновения в морской воде тока (величина которого могла достигать нескольких ампер) гальванической пары стальной корпус корабля – бронзовые гребные винты.
Основы физико-химических процессов, обуславливающих электрическое поле корабля, связаны с:
· металлами подводной части корпуса, включая гребной винт;
· морской водой, активной участницей в работе гальванических пар корпуса;
· реакциями вытеснения одних металлов другими из растворов солей (на них основано действие большинства гальванических элементов).
Приведем краткую характеристику этих составляющих.
1. Подводная часть корпуса корабля, в основном, изготовлена из судостроительных сталей и сплавов цветных металлов. Сталью мы называем сплавы железа с углеродом и другими элементами. Состав сталей определяет их подразделение на углеродистые и легированные. В кораблестроении применяется малоуглеродистая сталь с содержанием углерода от 0,017 до 0,22 %, носящая название судостроительной стали. Широкое применение имеют также судостроительные стали со специальными присадками. В качестве вводимых (легирующих) в сталь присадок применяют: никель, титан, медь, марганец и др. Судостроительная сталь, которая содержит специально введенные один или несколько легирующих элементов называется специальной или легированной. В зависимости от процента содержания легирующих элементов, она подразделяется на низколегированную (в сумме не более 2%), среднелегированную (от 2 до 5%) и высоколегированную (свыше 5%)
Легированные стали, применяются для изготовления отдельных конструктивных узлов подводной части корпуса корабля: для изготовления гребных и дейдвудных валов может идти нержавеющая сталь (или для плакирования их); для изготовления якорных клюзов, барабанов, лебедок, шпилей и др., применяют износоустойчивые стали.
Судостроительные стали применяются в виде проката (листового, полосового, профильного). Листовая сталь используется для наружной обшивки корпуса корабля. Профильный прокат употребляется для изготовления набора корпуса корабля. Литье и поковки идут на изготовление форштевней, ахтерштевней, кронштейнов гребных валов, якорей и т.д.
Некоторые корпусные конструкции изготовляются как из цветных металлов, так и сплавов. Так, для предохранения от коррозии стального корпуса корабля применяется протекторная защита. В качестве протекторов используется цинк, магний, магниевые сплавы, алюминиево-никелевые сплавы. Широко используются сплавы цветных металлов: для изготовления забортной арматуры применяют морскую латунь, в состав которой входят; медь (69-71%), цинк (28-30%) и олово (1-1,5%); для изготовления гребных винтов применяют специальную латунь, представляющую собой медно-цинковый сплав с небольшими добавлениями алюминия, никеля, марганца, олова и свинца.
Алюминиевые сплавы находят применение для изготовления корпусов малых кораблей (торпедных и ракетных катеров и др.).
2. Корабль плавает в морской воде, представляющей собой раствор различных солей. Жидкие или твердые вещества, в которых присутствуют в заметной концентрации ионы, обуславливающие ионную проводимость по ним электрического тока, носят название электролитов. При растворении электролитов их молекулы, под влиянием электрического поля молекул растворителя, распадаются на отдельные положительно и отрицательно заряженные ионы. Этот процесс называется электролитической диссоциацией. Электролиты, хорошо диссоциирующие на ионы, получили название сильных (в отличие от слабых электролитов, образующих в водных растворах незначительное число ионов). К сильным электролитам относятся почти все соли и такие кислоты, как соляная, азотная, серная и некоторые другие, а также щелочи (кроме 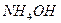 ).
).
Морская вода практически стабильна относительно своего процентного солевого состава. Изменение в солености в разных районах океанов связано с пропорциональным уменьшением или увеличением содержания всех солей, входящих в раствор, что иллюстрируется табл. 4.
Из табл. 4 видно, что морская вода является сложным раствором сильных электролитов, относительное содержание ионов в котором постоянно. Соленость ее (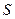 ), выражается в промиллях (‰).
), выражается в промиллях (‰).
Таблица 4 Основной солевой состав морской воды
| Соль | Содержание соли | Характеристика электролита |
 |  | Сильный |
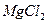 | 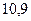 | Сильный |
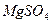 | 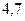 | Сильный |
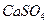 | 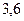 | Сильный |
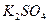 | 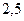 | Сильный |
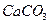 | 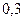 | Сильный |
 | 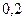 | Сильный |
 2014-02-02
2014-02-02 2155
2155
