Осмос
При разделении двух растворов различной концентрации или раствора и чистого растворителя полупроницаемой перегородкой (мембраной) возникает поток растворителя от меньшей концентрации к большей, выравнивающий концентрацию. Этот процесс называется осмосом.
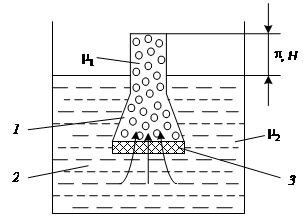 Осмос характерен не только для истинных, но и для коллоидных растворов. Схема осмоса приведена на рис. 9.4. В сосуд, имеющий полупроницаемую перегородку 3, помещен истинный или коллоидный раствор 1. Полупроницаемая перегородка способна пропускать дисперсионную среду или растворитель, но является препятствием для коллоидных частиц или растворенных веществ. С наружной стороны перегородки находится чистая жидкость (растворитель) 2. Концентрация раствора по обе стороны полупроницаемой перегородки будет различной. Внутри сосуда 1 часть раствора занимают молекулы растворенного вещества или частицы дисперсной фазы, поэтому концентрация жидкости (растворителя или дисперсионная среда) там будет меньше, чем в емкости 2 с чистой жидкостью.
Осмос характерен не только для истинных, но и для коллоидных растворов. Схема осмоса приведена на рис. 9.4. В сосуд, имеющий полупроницаемую перегородку 3, помещен истинный или коллоидный раствор 1. Полупроницаемая перегородка способна пропускать дисперсионную среду или растворитель, но является препятствием для коллоидных частиц или растворенных веществ. С наружной стороны перегородки находится чистая жидкость (растворитель) 2. Концентрация раствора по обе стороны полупроницаемой перегородки будет различной. Внутри сосуда 1 часть раствора занимают молекулы растворенного вещества или частицы дисперсной фазы, поэтому концентрация жидкости (растворителя или дисперсионная среда) там будет меньше, чем в емкости 2 с чистой жидкостью.
 За счет диффузии жидкость из области более высокой концентрации будет самопроизвольно перемещаться в область меньшей концентрации, т.е. из емкости 2 в емкость 1. Это перемещение на рис. 9.4 показано стрелками. Оно обусловлено тем, что число ударов молекул на мембрану растворителя со стороны чистого или более разбавленного раствора больше, чем со стороны раствора. Это избыточное число ударов и является причиной перемещения растворителя через поры мембраны туда, где его меньше, т.е. в область истинного или коллоидного раствора. Подобное объяснение переноса жидкости является кинетической трактовкой причины осмоса.
За счет диффузии жидкость из области более высокой концентрации будет самопроизвольно перемещаться в область меньшей концентрации, т.е. из емкости 2 в емкость 1. Это перемещение на рис. 9.4 показано стрелками. Оно обусловлено тем, что число ударов молекул на мембрану растворителя со стороны чистого или более разбавленного раствора больше, чем со стороны раствора. Это избыточное число ударов и является причиной перемещения растворителя через поры мембраны туда, где его меньше, т.е. в область истинного или коллоидного раствора. Подобное объяснение переноса жидкости является кинетической трактовкой причины осмоса.
Существует еще и термодинамическое объяснение осмотического переноса. Химический потенциал чистой жидкости m2 превышает химический потенциал этой же жидкости в растворе μ1. Процесс идет самопроизвольно в сторону меньшего химического потенциала до тех пор, пока не произойдет выравнивание химических потенциалов, т.е. до достижения условия μ2 = μ2.
В результате перемещения жидкости в емкости 1 создается избыточное давление p, называемое осмотическим. Растворитель, проникающий в область раствора 1, поднимает уровень жидкости на высоту Н, что компенсирует давление чистого растворителя в сторону раствора. Наступает момент, когда вес столба жидкости в области раствора уравнивается давлением растворителя. Дальнейшего изменения уровня уже не произойдет, а вес столба жидкости над уровнем растворителя будет служить мерой осмотического давления.
Осмотическое давление возникает при движении чистого растворителя в сторону раствора или от более разбавленного раствора в сторону более концентрированного, а следовательно, связано с разностью концентраций растворенного вещества и растворителя. Осмотическое давление — это такое избыточное давление над раствором, которое необходимо для исключения переноса растворителя через мембрану.
Осмотическое давление равно тому давлению, которое производила бы дисперсная фаза (растворенное вещество), если бы она в виде газа при той же температуре занимала тот же объем, что и коллоидная система (раствор). Осмотическое давление не есть проявление какого-либо внешнего воздействия. Оно возникает самопроизвольно, как следствие молекулярно-кинетических свойств дисперсионной среды.
Высота подъема жидкости Н над первоначальным положением раствора количественно определяет осмотическое давление, которое обычно обозначают через π.
Для чистого растворителя и идеального раствора неэлектролитов осмотическое давление выразится формулой
πV = RT In(1–x), (9.8, а)
где V — молярный объем растворителя; х — молярная доля растворенного вещества.
В случае разбавленных растворов неэлектролитов, когда x << 1, можно записать следующее уравнение:
πV = nRT. (9.9)
Согласно определению осмотическое давление можно найти из уравнения состояния (9.9), где n — число молей растворенного вещества.
Если масса растворенного вещества равна q, а молекулярная его масса М, то n = q/М; тогда согласно уравнению (9.9) осмотическое давление равно
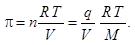 (9.10)
(9.10)
Величина q/V есть массовая концентрация растворенного вещества, поэтому осмотическое давление можно определить при помощи следующей формулы
π = (v м / M)RT. (9.11)
Формула (9.11) является основной для определения осмотического давления. Она позволяет найти зависимость осмотического давления от размеров частиц растворенного вещества. Для этой цели массу дисперсной фазы можно представить в виде
M = mNA, m = (4 / 3)πr3ρ, (9.12)
где m, r — молекулярная масса и радиус частиц дисперсной фазы; ρ — плотность материала частиц.
Подставив в уравнение (9.11) значение М из формулы (9.12), получим
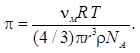 (9.13)
(9.13)
Формулу (9.13) используют для определения осмотического давления коллоидных растворов.
Осмотическое давление коллоидных растворов (высокодисперсных систем с жидкой дисперсионной средой) незначительно и составляет всего 1 мм водяного столба или даже меньше (1 мм водяного столба равен примерно 10 Па). Размеры и концентрация частиц в результате агрегации и других процессов могут изменяться. В связи с этим осмотическое давление для высокодисперсных систем непостоянно.
Из формулы (9.13) следует, что осмотическое давление прямо пропорционально концентрации дисперсной фазы и обратно пропорционально размеру частиц этой фазы в третьей степени. Чем меньше размер частиц, тем значительнее осмотическое давление. Если, например, для коллоидных растворов диаметр частиц составляет 100 нм, а размер молекул растворенного вещества — 1 нм, то осмотическое давление молекулярных растворов по сравнению с коллоидными будет в 106 раз больше. Осмотическое давление истинных растворов значительно превышает осмотическое давление коллоидных растворов и составляет для сока сахарной свеклы 35∙105 Па, экстракта кофе — 25∙105 Па, фруктовых соков — 1,5∙105 Па, 6%-го раствора сахара — 60∙105 Па.
Таким образом, осмос, как и все молекулярно-кинетические свойства, характерен для высокодисперсных систем, размеры частиц дисперсной фазы которых не превышают 0,1 мкм.
ОПТИЧЕСКИЕ СВОЙСТВА ДИСПЕРСНЫХ СИСТЕМ
Оптические свойства дисперсных систем обусловлены взаимодействием электромагнитного излучения, обладающего определенной энергией, с частицами дисперсной фазы. Особенности оптических свойств дисперсных систем определяются природой частиц и их размерами, соотношением между длиной волны электромагнитного излучения и размерами частиц. Одним из наиболее характерных оптических свойств дисперсных систем является рассеяние света.
В зависимости от свойств частиц дисперсной фазы и их размеров свет, проходя через дисперсную систему, может поглощаться, отражаться или рассеиваться. Последствия воздействия света на дисперсные системы (интерференция, дифракция, поляризация, преломление и отражение света и др.) определяются законами геометрической оптики.
Дисперсные системы способны к рассеянию света. В результате рассеяния проходящий через коллоидный раствор луч света становится видимым (эффект Тиндаля). Этот вид рассеяния называют опалесценцией. Для молекулярных и ионных растворов подобный эффект не наблюдается.
Способностью к светорасceиванию обладают не только частицы, но и ассоциаты молекул, макромолекулы и включения, нарушающие однородность среды. Рассеяние заключается в преобразовании света веществом, которое сопровождается изменением направления света.
Схематически рассеяние света можно представить следующим образом:
| Падающий свет с частотой ν | + | Молекулы высокодисперсных частиц (атомы) | → | Поляризация молекул (атомов) и возникновение диополей с пере- менным моментом | → | Излучение кванта с частотой ν1 |
Световая волна вызывает поляризацию молекул не проводящих и не поглощающих свет частиц; возникающий при этом дипольный момент m определяется по уравнению
µ = αE,
где α— поляризуемость; Е — напряженность возбужденного электрического поля, образованного падающим светом.
Возникающие диполи колеблятся с частотой падающего света и создают вторичное излучение во всех направлениях. В однородной среде свет, излучаемый всеми диполями вследствие интерференции*, распространяется прямолинейно. В неоднородной среде, к которой относятся высокодисперсные системы с различным показателем преломления фазы и среды, интерференция отсутствует, и испускается нескомпенсированное излучение в виде рассеянного света. Если энергия поглощенного кванта света (hu) равна энергии испускаемого кванта (hν1), то рассеяние будет рэлеевским, или упругим.
Oно реализуется в том случае, когда размеры частиц дисперсной фазы намного меньше длины волны света λ, а именно
а < 0,1l. (8.1)
Длина волны видимого света колеблется в пределах 380-760 нм. Поэтому условие (8.1) справедливо для частиц дисперсной фазы, размеры которых не превышает 76 нм, т.е. для высокодисперсных систем.
Теорию рассеяния света развил английский физик Рэлей, поэтому рассеяние света высокодисперсными системами при соблюдении условия (8.1) называют рэлеевским. еще раз подчеркнем, что характерной особенностью рэлеевского рассеяния является равенство энергий испускаемого и падающего квантов света (т.е. равенство частот падающего и рассеянного света).
В результате рассеяния интенсивность падающего света J0 изменяется и будет характеризоваться величиной Jp, которая, согласно Рэлею, определяется по формуле
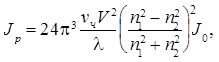 (8.2)
(8.2)
где νч — численная концентрация дисперсной фазы; V — объем частиц (для шарообразной частицы он равен 4pr3/3; r — радиус частиц); λ — длина волны падающего света; n1, n2 — показатели преломления дисперсной фазы и дисперсионной среды.
Рэлеевское рассеяние света характерно для неэлектропроводных, оптически однородных и прозрачных частиц (белые золи). При этом размер частиц должен соответствовать условию (8.1), частицы иметь изомермическую форму, а расстояние между ними должно превышать длину волны падающего света.
В обычных условиях витающие мелкие частицы в воздухе не видны, но при прохождении солнечного луча в затемненной комнате он становится видимым. Фактически глаз человека воспринимает интенсивность света, рассеянного высокодисперсными частицами.
В соответствии с уравнением (8.2) интенсивность рассеянного света при прочих равных условиях зависит от размеров частиц и их численной концентрации:
Jp = к1νчV2J0(ρ/ρ) = к1νм(4pr3/3ρ)J0. (8.3)
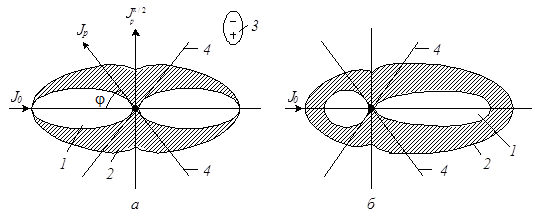
Рис. 8.1. Рассеяние света малой (а) и крупной (б) частицей:
1 и 2 — неполяризованная и поляризованная части света соответственно; 3 — полярная молекула (диполь). 4 — направление максимальной интенсивности рассеяния поляризованной части света.
В формуле (8.3) коэффициент пропорциональности к1 означает, что другие члены уравнения Рэлея остаются неизменными. Поясним преобразование уравнения (8.2) в уравнение (8.3). Если числитель и знаменатель уравнения (8.2) умножить на ρ (плотность материала частиц дисперсной фазы), то произведение νчVp соответствует массе дисперсной фазы в единице объема, т.е. массовой концентрации νм. Это значит, что интенсивность рассеянного света пропорциональна при постоянной массовой концентрации размеру частиц дисперсной фазы в третьей степени.
Как следует из уравнения (8.2), интенсивность рассеянного света обратно пропорциональна длине волны падающего света в четвертой степени:
Jp = к2J0/λ4. (8.4)
Cвет коротких волн рассеивается сильнее. Красный свет имеет наибольшую в видимой части спектра длину волны (620—760 нм) и рассеивается в меньшей степени. Поэтому запрещающие сигналы светофоров и других регулирующих устройств имеют красный свет, а бамперы электричек и электровозов, жилеты железнодорожных рабочих — красно-коричневую или оранжевую окраску.
Длина волны фиолетового света 380—450 нм; он рассеивается более интенсивно по сравнению с красным. Интенсивность рассеяния фиолетового света примерно в 16 раз выше интенсивности рассеяния красным, длина волны которого лишь в два раза превышает длину волны фиолетового света. Не случайно во время Великой Отечественной войны применялись синие лампочки для освещения затемненных объектов: значительное рассеяние света синими лампочками исключало возможность увидеть источник света даже на незначительном расстоянии.
Рассеянный солнечный свет, который образуется под действием аэрозольных частиц, ассоциатов молекул и других включений, нарушающих однородность среды, помимо фиолетового содержит и другие лучи спектра. Эти лучи ассимилируются и со стороны Земли придают небу голубую окраску. Со стороны Космоса, т.е. в направлении солнечных лучей, рассеяния не происходит: космонавты видят черное небо и голубой ореол Земли.
Заметим, что кроме особенности рассеянного света восприятие красного и фиолетового света зависит от специфики спектральной чувствительности глаза человека.
Интенсивность рассеянного света, согласно уравнению (8.2), зависит от показателей преломления вещества дисперсной фазы n1 и дисперсионной среды n2.
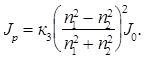 (8.5)
(8.5)
Если показатель преломления вещества, из которого формируется дисперсная фаза, равен показателю преломления дисперсионной среды (n1 = n2), то рассеяния не происходит. Так, в однородных средах светорассеяние не наблюдается.
Показатель преломления воздуха n1 равен 1,000, воды n2 — 1,333, поэтому капли воды в воздушной среде в соответствии с уравнением (8.5) способны к рассеянию света.
Свет рассеивается во всех направлениях, т.е. является векторной величиною. Однако, его интенсивность в различных направленных неодинакова. Интенсивность рассеянного света в пространстве может быть представлена в виде векторной диаграммы. Распределение интенсивности paссеянного света в одной плоскости можно представить при помощи рис. 8.1.
Рассеянный свет обычно поляризован. Поляризация заключается в поперечной анизотропии (неоднородности) световых лучей. Как следует из рис. 8.1, а рассеянный свет не поляризован в направлении падающего луча и полностью поляризован в плоскости, которая перпендикулярна падающему световому лучу. В этом направлении образуется седловина. Максимальная интенсивность поляризованного света достигается на краях седловины, прямые 4 рис. 8.1, когда угол между падающим и рассеянным светом (j) равен приближенно 55о. Если падающий свет не поляризован, то интенсивность рассеянного света, т.е. отношение между Jр/J0 пропорционально величине 1 + Cos2φ. При φ, равным нулю, рассеяние максимально, при φ = 90o оно отсутствует (Jрπ/2; рис. 8.1, а).
При значительной концентрации частиц, когда расстояние между частицами меньше длины волны падающего света, уравнение (8.2) теряет смысл.
Рассеяние света дисперсной системой, состоящей из множества частиц, существенно отличается от рассеяния света одиночными частицами. Это отличие обусловлено интерференцией волн, рассеянных отдельными частицами, и падающих волн; многократным рассеянием, которое наблюдается, когда свет, рассеянный одними частицами, повторно рассеивается другими; перемещением частиц.
В заключении отметим отличие между опалесценцией и флуоресценцией. Оба эти явления связаны со свечением растворов. При опалесценции свечение вызвано рассеянием света коллоидными растворами. Термин «опалесценция» широко используют как синоним видимого невооруженным глазом рассеяния света коллоидными растворами, которые по внешним признакам трудно отличить от истинных растворов.
Флуоресценция же характерна только для истинных растворов и связана с поглощением света одной длины волны и излучением света другой длины волны; в результате в отраженном свете раствор приобретает окраску. Кроме того, при опалесценции в отличие от флуоресценции рассеянный свет частично поляризован.
 2014-02-02
2014-02-02 4896
4896
