В липидный каркас клеточных мембран встроены белковые компоненты (протеины). На каждую клетку в среднем приходится около 10 пг мембранных белков (МБ). Различают периферические и собственные (интегральные) белки биологических мембран. Белки первого типа располагаются на поверхности липидного бислоя. Здесь связь между липидами и белками осуществляется за счет электростатического взаимодействия между противоположно заряженными полярными группами этих веществ. Интегральные белки взаимодействуют своими гидрофобными областями с углеводородными цепочками липидов только за счет Ван-дер-ваальсовых сил. У интегральных белков все гидрофильные области спрятаны внутрь молекулы, а наружу направлены неполярные группы. В этой связи, собственные белки полностью или частично погружаются в биологическую мембрану, при этом крупные белковые молекулы могут пронизывать БМ насквозь.
Наиболее характерным типом вторичных структур интегральных белков является спираль. Причем, на участках, окруженных липидами, преобладает 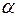 -спираль, у которой все аминокислотные остатки - гидрофобные. Реже встречается
-спираль, у которой все аминокислотные остатки - гидрофобные. Реже встречается 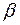 - спираль, представляющая собой полое микро трубчатое образование, наружные стенки которого сосредоточены гидрофобные аминокислотные остатки, а внутрь полости ориентированы гидрофильные группы. Предполагается, что белки, имеющие структуру
- спираль, представляющая собой полое микро трубчатое образование, наружные стенки которого сосредоточены гидрофобные аминокислотные остатки, а внутрь полости ориентированы гидрофильные группы. Предполагается, что белки, имеющие структуру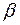 - спирали, образуют ионные каналы в клеточных мембранах.
- спирали, образуют ионные каналы в клеточных мембранах.
Функции мембранных белков весьма разнообразны. Среди них можно выделить следующие основные:
1. Обеспечение транспортных свойств БМ (образование мембранных каналов, работа в качестве переносчиков определенных веществ, участие в системах активного транспорта);
2. Белки несут функцию структурного компонента БМ, тем самым, они усиливают прочность липидного каркаса.
3. Большим разнообразием различаются мембранные протеины, катализирующие химические реакции. Причем, белки-ферменты, встроенные в БМ, действуют активнее, чем при их пребывании в растворе. Установлено, что основная часть всех биохимических реакций, протекает на клеточных мембранах.
4. Важным функциональным типом МБ являются белки-рецепторы. Они столь разнообразны, сколь разнообразны стимулы, которые воспринимаются рецепторными белками. Так, например, восприятие света, обеспечивается пигментами, в состав которых, наряду с белками, входят хромофорные группы с определенным спектром поглощения. Таким пигментом является родопсин, который обеспечивает реакции на свет палочек или колбочек.
5. Белки, присутствующие в мембранах любой клетки, осуществляют ее взаимодействие с окружающей средой, а также обмен информацией между органеллами внутри клетки.
6. Белки, образующие антитела, способны связывать специфический антиген (белок бактерии, вируса, токсина и т. д.) и вызывать иммунный ответ клетки, в плазмолемме которой белки сосредоточены.
В различных мембранах белки распределены среди липидов по-разному. В плазмолемме их распределение довольно равномерное. Для специализированных внутриклеточных мембран, характерно неоднородное распределение белков в БМ.
Различия между клеточными мембранами разных типов, между участками БМ и даже, между сторонами одной и той же мембраны, привели к выводу о гетерогенности БМ. Под гетерогенностью понимают разнородность их структур и функциональных свойств. Особенности молекулярных структур клеточных мембран и предопределяют их физические и физико-химические свойства.
ФИЗИЧЕСКИЕ И ФИЗИКО-ХИМИЧЕСКИЕ
СВОЙСТВА БМ
В живых клетках БМ представляют собой жидкокристаллические структуры. Структуры жидкого кристалла образуют как липидные, так и белковые молекулы. Молекулярной организации клеточных мембран, как жидкого кристалла, характерно состояние с высокой степенью упорядоченности и текучести (лабильности).
БМ присущи такие свойства:
1. Значительная прочность на разрыв.
2. Упругость (эластичность).
4. Вязкость.
5. Электрострикция.
6. Флексоэлектрострикция.
Два последних свойства обусловлены наличием повторного заряда на БМ.
ПОВЕРХНОСТНЫЙ ЗАРЯД НА КЛЕТОЧНОЙ МЕМБРАНЕ (КМ )
Он создается полярными головками фосфолипидов, гликопродеидами (главным образом, карбоксильными группами сиаловой кислоты и аминокислотными остатками), а также, гликолипидами. За счет этих веществ, поверхность БМ заряжена отрицательно. Поверхностный заряд плазмолеммы играет важную роль в межклеточных взаимодействиях. Он способствует стабильности мембранных структур, а также, связыванию ионов, находящихся в межклеточной среде. От поверхностного заряда плазмолеммы зависит ионный состав предмембранных слоев, что оказывает влияние на многие внутриклеточные обменные процессы.
Существование заряженных групп на БМ приводит к образованию двойного диффузионного электронного слоя, в котором фиксированный отрицательный заряд клеточной поверхности уравновешен положительным зарядом, который создается межклеточной средой за счет положительных ионов. Подвижность ионов не одинакова в различных условиях. Разность потенциалов между неподвижными и подвижными частями двойного электронного слоя называют электрокинетическим потенциалом или дзета потенциалом. Толщина двойного электрического слоя и дзета потенциала зависит от природы электролита и концентрации ионов (в межклеточной среде). Так, при уменьшении концентрации 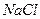 в межклеточной среде в 200 раз, толщина двойного электрического слоя возрастает в 5 раз. При высокой концентрации электролита, дзета потенциал стремиться к нулю. Когда в межклеточной среде присутствуют двухвалентные катионы, избыток положительного заряда может стать настолько велик, что дзета потенциал изменит свой знак. Снижение дзета потенциала и, тем более, изменение его знака на противоположный, вызывает слипание плазматических мембран соседних клеток. Это проявляется при избытке ионов в межклеточной среде, а также, при перестройках клеточных мембран, приводящих к сдвигам дзета потенциала. Подобный эффект имеет свои особенности у клеток крови, в которых дзета потенциал форменных элементов (эритроцитов) может падать за счет нарушения не только солевого, но и белкового состава кровяной плазмы. Это явление лежит в основе изменения скорости осаждения эритроцитов (СОЭ), измерение которых широко используется в диагностических целях.
в межклеточной среде в 200 раз, толщина двойного электрического слоя возрастает в 5 раз. При высокой концентрации электролита, дзета потенциал стремиться к нулю. Когда в межклеточной среде присутствуют двухвалентные катионы, избыток положительного заряда может стать настолько велик, что дзета потенциал изменит свой знак. Снижение дзета потенциала и, тем более, изменение его знака на противоположный, вызывает слипание плазматических мембран соседних клеток. Это проявляется при избытке ионов в межклеточной среде, а также, при перестройках клеточных мембран, приводящих к сдвигам дзета потенциала. Подобный эффект имеет свои особенности у клеток крови, в которых дзета потенциал форменных элементов (эритроцитов) может падать за счет нарушения не только солевого, но и белкового состава кровяной плазмы. Это явление лежит в основе изменения скорости осаждения эритроцитов (СОЭ), измерение которых широко используется в диагностических целях.
Дзета потенциал, измеряемый у различных клеток, изменяется в пределах от -10 до -30 мВ. Его величина спадает по exp закону, с увеличением расстояния от поверхности БМ. Дзета потенциал оказывает существенное влияние на размеры межклеточных пространств, и противодействует силам их притяжения. Наименьшее расстояние между клетками составляет порядка 10-20 нм. При таком расстоянии существует энергетическая "яма" во взаимодействии кулоновских и Ван-дер-Ваальсовских сил. В большинстве тканей расстояние между клетками составляет от 0,1 до 1 микрона.
Липидная часть БМ обладает свойствами диэлектрика. Относительная диэлектрическая проницаемость (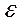 ) гидрофобной зоны составляет порядка 2-2,2, тогда, как в гидрофильной части
) гидрофобной зоны составляет порядка 2-2,2, тогда, как в гидрофильной части 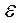 гораздо выше, и составляет около 10-20. Емкость полярных головок липидов достигает примерно 30
гораздо выше, и составляет около 10-20. Емкость полярных головок липидов достигает примерно 30 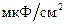 , а жирно-кислотные хвосты имеют емкость около 0,5-0,9
, а жирно-кислотные хвосты имеют емкость около 0,5-0,9 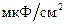 . Общая емкость БМ составляет примерно 1
. Общая емкость БМ составляет примерно 1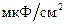 .
.
Благодаря существованию в БМ заряженных групп, ей присуща ярко выраженная электрострикция, то есть, по мере повышения трансмембранной разности потенциалов, БМ сжимается, что приводит к утоньшению гидрофобной зоны мембраны и, соответственно, к увеличению мембранной емкости. Возрастание дзета потенциала сопровождается увеличением клеточной поверхности.
Механические свойства КМ весьма своеобразны. Величина модуля Юнга в поперечном направлении достигает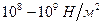 . Вместе с тем, устойчивость к деформации сдвига примерно на 4 порядка меньше. Сила, достаточная для разрушения БМ на участке в 1 мкм, оценивается величиной примерно
. Вместе с тем, устойчивость к деформации сдвига примерно на 4 порядка меньше. Сила, достаточная для разрушения БМ на участке в 1 мкм, оценивается величиной примерно 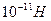 . Значительный вклад в повышение упругости и прочности мембраны вносят не только интегральные, но, также, довольно густая цепь периферических белков.
. Значительный вклад в повышение упругости и прочности мембраны вносят не только интегральные, но, также, довольно густая цепь периферических белков.
ВЯЗКОСТЬ БМ
В живой клетке БМ находятся в жидкокристаллическом состоянии. Жидкокристаллическому состоянию присущи текучесть и определенная вязкость. Величина вязкости была измерена с помощью ЭПР (эл. парамагнитного резонанса) и ДСК (диффузионно - сканирующей микрокаллометрией). Результаты измерения вязкости разными методами совпали. При этом вязкость БМ изменилась от 0,03 до 0,1 Па*с (30-100 ) или 30-100 сП (сантипуаз). Это примерно в 30-100 раз больше, чем вязкость воды и примерно такая же, как вязкость оливкового или подсолнечного масла. При изменении температуры молекулярного состава и других параметров биологических мембран, изменяется ее вязкость, вследствие чего происходят фазовые изменения в структуре мембраны, то есть, осуществляется переход жидкий кристалл - твердый кристалл.
) или 30-100 сП (сантипуаз). Это примерно в 30-100 раз больше, чем вязкость воды и примерно такая же, как вязкость оливкового или подсолнечного масла. При изменении температуры молекулярного состава и других параметров биологических мембран, изменяется ее вязкость, вследствие чего происходят фазовые изменения в структуре мембраны, то есть, осуществляется переход жидкий кристалл - твердый кристалл.
Одним из важных достоинств температурного гомеостаза является поддержание БМ в жидкокристаллическом состоянии, что обеспечивает стабильность транспорта веществ через нее. Жизнеспособность организма страдает как при понижении, так и при повышении мембранной проницаемости, которая, в свою очередь, зависит от вязкости БМ.
 2014-02-03
2014-02-03 2755
2755
