Живые системы на 99 % состоят из атомов 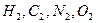 . Большую роль биохимических процессов играют атомы
. Большую роль биохимических процессов играют атомы 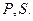 Для атомов
Для атомов 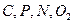 и
и 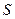 характерно наличие не поделенной пары электронов и способность образовывать кратные связи. Состояние электронов в атоме описывается волновыми функциями АО. Эти атомные орбиты (АО) характеризуют движение электронов вокруг ядра. В зависимости от орбитального квантового числа, АО могут быть
характерно наличие не поделенной пары электронов и способность образовывать кратные связи. Состояние электронов в атоме описывается волновыми функциями АО. Эти атомные орбиты (АО) характеризуют движение электронов вокруг ядра. В зависимости от орбитального квантового числа, АО могут быть  . АО, которые используются для образования связей, называются валентными орбитами.
. АО, которые используются для образования связей, называются валентными орбитами.
Состав электронов в молекуле также может быть описан с помощью волновой функции, которые именуются молекулярными орбитами МО. МО образуются путем перекрытия атомных орбиталей, в зависимости от того, какие атомные орбитали образуют данную МО различают 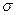 и
и 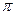 орбитали. Необходимо отметить, что именно электроны находятся на
орбитали. Необходимо отметить, что именно электроны находятся на 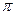 орбитали обусловливая образование кратных связей. Для атомов
орбитали обусловливая образование кратных связей. Для атомов 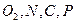 характерно наличие не поделенной пары электронов и образование кратных связей.
характерно наличие не поделенной пары электронов и образование кратных связей.
Все многоатомные молекулы могут быть разделены на две группы:
1) несопряженные системы;
Несопряженные системы содержат только одинарные связи или же, в них имеются изолированные кратные связи, отделенные друг от друга или от атомов с неподеленной парой электронов, по крайней мере, одним атомом с насыщенной валентностью. Такие молекулы можно рассматривать, как состоящие из примыкающих друг к другу и почти независимых друг от друга, связей. Каждая связь описывает локализованную двуцентровую МО, аналогично молекулярным орбитам в двухатомной молекуле. Свойства образующих молекулярных связей постоянны и для одной и той же связи, входящей в разные молекулы, свойства меняются незначительно.
Сопряженные системы представляют собой молекулы, содержащие несколько кратных связей, в которых участвуют соседние атомы или же молекулы, в состав которых входят атомы с неподеленными электронными парами, расположенными рядом с кратной связью. Для таких систем характерно нелокализованные многоцентровые молекулярные орбитали, которые относятся к молекуле в целом или к большей ее части.
Если молекула с сопряженными связями, содержит атомы, обладающие неподеленными электронными парами, то электронами этих пар могут включаться в общую систему 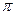 - электронов. Существование делокализованных
- электронов. Существование делокализованных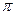 -электронов является важнейшим свойством молекул с сопряженными связями. Основные химические, физико-химические и биохимические свойства таких систем определяются
-электронов является важнейшим свойством молекул с сопряженными связями. Основные химические, физико-химические и биохимические свойства таких систем определяются 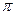 - электронами, так как они более подвижны, по сравнению с
- электронами, так как они более подвижны, по сравнению с 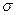 -электронами и с большей легкостью вступают в химические реакции.
-электронами и с большей легкостью вступают в химические реакции.
 2014-02-03
2014-02-03 1003
1003








