Относятся к классу железосодержащих белков, называемых гемопротеинами. Гем представляет собой тетрапиррольный хелат железа. В этой структуре четыре пиррольных ядра, имеющих заместителей на периферии, объединены в порфириновое кольцо (рис. 15).
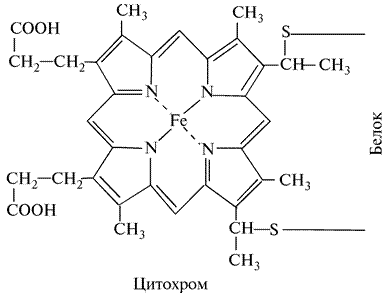
Рис. 15. Схема строения молекулы цитохрома
В центре порфиринового кольца цитохромов находится ион Fe2+. Комплексы с Fe2+ называют гемами. Эти соединения называют также феррогемами, а с Fe3+ — соединения, образующиеся путем окисления Fe2+ ферригемами.
Гемопротеин — это белок, содержащий в качестве простетической группы гем. Цитохромы — это гемопротеины, характерной особенностью которых является перенос электронов, сопряженный с обратным изменением степени окисления простетической группы. Это изменение окислительно-восстановительного состояния включает обратимое равновесие между Fe2+ и Fe3+ состояниями гема:
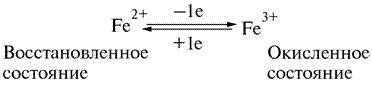
Цитохромы относятся к одноэлектронным окислительно-восстановительным соединениям. Они не могут принимать или отдавать водород, поэтому их называют переносчиками электронов. Цитохромы присутствуют во многих тканях животного, растительного и бактериального происхождения. Цитохромы подразделяются на цитохромы a, b, c и d в соответствии с положением их спектральных полос поглощения в восстановленном состоянии.
Цитохромы а и а 3 существуют и функционируют в виде единого прочного комплекса. Особенностью комплекса цитохрома а · а 3 является наличие в нем меди, связанной с компонентом а 3, необходимой для его функционирования. Перенос электронов комплексом а · а 3 включает следующие реакции:
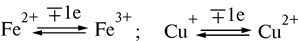
Цитохром а · а 3 непосредственно реагирует с молекулярным кислородом воздуха, т. е. электроны передаются на кислород, переводя его в ионы (О-2). Далее ионы кислорода вступают во взаимодействие с протонами, образуя воду. Комплекс а · а 3 часто называют цитохромоксидазой.
 2014-02-09
2014-02-09 9743
9743








