Примечание.
1.Постоянная или число Авогадро – это число молекул в грамм-молекуле или атомов в грамм-атоме, одинаковое для всех веществ и равное  моль- 1.
моль- 1.
2. Грамм-атомом называется такое количество химически простого вещества, масса которого выраженная в граммах, равна его атомному весу.
Молярная теплоемкость твердого тела находится дифференцированием внутренней энергии (1), то есть,
 Дж/(моль·К). (2)
Дж/(моль·К). (2)
Как следует из результата (2), молярная (атомная) теплоемкость химически простых тел в кристаллическом состоянии одинакова (равна 3·R) и не зависит от температуры.
Этот закон был эмпирически получен французскими учеными П. Дюлонгом (1785—1838) и Л. Пти (1791—1820). Он носит название закона Дюлонга и Пти.
Если твердое тело является химическим соединением (например, NaCl), то число частиц в моле не равно постоянной Авогадро, а равно n·NA, где n — число атомов в молекуле (для NaCl число частиц в моле равно 2·NA, так, в одном моле NaCl содержится NA атомов Na и NA атомов Cl).
Таким образом, молярная теплоемкость твердых химических соединений
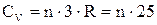 Дж/(моль·К). (3)
Дж/(моль·К). (3)
Как следует из результата (3), молярная теплоемкость твердых химических соединенийравна сумме атомных теплоемкостей элементов, составляющих это соединение.
Как показывают опытные данные, для многих веществ закон Дюлонга и Пти выполняется с довольно хорошим приближением, хотя отмечены отклонения для некоторых веществ и определённых условий экспериментов.
Расхождение опытных и теоретических значений теплоемкостей, вычисленных на основе классической теории, объяснили, исходя из квантовой теории теплоемкостей, А. Эйнштейн и П. Дебай.
Как в жидкостях, так и в твердых телах всегда имеется некоторое число молекул, энергия которых достаточна для преодоления притяжения к другим молекулам и которые способны оторваться от поверхности жидкости или твердого тела и перейти в окружающее их пространство.
Определение 1.
 2014-02-18
2014-02-18 1104
1104







