Введение. Витамины это группа органических веществ, обладающих разнообразным строением и физико- химическими свойствами, абсолютно необходимых для нормальной жизнедеятельности любого организма и выполняющих в нем непосредственно или в составе более сложных соединений каталитические и регуляторные функции.
Антиокислительные свойства витаминов
Учебные и воспитательные цели: Составить современное представление о структуре, метаболизме и молекулярных механизмах действия жирорастворимых витаминов
ЛИТЕРАТУРА
1. Основы биохимии:А.Уайт, Ф.Хендлер,Э.Смит, Р.Хилл, И.Леман.-М. книга,
1981,т.3,.с.1703-1757.
2. Питание в профилактике и лечении рака.- Т.С. Морозкина., К.К.Далидович.
Минск., 1998г
3..Биохимия человека:, Р.Марри, Д.Греннер, П.Мейес, В.Родуэлл.- М.книга,2004.
- т.1, 2.
4.Наглядная биохимия: Кольман., Рем К.-Г-М.книга 2004г
5. Спиричев
1.Мультимедийная презентация
РАСЧЕТ УЧЕБНОГО ВРЕМЕНИ
| №п/п | Перечень учебных вопросов | Количество выделяемого времени, мин. |
| 1. | Жирорастворимые витамины | 70 мин |
| 2. | Антиокислительные свойства витаминов | 20 мин |
Всего: 90 минут
Витамин А (ретинол), антиксерофтальмический, витамин роста.
Химическое строение и свойства. Витамин А был открыт в 1940 г. и назван фактором роста, так как с его удалением при экстракции корма грызунов жирорастворителями наблюдалась остановка роста и гибель мышей-отъёмышей.
Жирорастворимый витамин А представляет собой циклический непредельный одноатомный спирт, состоящий из β–иононового кольца и боковой цепи из 2-х остатков изопрена и первичной спиртовой группы.
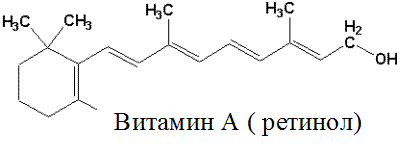
Спиртовая форма витамина А, ретинол, в организме окисляется до ретиналя (альдегид витамина А) и ретиноевой кислоты (вместо спиртовой группы образуется карбоксильная). Депонируется витамин А в печени в форме эфиров пальмитиновой и уксусной кислот (ретинилпальмитата и ретинилацетата), а также в виде ретинилфосфата.
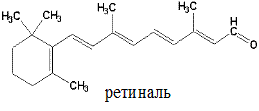
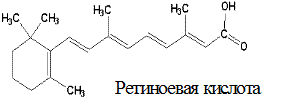
Метаболизм. Витамин А может образовываться в слизистой кишечника и печени из провитаминов – α-, β- и γ-каротинов под воздействием каротиноксигеназы. Наибольшей активностью обладает β-каротин (из него образуется 2 молекулы ретинола, из других – по одной).
Всасывание витамина и его провитаминов происходит в составе мицелл, затем в энтероцитах они включаются в состав хиломикронов. В крови витамин А связывается с ретинолсвязывающим белком (один из белков фракции α1-глобулинов). Ретинолсвязывающий белок обеспечивает растворимость ретиола, защиту его от окисления, транспорт и доставку в различные ткани. В сетчатке глаза ретинол превращается в ретиналь, в печени – в ретиналь и затем в ретиноевую кислоту, которая выводится с желчью в виде глюкуронидов.
Биохимические функции. Роль витамина А заключается в следующем:
1. Ретинол является структурным компонентом клеточных мембран.
2. Регулирует рост и дифференцировку клеток эмбриона и молодого организма, а также деление и дифференцировку быстро пролиферирующих тканей, в первую очередь, эпителиальных, хряща и костной ткани. Он контролирует синтез белков цитоскелета, реакции распада и синтеза гликопротеинов. Синтез последних осуществляется в аппарате Гольджи. Недостаток витамина А приводит к нарушению синтеза гликопротеинов (точнее, реакциях гликозилирования, т.е. присоединения углеводного компонента к белку), что проявляется потерей защитных свойств слизистых оболочек.
3. Участвует в фотохимическом акте зрения.
4. Является важнейшим компонентом антиоксидантной защиты организма.
5. Витамин А и ретиноиды стимулируют реакции клеточного иммунитета, в частности, увеличивают активность Т-киллеров.
6. Витамин А является антиканцерогеном, так как при его недостатке в организме увеличивается заболеваемость раком лёгкого и раком других локализаций.
Рассмотрим подробнее некоторые аспекты действия витамина А.
Участие витамина А в процессе зрения.
В сетчатке глаза имеются специализированные фоторецепторные клетки двух типов – палочки и колбочки. Наибольшей светочувствительностью обладают палочки, колбочки обеспечивают цветовое зрение. Наружные сегменты палочек содержат уплощенные замкнутые мембранные пузырьки – диски, уложенные в стопку. Диски богаты белком опсином. Опсин способен связываться с 11-цис-ретиналем, образуя пигмент пурпурно-красного цвета родопсин. Механизм образования зрительного сигнала достаточно хорошо изучен (см. рис.):
1. Квант света стимулирует мембранные рецепторы наружного сегмента палочек сетчатки (родопсин).
2. Абсорбция света родопсином изомеризует цис-связь в 11-цис-ретинале в транс-связь. Такая транс-структура называется батородопсином (ативированным родопсином). Транс-ретиналь имеет бледно-жёлтого оттенок, следовательно, при освещении родопсин обесцвечивается.
3. При освобождении протона из батородопсина образуется метародопсин II, гидролитический распад которого даёт опсин и all-транс-ретиналь. Фотохимическая цепь в батородопсине (т.е. транс-ретиналь) служит для активации G-белка, называемого трансдуцином. Трансдуцин активируется ГТФ-ом.
4. Комплекс трансдуцин-ГДФ активирует специфическую фосфодиэстеразу, последнярасщепляет цГМФ.
5. 
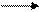 ГМФ стимулирует каскад событий, генерализующих зрительный сигнал в мозге: перекрытие Na+-K+-каналов деполяризация мембраны возникновение электрического импульса преобразование импульса в зрительное восприятие в мозге.
ГМФ стимулирует каскад событий, генерализующих зрительный сигнал в мозге: перекрытие Na+-K+-каналов деполяризация мембраны возникновение электрического импульса преобразование импульса в зрительное восприятие в мозге.
Образование цис-ретиналя из транс-формы, катализируемое ретинальизомеразой, является медленным процессом, протекающим на свету. Цис-ретиналь связывается с опсином и образуется родопсин. В темноте синтез родопсина максимален. Однако нужно отметить,

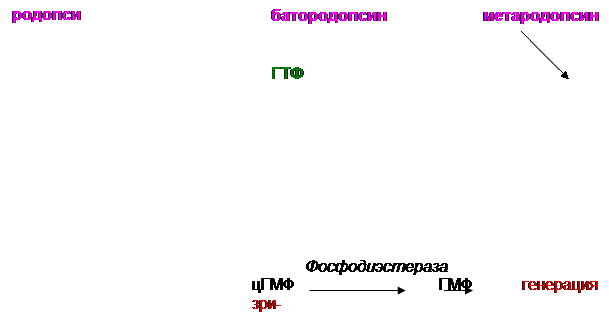
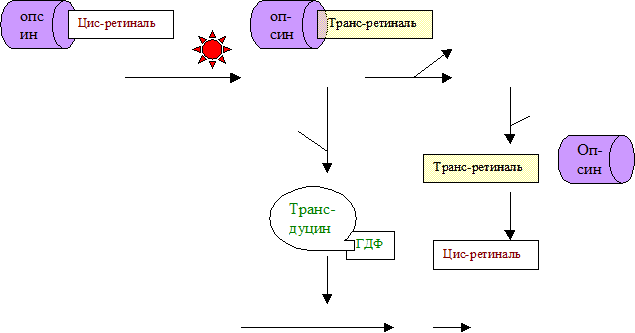
что синтез цис-ретиналя лишь частично протекает в сетчатке глаза, основное место его образования – печень. Кроме того, в сетчатке под действием специфической дегидрогеназы транс-ретиналь (альгид) превращается в транс-ретинол (спирт), который поступает в кровь, где соединяется с ретинолсвязывающим белком плазмы. Таким способом он доставляется в печень. В печени ретинолизомераза превращает транс-ретинол в цис-ретинол, последний с помощью NAD+-зависимой дегидрогеназы окисляется в цис-ретиналь, который также поступает в кровь. Этот комплекс улавливается пигментным эпителием сетчатки, и цис-ретиналь уже без участия ферментов связывается с опсином. Отсутствие регенерации родопсина приводит к слепоте в сумерках.
Участие витамина А в антиоксидантной защите организма. Благодаря наличию сопряжённых двойных связей в молекуле ретинол способен взаимодействавать со свободными радикалами различных типов, в том числе и со свободными радикалами кислорода. Эта важнейшая особенность витамина позволяют считать его эффективным антиоксидантом.
Антиоксидантное действие ретинола проявляется также в том, что он значительно усиливает антиоксидантное действие витамина Е. Вместе с токоферолом и витамином С он активирует включение Se в состав глутатионпероксидазы (фермента, обезвреживающего перекиси липидов). Витамин А способствует поддержанию SH-групп в восстановленном состоянии (SH-группам многообразного класса соединений также присуща антиоксидантная функция). В частности, препятствуя окислению SH-содержаших белков и образованию в них поперечных S-S- сшивок в составе кератина, ретинол тем самым препятствует кератинизации эпителия (усиление кератинизации кожи приводит к усиленному слущиванию эпителия, развитию дерматита и раннему старению кожи).
Однако витамин А может проявлять себя и как прооксидант, так как он легко окисляется кислородом с образованием высокотоксичных перекисных продуктов. Полагают, что симптомы гипервитаминоза А как раз и обусловлены его прооксидантным действием на биомембраны, особенно усиливается процесс ПОЛ в лизосомных мембранах, к которым витамин А проявляет выраженную тропность. Витамин Е, предохраняя ненасыщенные двойные связи ретинола от окисления и образования вследствие этого свободнорадикальных продуктов самого ретинола, тем самым препятствует проявлению его прооксидантных свойств. Необходимо отметить и синергичную с токоферолом роль аскорбиновой кислоты в этих процессах.
В настоящее время большое внимание в мировой литературе уделяется производным витамина А – ретиноидам. Полагают, что их механизм действия сходен со стероидными гормонами. Ретиноды действуют на специфические рецепторные белки в клеточных ядрах.Далее такой лиганд-рецепторный комплекс связывается со специфическими участками ДНК, которые контролируют транскрипцию специальных генов. Идентификация этих генов служит предметом активного научного поиска.
Гиповитаминоз. Наиболее ранним симптомам недостаточности витамина А является «куриная слепота» - резкое снижение темновой адаптации. Характерным является поражение эпителиальных тканей: кожи (фолликулярный гиперкератоз), слизистых оболочек кишечника (вплоть до развития язв), бронхов (частые бронхиты), мочеполовой системы (легкое инфицирование).
Дерматиты сопровождаются патологической пролиферацией, кератинизацией и слущиванием эпителия. Десквамация эпителия слёзных каналов может приводить к их закупорке и уменьшению смачивания роговицы глаза слёзной жидкостью – она высыхает (ксерофтальмия) и размягчается (кератомаляция) с образованием язв и «бельма». Поражение роговицы может развиваться очень быстро, так как нарушение защитных свойств эпителия приводит к присоединению вторичной инфекции.
Витамин А называется также витамином роста. Особенно демонстративно отставание в росте и гибель животного при недостатке ретинола прослеживаются у хищников, которые не способны синтезировать этот витамин из каротинов.
В качестве эффективного антиоксиданта витамин А защищает организм от «пероксидного стресса» – важнейшего патогенетического звена многих тяжёлых заболеваний.
Гиперкаротинемия. Причиной заболевания является отсутствие кишечной β-каротин-оксигеназы,.катализирующей реакцию образования ретинола из каротиов. Основными симптомами являются «куриная слепота» и помутнение роговицы. Резко снижено содержание ретинола в крови.
Фолликулярный кератоз Дарье. При этом наследственном заболевании наряду с изменениями кожи и слизистых оболочек отмечаются отставание умственного развития и психозы. Типичны продольная исчерченность и зазубренность ногтей. Эффективно длительное назначение повышенных доз витамина А.
Гипервитаминоз А. Для гипервитаминоза А характерны следующие симптомы: воспаление роговицы глаза, гиперкератоз, потеря аппетита, тошнота (при остром отравлении – рвота), понос, головные боли, боли в суставах, увеличение печени. Развивается общее истощение организма.
Хроническое отравление витамином наблюдается при регулярном употреблении высоких доз витамина, больших количеств рыбьего жира. Случаи острого отравления со смертельным исходом наблюдали при употреблении в пищу печени акулы, белого медведя, морских животных (печень и жировая ткань – основные депо витамина).
Оценка обеспеченности организма ретинолом. Степень обеспеченности определяется по содержанию витамина в крови. Используются также показатели темновой адаптации, электроренограмма. Косвенный показатель – увеличение активности лизосомных ферментов.
Суточная потребность. Пищевые источники. Ретинол присутствует только в животной пище, особенно много его в печени и жире морских рыб и млекопитающих. Источником витамина А для человека являются также каротины. Однако следует заметить, что β-каротины полностью заменить витамин А не могут, так как лишь ограниченное их количество способно превратиться в ретинол. И этого количества недостаточно для проявления характерных антиоксидантных свойств витамина А.
Суточная потребность в витамине А составляет 1,5-2 мг.
Каротины (провитамины А ).
Химическое строение и свойства. Каротины являются изопреноидами и образуются в растениях при фотосинтезе. Известны 3 типа каротинов: α-, β- и γ-каротины.
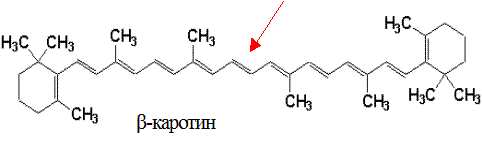
Впервые каротины были выделены из моркови, отсюда и их название (carota – морковь). α- и γ-каротины содержат по одному β-иононовому кольцу и при их окислительном распаде образуется 1 молекула витамина А, в молекуле β-каротина – два β-иононовых кольца и он обладает большей биологической активностью, поскольку из него образуется 2 молекулы ретинола:

 β-каротин + 2 НАД (Ф)H∙H+ 2 all- транс -ретинол +2 НАД+
β-каротин + 2 НАД (Ф)H∙H+ 2 all- транс -ретинол +2 НАД+
Реакция катализируется двумя ферментами: каротиндиоксигеназой, расщепляющей молекулу β-каротина в центральной его части, и редуктазой с участием коферментов НАДH∙H+ либо НАДФH∙H+ . Одновременный приём с пищей антиоксидантов, препятствующих окислению каротина по периферическим двойным связям, а также витамина В12, повышающего активность каротиндиоксигеназы, увеличивается количество молекул каротина, расщепляющегося по центру, и эффективность синтеза витамина А вследствие этого возрастает в 1,5-2 раза. Усвоению каротина способствуют также флавоноиды.
Главным местом превращения каротина в витамин А является стенка кишечника. Поскольку каротины являются жирорастворимыми соединениями, их усвоение происходит вместе с липидами.
Каротины легко окисляются кислородом воздуха; чувствительны к свету. Процесс их окисления идёт аутокаталитически с образованием свободных радикалов. Витамин Е способен предохранять двойные связи в молекуле β-каротина от окисления.
Биохимические функции. Наличие сопряжённых двойных связей в молекуле витамина А и каротинов обуславливает их высокую реакционную способность при взаимодействии со свободными радикалами различных типов. В молекуле β-каротина 11 ненасыщенных двойных связей, константа скорости реакции со свободными раликалами у него в 5 раз больше, чем у ретинола. β-каротин способен быть перехватчиком свободных радикалов благодаря стабилизации в его молекуле неспаренного электрона. Таким образом, каротиноиды выполняют роль антиоксидантов, перехватывая синглетный кислород и другие активные формы кислорода (О2˙, ОН˙, Н2О2). β-каротин является наиболее важным гасителем синглетного кислорода. Поскольку облучение и канцерогенез имеют свободнорадикальную природу, β-каротин по праву считается радиозащитным соединением и антиканцерогенном
Поскольку каротины являются жирорастворимыми соединениями, их усвоение происходит вместе с липидами.
Каротины легко окисляются кислородом воздуха; чувствительны к свету. Процесс их окисления идёт аутокаталитически с образованием свободных радикалов. Витамин Е способен предохранять двойные связи в молекуле β-каротина от окисления.
Биохимические функции. Наличие сопряжённых двойных связей в молекуле витамина А и каротинов обуславливает их высокую реакционную способность при взаимодействии со свободными радикалами различных типов. В молекуле β-каротина 11 ненасыщенных двойных связей, константа скорости реакции со свободными раликалами у него в 5 раз больше, чем у ретинола. β-каротин способен быть перехватчиком свободных радикалов благодаря стабилизации в его молекуле неспаренного электрона. Таким образом, каротиноиды выполняют роль антиоксидантов, перехватывая синглетный кислород и другие активные формы кислорода (О2˙, ОН˙, Н2О2). β-каротин является наиболее важным гасителем синглетного кислорода. Поскольку облучение и канцерогенез имеют свободнорадикальную природу, β-каротин по праву считается радиозащитным соединением и антиканцерогеном. Он обладат также антимутагенными свойствами. Установлена обратная корреляция межу содержанием в диете β-каротинов и частотой заболеваемости раком.
β-каротины синергично взаимодействуют с витамином Е как мембранные антиоксиданты. β-каротины способны депонировать в клетках кислород. Недостаточность каротинов не описана.При избыточном потреблении каротинов у человека возможно пожелтение ладоней, подошв стоп и слизистых, однако даже в таких крайних случаях выраженных симптомов ин-токсикации не отмечалось. У животных более чем 100-кратное превышение дозировки β-каротинов увеличивало интенсивность реакций ПОЛ в тканях (прооксидантный эффект), этого не наблюдалось в присутствии витаминов Е и С (защита молекулы каротина от окислительной деструкции). Суточная потребность. Пищевые источники. Наибольшее количество β-каротинов содержится в моркови, но в различных сортах моркови их концентрация может резко варьировать (от 8 до 25 мг на 100 г сырого веса). Хорошим источником каротинов являются красный перец, зелёный лук, салат, тыква и томаты.Суточная потребность в β-каротинах составляет 5 мг.
Витамин Е (токоферол), витамин размножения.
Химическое строение и свойства. В 20-е годы Г. Эванс сумел излечить бесплодие у содержащихся на синтетической диете крыс, добавляя им в корм листья салата. Активное соединение, способствующее развитию эмбриона, было выделено также из масел зародышей пшеницы и других семян. Оно получило название «токоферол» (от греч. tokos – потомство, phero – несу).
В 1938 г. токоферол, или витамин Е, был синтезирован химическим путём. Однако между природным и синтетическим витамином Е существуют различия, что отражено в их классификации. Натуральные формы токоферола обозначаются как RRR-альфа-токоферолы (R обозначает конфигурацию метильной группы) и имеют единственный стереоизомер; синтетические формы называются all-rac-альфа-токоферолы и являются рацемической смесью из 8 стереоизомеров, из которых 7 не найдено в природе. Основной биологически активной формой является RRR-α-токоферол:
Свободная ОН-группа обуславливает свойства витамина Е как антиоксиданта.
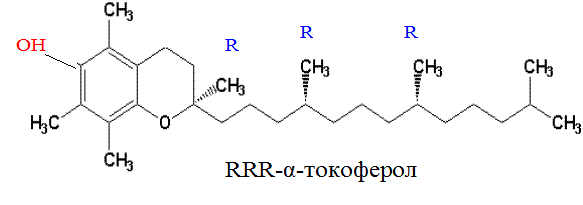
Кроме токоферолов к группе витамина Е относятся α, β, γ и δ-токотриенолы – аналоги соответствующих токоферолов, которые отличаются от последних наличием двойных связей в боковой цепи. Токоферолы – прозрачные, светло-жёлтые, вязкие масла, хорошо растворимые в большинстве органических растворителей. Медленно окисляются на воздухе, разрушаются под действием УФ-лучей.
Метаболизм. Витамин Е поступает в желудочно-кишечный тракт в составе масел, гидролиз которых липазой и эстеразой приводит к высвобождению витамина. Затем он всасывается и в составе хиломикронов поступает в лимфатическую систему и кровяное русло. В печени витамин связывается с токоферол-связывающими белками, причём наибольшим сродством обладает RRR-α-токоферол. Другие токоферолы выделяются из печени с желчными кислотами. Эти белки «экспортируют» витамин в кровь в составе ЛПОНП. В плазме крови происходит обмен токоферолом между ЛПОНП и другими липопротеинами крови. Обмен между фракциями липопротеинов (особенно между ЛПНП и ЛПВП) и эритроцитами обеспечивает равновесие токоферола в крови.
Витамин поступает в экстрапечёночные ткани в составе ЛННП, которые захватываются соответствующими рецепторами. Кроме такого рецепторно -опосредованного механизма имеется и другой, ферментативно -опосредованный, зависящий от активности липопротеинлипазы: фермент высвобождает токоферол из хиломикронов и ЛПОНП, после чего витамин поступает в ткани путём пассивной диффузии (см. рис.). Благодаря пассивной диффузии через клеточную мембрану концентрация RRR-α-токоферола увеличивается во всех тканях организма, особенно в мозге. Структурная организация фосфолипидов клеточных мембранах способна «узнавать» хиральную форму RRR-α-токоферола, благодаря чему витамин задерживается в мембране, где и выполняет свою функцию (синтетические токоферолы в составе мембраны обеспечивают меньшую её защиту от оксидативного стресса).
Не всосавшиеся в кишечнике токоферолы выводятся с калом. Продукты метаболизма витамина – токофериновая кислота и её водорастворимые глюкурониды – выводятся с мочой.
Биохимические функции. Биохимические функции токоферола многообразны:
1. Витамин Е является универсальным протектором клеточных мембран от окислительного повреждения. Он занимает такое положение в мембране, которое препятствует контакту кислорода с ненасыщенными липидами мембран (образование гидрофобных комплексов). Это защищает биомембраны от их перекисной деструкции. Антиоксидантные свойства токоферола обусловлены также способностью подвижного гидроксила хроманового ядра его молекулы непосредственно взаимодействовать со свободными радикалами кислорода (О2˙, НО˙, НО2˙), свободными радикалами ненасыщенных жирных кислот (RO˙, RO2˙) и перекисями жирных кислот. Мембраностабилизирующее действие витамина проявляется и в его свойстве предохранять от окисления SH-группы мембранных белков. Его антиоксидантное действие заключается также в способности защищать от окисления двойные связи в молекулах каротина и витамина А. Витамин Е (совместно с аскорбатом), способствует включению селена в состав активного центра глутатионпероксидазы, тем самым он активизирует ферментативную антиоксидантную защиту (глутатионпероксидаза обезвреживает гидропероксиды липидов).
 | |||
 | |||
/ \ ООi
\ / / / \
 / \ _║¯\ + ОН-ТФ \ / + •O-ТФ
/ \ _║¯\ + ОН-ТФ \ / + •O-ТФ
 \ / / / / \
\ / / / / \
/ \‗/‾ \ \ /
\ / / \‗
/ \ \_
\ / \‗
/ \ \
\ / /
/ \ \
/
перекисный радикал ненасы- ненасыщенная жир- радикал
сыщенной жирной кислоты токоферол ная кислота токоферола
2. Токоферол является не только антиоксидантом, но и антигипоксантом, что объясняется его способностью стабилизировать митохондриальную мембрану и экономить потребление кислорода клетками. Следует отметить, что из всех клеточных органелл митохондрии наиболее чувствительны к повреждению, так как в них содержится больше всего легко окисляющихся ненасыщенных липидов. Вследствие мембраностабилизирующего эффекта витамина Е в митохондриях увеличивается сопряжённость окислительного фосфорилирования, образование АТФ и креатинфосфата. Важно также отметить, что витамин контролирует биосинтез убихинона – компонента дыхательной цепи и главного антиоксиданта митохондрий.
3. Токоферол контролирует синтез нуклеиновых кислот (на уровне транскрипции), а также гема, микросомных цитохромов и других гем-содержащих белков.
4. Витамин Е обладает способностью угнетать активность фосфолипазы А2 лизосом, разрушающей фосфолипиды мембран. Повреждение мембран лизосом приводит к выходу в цитозоль протеолитических ферментов, которые и повреждают клетку.
5. Витамин Е является эффективным иммуномодулятором, способствующим укреплению иммунозащитных сил организма.
Гиповитаминоз. Недостаточность токоферола – весьма распространённое явление, особенно у людей, проживающих на загрязнённых радионуклидами территориях, а также подвергающихся воздействию химических токсикантов. Глубокий гиповитаминоз встречается редко – преимущественно у недоношенных детей (проявляется гемолитической анемией).
При Е-витаминной недостаточности наблюдается частичный гемолиз эритроцитов, в них снижается активность ферментов антиоксидантной защиты. Повышение проницаемости мембран всех клеток и субклеточных структур, накопление в них продуктов ПОЛ – главное проявление гиповитаминоза. Именно этим обстоятельством объясняется разнообразие симптомов недостаточности токоферола. – от мышечной дистрофии и бесплодия вплоть до некроза печени и размягчения участков мозга, особенно мозжечка. Увеличение активности выходящих из повреждённых тканей ферментов в сыворотке крови (креатинфосфокиназы, аланинаминотрансферазы и других) и увеличение содержания в ней продуктов ПОЛ наблюдается уже на ранних стадиях Е-гиповитаминоза.
Дефицит витамина Е в организме сопровождается снижением содержания иммуноглобулинов E. После его введения нормализуется численность Т- и В-лимфоцитов в периферической крови и восстанавливается функциональная активность Т-клеток.
Врождённые нарушения обмена витамина Е:
Акантоцитоз (шиповидные эритроциты) – при этой патологии в плазме крови отсутствуют хиломикроны, ЛПНП и ЛПОНП вследствие нарушения в печени больных синтеза одного из структурных белков этих липопротеинов. Так как витамин Е транспортируется в крови в составе хиломикронов и ЛПНП, то отсутствие последних приводит к нарушению всасывания токоферола и поступления его в ткани. Клинически это проявляется в резком снижении гемолитической устойчивости эритроцитов и акантоцитозе, пигментном ретините, мышечной слабости и атаксической нейропатии. Лечение сводится к ограничению потребления жиров и дополнительному введению водорастворимых форм жирорастворимых витаминов (например, токоферилполиэтиленгликоль сукцинат).
Врождённая дисэритропоэтическая анемия типа II. При этом заболевании увеличивается расход витамина Е на процесс стабилизации и защиты от перекисной деструкции дефектных эритроцитарных мембран.
Врождённые мышечные дистрофии. В некоторых случаях дистрофия мышц обуславливается врождённым нарушением процесса поступления или обмена в них токоферола.
Оценка обеспеченности организма токоферолом. Основным методом является определение концентрации витамина Е в крови. Однако при гипер-β-липопротеинемиях (в том числе и возрастных) содержание токоферола в крови не отражает уровень обеспеченности им тканей организма (ЛПНП- одна из транспортных форм витамина).
Наиболее доступны клинической лаборатории функциональные тесты, позволяющие оценить глубину Е-витаминной недостаточности. Основными являются тесты на перекисную или гемолитическую устойчивость эритроцитов, определение суточной экскреции креатина (мышцы при Е-гиповитаминозе плохо «удерживают» креатин) и содержание продуктов ПОЛ в крови и эритроцитах.
Гипервитаминоз. Витамин не токсичен при значительных (10-20-кратных к суточной потребности) и длительных превышениях его дозировки, что обусловлено ограничением способности специфических токоферол-связывающих белков печени включать витамин в состав ЛПОНП. Его избыток выводится из организма с желчью. В некоторых случаях длительный приём мегадоз токоферола (более 1г/сутки) может привести к гипертриглицеридемии и повышению кровяного давления.
Суточная потребность. Пищевые источники. Основной источник токоферола – растительные масла, однако только свежие, получаемые методом холодного прессования. Поскольку растительное масло обычно экстрагируют из семян при высокой температуре, затем подвергают очистке, дезодорированию и рафинированию, оно значительно обедневает токоферолом. Более того, избыток растительных масел в рационе усиливает недостаточность витамина Е в организме, так как он расходуется на интенсифицированный потреблением ненасыщенных жирных кислот масел процесс ПОЛ.
Лучшим пищевым источником витамина Е являются орехи, семечки, гречневая крупа, проросшие ростки пшеницы. Он содержится в листьях салата и капусты. Из продуктов животного происхождения более всего токоферолов в сливочном масле, сале, мясе, желтке яиц. В молоке этого витамина мало.
Суточная потребность – 10 мг. Однако токоферол быстро расходуется в организме, особенно в условиях стимулированного ПОЛ, что имеет место при многих заболеваниях. Окислительной деструкции витамина Е препятствует витамин С. Это обусловлено присут Это обусловлено присутствием в молекуле последнего енольной группы - донора водорода, который способен «гасить» свободный радикал токоферола. Тем самым витамин С экономит фонд витамина Е. С целью усиления антиоксидантного эффекта токоферола его следует назначать с аскорбиновой кислотой.
Витамин Д (кальциферол), антирахитический.
Химическое строение и свойства. В 1936 г. А. Виндаусом из рыбьего жира был выделен препарат, излечивающий рахит. Он был назван витамином Д3, так как ранее А. Гессом и М. Вейнштоком из растительных масел был выделен эргостерин, получивший название витамин Д1. При воздействии на витамин Д1 УФ-лучей образовывалось излечивающее рахит соединение – витамин Д2, эргокальциферол (кальциферол означает несущий кальций). В растениях при УФ-облучении синтезируются и другие витамеры эргостерина (Д4 -7).
Наиболее важным из группы витаминов Д является витамин Д3 –холекальциферол. Холекальциферол образуется в качестве промежуточного продукта при биосинтезе холестерола (из 7-дегидрохолестерола) в клетках кожи человека под влиянием УФ-лучей.
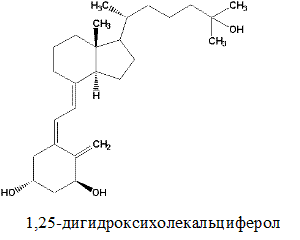
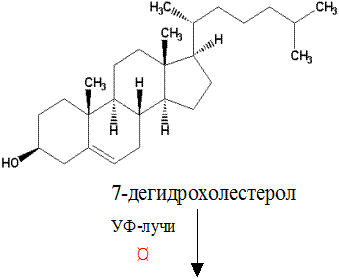
Витамин Д3 (холекальциферол)
Метаболизм. Витамины группы Д всасывается подобно витамину А (см. выше). В печени витамины подвергаются гидроксилированию микросомной системой оксигеназ по С-25 (из витамина Д3 образуется 25(ОН)-Д3, т.е. 25-гидроксихолекальциферол) и затем переносятся с током крови с помощью специфического транспортного белка в почки. В почках осуществляется вторая реакция гидроксилирования по С-1 с помощью митохондриальных оксигеназ (образуется 1,25(ОН)2-Д3, т.е. 1,25-дигидрокси-холекальциферол, или кальцитриол). Эта реакция активируется паратиреоидным гормоном, секретируемым паращитовидной железой, когда уровень кальция в крови снижается. Если уровень кальция адекватен физиологической потребности организма, вторичное гидроксилирование происходит по С-24 (вместо С-1), при этом образуется неактивный метаболит 1,24(ОН)2-Д3. В реакциях гидроксилирования принимает участие витамин С.
Витамин Д3 накапливается в жировой ткани. Выводится главным образом с калом в неизменённом или окисленном виде, а также в виде конъюгатов.
Биохимические функции. Витамин Д3 можно рассматривать как про гормон, так как он превращается в 1,25(ОН)2-Д3, действующий аналогично стероидным гормонам. Так, проникая в клетки-мишени, он связывается с белковыми рецепторами, которые мигрируют в ядро клетки. В энтероцитах этот гормон-рецепторный комплекс стимулирует транскрипцию iРНК, несущую информацию на синтез белка-переносчика ионов кальция. Вероятно, витамин отвечает также за синтез Са2+-АТФ-азы в разных клетках.
В кишечнике всасывание кальция осуществляется как путём облегченной диффузии (с участием кальций-связывающего белка), так и путём активного транспорта (с помощью Са2+-АТФ-азы). Одновременно ускоряется и всасывание фосфора.
В костной ткани 1,25(ОН)2-Д3стимулирует процесс деминерализации (синергично с паратирином).
В почках активация витамином 1,25(ОН)2-Д3кальциевой АТФ-азы мембран почечных канальцев приводит к увеличению реабсорбции ионов кальция; возрастает и реабсорбция фосфатов.
Кальцитриол принимает участие в регуляции роста и дифференцировке клеток костного мозга. Он обладает антиоксидантным и антиканцерогенным действием.
Гиповитаминоз. Недостаток витамина Д у детей приводит к заболеванию рахитом. Основные проявления этого заболевания сводятся к симптоматике недостаточности кальция. Прежде всего страдает остеогенез: отмечается деформация скелета конечностей (искривление их в результате размягчения – остеомаляции), черепа (позднее заращение родничков), грудной клетки (появление своеобразных «чёток» на костно-хрящевой границе рёбер), задерживается прорезывание зубов. Развивается гипотония мышц (увеличенный живот), возрастает нервно-мышечная возбудимость (у младенца выявляется симптом облысения затылочка из-за частого вращения головкой), возможно появлние судорог. У взрослого недостаточность кальция в организме приводит к кариесу и остеомаляции (размягчение кости); у пожилых – к развитию остеопороза (снижение плотности костной ткани вследствие нарушения остеосинтеза). Разрушение неорганического матрикса объясняется усиленным «вымыванием» кальция из костной ткани и нарушением реабсорбции кальция в почечных канальцах при дефиците витамина Д:
На схеме показано угнетение (пунктирная стрелка) всасывания, снижение поступления кальция в кость и уменьшение экскреции кальция при недостатке витамина Д. Одновременно в ответ на гипокальциемию секретируется паратирин и увеличивается (сплошная стрелка) поступление кальция из кости в кровяное русло (вторичный гиперпаратиреоидизм).
|
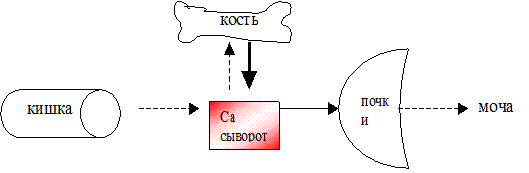
На схеме показано угнетение (пунктирная стрелка) всасывания, снижение поступления кальция в кость и уменьшение экскреции кальция при недостатке витамина Д. Одновременно в ответ на гипокальциемию секретируется паратирин и увеличивается (сплошная стрелка) поступление кальция из кости в кровяное русло (вторичный гиперпаратиреоидизм).
 2014-02-09
2014-02-09 5951
5951