Причину отклонения растворов электролитов от законов Рауля и Вант-Гоффа впервые объяснил шведский ученый С. Аррениус. Он показал, что электролиты за счет действия молекул растворителя распадаются на ионы. Этот процесс приводит к увеличению реального числа частиц растворенного вещества.
Изотонический коэффициент показывает, во сколько раз реальное число частиц растворенного вещества больше, чем теоретически ожидаемое (если предполагать, что вещество в растворе присутствует только в виде молекул).
Для идеальных растворов электролитов i >1.
Коэффициент Вант-Гоффа показывает также, во сколько раз наблюдаемое опытное значение росм., Dtкип., Dtзам., 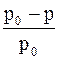 больше теоретически вычисленного, т.е.:
больше теоретически вычисленного, т.е.:
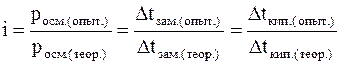
Максимально значение изотонического коэффициента (imax) для любого электролита будет при этом равно числу ионов, которые образуются при полной диссоциации его молекулы (или формульной единицы), т.к. именно во столько раз возрастет число частиц электролита в растворе.
 Сванте Аррениус (1859 – 1927). Шведский физикохимик, основные работы которого посвящены учению о растворах и кинетике химических реакций. Он получил Нобелевскую премию по химии в 1903 году за создание теории электролитической диссоциации. Также им была разработана одна из наиболее известных теорий кислот и оснований. Однако еще большую известность имеют его работы в области химической кинетики. С. Аррениус высказал мысль, что реакционными являются не все, а только активные молекулы. Он ввел понятие энергии активации и вывел уравнение зависимости константы скорости реакции от температуры, носящее его имя.
Сванте Аррениус (1859 – 1927). Шведский физикохимик, основные работы которого посвящены учению о растворах и кинетике химических реакций. Он получил Нобелевскую премию по химии в 1903 году за создание теории электролитической диссоциации. Также им была разработана одна из наиболее известных теорий кислот и оснований. Однако еще большую известность имеют его работы в области химической кинетики. С. Аррениус высказал мысль, что реакционными являются не все, а только активные молекулы. Он ввел понятие энергии активации и вывел уравнение зависимости константы скорости реакции от температуры, носящее его имя.
Так, для NaCl imax = 2, для Na3PO4 imax = 4.
В реальных растворах диссоциация часто протекает не полностью, особенно если электролит является слабым.
Кроме того, наблюдаются межионные взаимодействия, приводящие к уменьшению числа кинетически активных частиц.
В этом случае величина i будет меньше его возможного максимального значения и будет зависеть от степени диссоциации электролита:
i = 1 + α (m – 1)
где α – степень диссоциации электролита (в долях единицы); m – число ионов, образующихся при полном распаде одной молекулы или одной формульной единицы электролита.
Таким образом, из двух растворов однотипных электролитов (т.е. распадающихся на одно и то же число ионов) с одинаковой молярной концентрацией изотонический коэффициент будет больше в растворе электролита с более высокой степенью диссоциации α. Соответственно, и росм., Dtкип., Dtзам. для такого раствора тоже будут иметь большие значения.
Если же молярная концентрация и степень диссоциации электролитов разного типа в растворе одинаковые, то значение i будет выше для электролита, диссоциирующего на большее число ионов m.
Электролиты и неэлектролиты. Теория
электролитической диссоциации
Все вещества делятся на 2 большие группы: электролиты и неэлектролиты.
Электролитами называются вещества (исключая металлы), растворы или расплавы которых проводят электрический ток. К электролитам относятся соединения, образованные ионными или ковалентными полярными связями. Это сложные вещества: соли, основания, кислоты, оксиды металлов (проводят электрический ток только в расплавах).
Неэлектролитами называются вещества, растворы или расплавы которых электрический ток не проводят. К ним относятся простые и сложные вещества, образованные малополярными или неполярными ковалентными связями.
Свойства растворов и расплавов электролитов впервые объяснил в конце XIX века шведский учёный Сванте Аррениус. Им была создана специальная теория электролитической диссоциации, основные положения которой, доработанные и развитые другими учёными, в настоящее время формулируются следующим образом.
1. Молекулы (или формульные единицы) электролитов в растворах или расплавах распадаются на положительно и отрицательно заряженные ионы. Этот процесс называется электролитической диссоциацией. Общая сумма зарядов положительных ионов равна сумме зарядов отрицательных ионов, поэтому растворы или расплавы электролитов в целом остаются электронейтральными. Ионы могут быть как простые, состоящие только из одного атома (Na+, Cu2+, Cl–, S2-), так и сложные, состоящие из атомов нескольких элементов (SO42–, PO43–, NH4+, [Al(OH)4]–).
Простые ионы по своим физическим, химическим и физиологическим свойствам существенно отличаются от нейтральных атомов, из которых они образовались. В первую очередь, ионы являются гораздо более устойчивыми частицами, чем нейтральные атомы, и могут существовать в растворах или расплавах неограничено долгое время, не вступая в необратимое взаимодействие с окружающей средой.
Такое различие в свойствах атомов и ионов одного и того же элемента объясняется разным электронным строением этих частиц.
Так, простые ионы s- и p-элементов находятся в более устойчивом состоянии, чем нейтральные атомы, потому что имеют завершённую электронную конфигурацию внешнего слоя, например:
| Nao | – 1ē ® | Na+ | |
| 1s22s22p6 3s1 | 1s2 2s22p6 | ||
| нейтральный атом натрия; на внешнем электронном слое находится один электрон | положительно заряженный ион натрия; на внешнем электронном слое находится 8 электронов (как у ближайшего благородного газа неона) | ||
| Fo | + 1ē ® | F– | |
| 1s2 2s22p5 | 1s2 2s22p6 | ||
| нейтральный атом фтора; на внешнем электронном слое находится 7 электронов | отрицательно заряженный ион фтора; на внешнем электронном слое находится 8 электронов | ||
Распад электролитов на ионы в расплавах осуществляется за счёт действия высоких температур, а в растворах за счёт действия молекул растворителя.
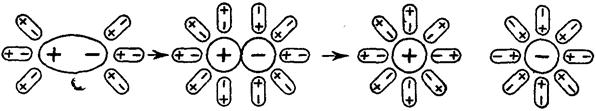
Особенностью ионных соединений является то, что в узлах их кристаллической решётки имеются уже готовые ионы, и в процессе растворения таких веществ диполям растворителя (воды) остаётся только разрушить эту ионную решётку (рис. 18).
Вещества, образованные полярными ковалентными связями, переходят в раствор в виде отдельных молекул, которые, как и молекулы Н2О, представляют собой диполи, например:

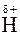 ¾
¾ 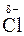 ® + –
® + –
В этом случае диполи Н2О, ориентируясь соответствующим образом вокруг растворенной молекулы электролита, вызывают в ней дальнейшую поляризацию ковалентной связи, а затем и её окончательный гетеролитический разрыв (рис. 29).
H – Cl ® H+ + Cl
 2014-02-09
2014-02-09 1747
1747