Закон Генри — закон, по которому при постоянной температуре растворимость газа в данной жидкости прямо пропорциональна давлению этого газа над раствором. Закон пригоден лишь для идеальных растворов и невысоких давлений.

Закон Генри описывает процесс растворения газа в жидкости. Что представляет собой жидкость, в которой растворен газ, мы знаем на примере газированных напитков — безалкогольных, слабоалкогольных, а по большим праздникам — шампанского. Во всех этих напитках растворена двуокись углерода (химическая формула CO2) — безвредный газ, используемый в пищевой промышленности по причине его хорошей растворимости в воде, а пенятся после открытия бутылки или банки все эти напитки по той причине, что растворенный газ начинает выделяться из жидкости в атмосферу, поскольку после открытия герметичного сосуда давление внутри падает.
Собственно, закон Генри констатирует достаточно простой факт: чем выше давление газа над поверхностью жидкости, тем труднее растворенному в ней газу высвободиться. И это совершенно логично с точки зрения молекулярно-кинетической теории, поскольку молекуле газа, чтобы вырваться на свободу с поверхности жидкости, нужно преодолеть энергию соударений с молекулами газа над поверхностью, а чем выше давление и, как следствие, число молекул в приграничной области, тем сложнее растворенной молекуле преодолеть этот барьер.
В формуле мы использовали:
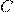 — Концентрация газа в растворе в долях моля
— Концентрация газа в растворе в долях моля
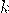 — Коэффициент Генри
— Коэффициент Генри
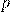 — Парциальное давление газа над раствором
— Парциальное давление газа над раствором
Закон излучения Кирхгофа - отношение испускательной и поглощательной способностей не зависит от природы тела, оно является для всех тел одной и той же.
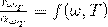
По определению, абсолютно чёрное тело поглощает всё падающее на него излучение, то есть для него 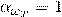 (Поглощательная способность тела). Поэтому функция совпадает с испускательной способностью
(Поглощательная способность тела). Поэтому функция совпадает с испускательной способностью 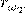
В формуле мы использовали:
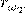 — Испускательная способность тела
— Испускательная способность тела
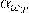 — Поглощательная способность тела
— Поглощательная способность тела
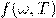 — Функция Кирхгофа
— Функция Кирхгофа
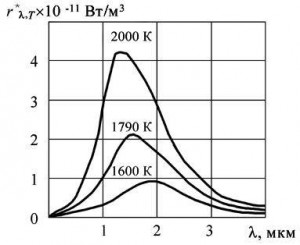
Закон Стефана-Больцмана — Энергетическая светимость абсолютно черного тела пропорциональна четвертой степени абсолютной температуры.
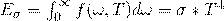
Из формулы видно, что при повышении температуры светимость тела не просто возрастает — она возрастает в значительно большей степени. Увеличьте температуру вдвое, и светимость возрастет в 16 раз!
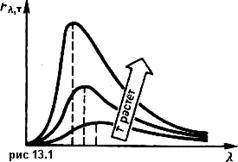
Нагретые тела излучают энергию в виде электромагнитных волн различной длины. Когда мы говорим, что тело «раскалено докрасна», это значит, что его температура достаточно высока, чтобы тепловое излучение происходило в видимой, световой части спектра. На атомарном уровне излучение становится следствием испускания фотонов возбужденными атомами.
Чтобы понять, как действует этот закон, представьте себе атом, излучающий свет в недрах Солнца. Свет тут же поглощается другим атомом, излучается им повторно — и таким образом передается по цепочке от атома к атому, благодаря чему вся система находится в состоянии энергетического равновесия. В равновесном состоянии свет строго определенной частоты поглощается одним атомом в одном месте одновременно с испусканием света той же частоты другим атомом в другом месте. В результате интенсивность света каждой длины волны спектра остается неизменной.
Температура внутри Солнца падает по мере удаления от его центра. Поэтому, по мере движения по направлению к поверхности, спектр светового излучения оказывается соответствующим более высоким температурам, чем температура окружающий среды. В результате, при повторном излучении, согласно закону Стефана—Больцмана, оно будет происходить на более низких энергиях и частотах, но при этом, в силу закона сохранения энергии, будет излучаться большее число фотонов. Таким образом, к моменту достижения им поверхности спектральное распределение будет соответствовать температуре поверхности Солнца (около 5 800 К), а не температуре в центре Солнца (около 15 000 000 К).
Энергия, поступившая к поверхности Солнца (или к поверхности любого горячего объекта), покидает его в виде излучения. Закон Стефана—Больцмана как раз и говорит нам, какова излученная энергия.
В вышеприведенной формулировке закон Стефана—Больцмана распространяется только на абсолютно черное тело, поглощающее всё попадающее на его поверхность излучение. Реальные физические тела поглощают лишь часть лучевой энергии, а оставшаяся часть ими отражается, однако закономерность, согласно которой удельная мощность излучения с их поверхности пропорциональна Т в 4, как правило, сохраняется и в этом случае, однако постоянную Больцмана в этом случае приходится заменять на другой коэффициент, который будет отражать свойства реального физического тела. Такие константы обычно определяются экспериментальным путем.
В формуле мы использовали:
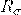 — Энергетическая светимость тела
— Энергетическая светимость тела
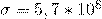 — Постоянная Стефана-Больцмана
— Постоянная Стефана-Больцмана
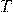 — Абсолютная температура
— Абсолютная температура
Закон Шарля — давление данной массы идеального газа при постоянном объеме прямо пропорционально абсолютной температуре
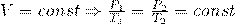
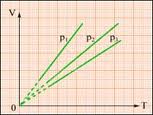
Чтобы легче было понять закон Шарля, представьте себе воздух внутри воздушного шарика. При постоянной температуре воздух в шарике будет расширяться или сжиматься, пока давление, производимое его молекулами, не достигнет 101 325 паскалей и не сравняется с атмосферным давлением. Иными словами, пока на каждый удар молекулы воздуха извне, направленный внутрь шарика, не будет приходиться аналогичный удар молекулы воздуха, направленный изнутри шарика вовне.
Если понизить температуру воздуха в шарике (например, положив его в большой холодильник), молекулы внутри шарика станут двигаться медленнее, менее энергично ударяя изнутри о стенки шарика. Молекулы наружного воздуха тогда будут сильнее давить на шарик, сжимая его, в результате объем газа внутри шарика будет уменьшаться. Это будет происходить до тех пор, пока увеличение плотности газа не компенсирует понизившуюся температуру, и тогда опять установится равновесие.
Так же есть:
Уравнение Менделеева Клапейрона: 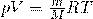
Закон Гей Люссака: 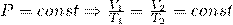
Закон Бойля Мариотта: 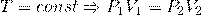
В законе мы использовали:
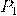 — Давление в 1 сосуде
— Давление в 1 сосуде
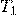 — Температура в 1 сосуде
— Температура в 1 сосуде
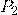 — Давление в 2 сосуде
— Давление в 2 сосуде
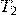 — Температура в 2 сосуде
— Температура в 2 сосуде
Первый закон термодинамики — Изменение внутренней энергии ΔU не изолированной термодинамической системы равно разности между количеством теплоты Q, переданной системе, и работой A внешних сил

Вместо работы А, совершаемой внешними силами над термодинамической системой, часто удобнее бывает рассматривать работу A’, совершаемую термодинамической системой над внешними телами. Так как эти работы равны по абсолютному значению, но противоположны по знаку:
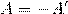
Тогда после такого преобразования первый закон термодинамики будет иметь вид:
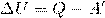
Первый закон термодинамики — В не изолированной термодинамической системе изменение внутренней энергии равно разности между полученным количеством теплоты Q и работой A’, совершаемой данной системой
Говоря простым языком первый закон термодинамики говорит о энергии, которая не может сама создаваться и исчезать в никуда, она передается от одной системы к другой и превращается из одной формы в другую (механическая в тепловую).
Важным следствием первого закона термодинамики является то, что невозможности создать машину (двигатель), которая способна совершать полезную работу без потребления энергии извне. Такая гипотетическая машина получила название вечного двигателя первого рода.
1. В изохорном процессе (V=const). При изохорном процессе объем газа остается постоянным, поэтому газ не совершает работу. Изменение внутренней энергии газа происходит благодаря теплообмену с окружающими телами:
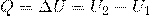
Здесь U1 и U2 – внутренние энергии газа в начальном и конечном состояниях. Внутренняя энергия идеального газа зависит только от температуры. При изохорном нагревании тепло поглощается газом Q > 0, и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам Q < 0
2. В изобарном процессе (P=const). При изобарном расширении газа подведенное к нему количество теплоты расходуется как на увеличение его внутренней энергии и на совершение работы газом:
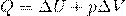
При изобарном расширении Q > 0 – тепло поглощается газом, и газ совершает положительную работу. При изобарном сжатии Q < 0 – тепло отдается внешним телам. В этом случае A < 0. Температура газа при изобарном сжатии уменьшается, T2 < T1; внутренняя энергия убывает, ΔU < 0.
3. В изотермическом процессе (T=const). При изотермическом процессе температура газа не изменяется, следовательно, не изменяется и внутренняя энергия газа, ΔU = 0.

Количество теплоты Q, полученной газом в процессе изотермического расширения, превращается в работу над внешними телами. При изотермическом сжатии работа внешних сил, произведенная над газом, превращается в тепло, которое передается окружающим телам. Наряду с изохорным, изобарным и изотермическим процессами в термодинамике часто рассматриваются процессы, протекающие в отсутствие теплообмена с окружающими телами.
4. В адиабатном процессе (Q=0). При адиабатном процессе первый закон термодинамики выглядит:
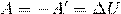
То есть газ совершает работу за счет убыли его внутренней энергии. На плоскости (p, V) процесс адиабатического расширения (или сжатия) газа изображается кривой, которая называется адиабатой. При адиабатическом расширении газ совершает положительную работу (A > 0); поэтому его внутренняя энергия уменьшается (ΔU < 0). Это приводит к понижению температуры газа. Вследствие этого давление газа при адиабатическом расширении убывает быстрее, чем при изотермическом расширении.
В Формуле мы использовали:
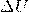 — Изменение внутренней энергии
— Изменение внутренней энергии
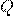 — Количество теплоты
— Количество теплоты
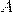 — Работа внешних сил
— Работа внешних сил
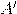 — Работа совершаемая системой
— Работа совершаемая системой
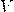 — Объем газа
— Объем газа
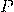 -Давление газа
-Давление газа
 2014-02-24
2014-02-24 5595
5595