П р о м е ж у т о ч н ы е т е с т ы к теме 1.2
I. Каков наиболее вероятный порядок величины периода (параметра) кри-
сталлической решетки?
1. 10-1 см. 2. 10-6 см. 3. 10-8 см. 4. 10-10 см. 5. 101 см.
II. Сколько целых атомов приходится на элементарную ячейку простой
кубической решетки?
1. 8. 2. 1/8. 3. 1. 4. 6. 5. 4.
III. Какой вид дефектов кристаллической решетки обеспечивает высокую
пластичность металлов?
1. Вакансии.
2. Дислокации.
3. Атомы примесей.
4. Дислоцированные (междоузельные) атомы. 5. Границы зерен.
IV. Какое из перечисленных утверждений неверно? Холодная пластиче-
ская деформация:
1) повышает прочность металла;
2) повышает электросопротивление; 3) снижает пластичность;
4) повышает ударную вязкость; 5) повышает твердость.
V. Какое из перечисленных утверждений неверно? Практические пути
повышения прочности металлов основаны на:
1) увеличении количества точечных дефектов; 2) измельчении зерна;
3) торможении дислокаций;
4) введении примесных атомов; 5) полном удалении дислокаций.
В конце предыдущей темы отмечалось, что создание сплавов – наиболее
общий путь повышения прочности металлических материалов. Этот метод
(сплавления) позволяет получить также более широкий диапазон особых полез-
ных свойств (например, жаропрочность, коррозионную стойкость, тепло – и из-
носостойкость и др.).
Сплавы – это материалы, полученные сплавлением или спеканием (по-
рошковая металлургия) двух или более компонентов.
Компоненты – вещества, образующие сплав; ими могут быть химиче-
ские элементы или устойчивые химические соединения.
Структура и свойства сплава определяются в первую очередь природой
(типом) фаз, образующихся при сплавлении компонентов.
Фаза – однородная по химическому составу, типу решетки и свойствам
часть сплава, отделенная от других частей границей раздела.
В зависимости от характера физико–химического взаимодействия компо-
нентов в металлических сплавах возможны три основных типа твердых (кри-
сталлических) фаз:
1) химические элементы,
2) химические соединения,
3) твердые растворы.
Основной (матричной) фазой большинства промышленных сплавов яв-
ляются твердые растворы, поэтому рассмотрим их более подробно.
Твердые растворы – это фазы, в которых атомы одного компонента В
размещены (растворены) в кристаллической решетке другого компонента А –
«растворителя». По мере увеличения числа атомов В в решетке А химический
состав и свойства твердого раствора плавно изменяются (в частности, темпера-
тура плавления), т.е. это фазы переменного состава (в отличие от химических
элементов и химических соединений).
Сплав, представляющий собой твердый раствор, является однофазным
веществом с решеткой, присущей основному компоненту (растворителю).
Атомы второго компонента (растворенного) размещены в решетке растворите-
ля, как правило, случайным, неупорядоченным образом.
По способу размещения атомов растворенного вещества (В) в решетке А
различают два основных типа твердых растворов – растворы замещения и вне-
дрения (рис. 1.3.1)
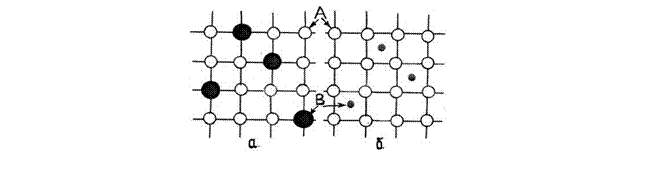 Рис. 1.3.1. Твердые растворы замещения (а) и внедрения (б)
Рис. 1.3.1. Твердые растворы замещения (а) и внедрения (б)
Видно, что при образовании твердых растворов замещения атомы В рас-
полагаются в вакансиях решетки компонента А (см. рис. 1.2.5). При этом коли-
чество атомов В в решетке А может изменяться в широких пределах (при опре-
деленных условиях возможна даже неограниченная взаимная растворимость
компонентов в твердом состоянии).
В случае твердых растворов внедрения атомы В располагаются в междо-
узлиях решетки А. Понятно, что это возможно, если размеры атомов В сравни-
мы с размерами межатомных пустот решетки А. Поэтому растворы внедрения
образуют с металлами элементы, имеющие наименьший атомный радиус (H, B,
C, N). Такие растворы всегда имеют ограниченную растворимость.
Очевидно, что растворенные атомы (В) являются точечными дефектами,
вызывающими искажение решетки А (см. рис. 1.2.6), поэтому образование
сплавов – твердых растворов должно приводить к повышению прочности ис-
ходных компонентов (см. параграфы 1.2.2 и 1.2.3).
Химические соединения обычно имеют фиксированный состав, отве-
чающий формуле АnВm, где n и m – простые числа, причем тип решетки соеди-нения АnВm отличается от решетки исходных компонентов.
В железоуглеродистых сплавах (сталях и чугунах), которые обсуждаются в последующих темах, наиболее важны соединения металлов (например, желе-
за) с углеродом – карбиды.
Независимо от природы химические соединения в металлических спла-
вах, как правило, обладают высокой твердостью и хрупкостью (т.е. малопла-
стичны); твердые растворы, напротив, имеют хорошую пластичность (и вяз-
кость), но невысокую прочность и твердость.
Поэтому оптимальному сочетанию свойств конструкционных металли-
ческих сплавов (высоким значения прочности и ударной вязкости) соответству-
ет структура, в которой дисперсные (» 10 нм) частицы твердых химических со-
единений равномерно и достаточно плотно (на расстояниях» 20…40 нм) рас-
пределены в пластичной матричной фазе – твердом растворе.
Исходя из этого можно сказать, что свойства сплавов зависят в первую
очередь от природы и относительных количеств присутствующих фаз, но
также и от формы, размеров, взаимного расположения кристаллов этих
фаз, т.е. от конкретной структуры сплава. Например, если частицы химиче-
ских соединений расположены в виде сетки в твердом растворе, эксплуатаци-
онная надежность такого материала будет понижена из-за возможности облег-
ченного разрушения по хрупким оболочкам (химических соединений), разоб-
щающим зерна твердого раствора.
Итак, свойства сплавов (данного химического состава) определяются
их структурой. Чтобы прогнозировать свойства какого-либо сплава, нужно
знать его структуру.
Структуру сплавов различного химического состава можно установить
путем анализа соответствующих диаграмм фазового равновесия или диа-грамм состояния. 1
Под состоянием понимают наличие тех или иных фаз в сплаве данного
химического состава при данной температуре. То есть диаграммысостояния
строятся в координатах «температура–химический состав сплавов системы
А–В».
 1Прямой метод изучения структуры – микроанализ - исследование микроструктуры мате-риалов с помощью микроскопов; ему посвящен ряд лабораторных работ.
1Прямой метод изучения структуры – микроанализ - исследование микроструктуры мате-риалов с помощью микроскопов; ему посвящен ряд лабораторных работ.
Линии диаграмм состояния – это линии фазовых превращений («критиче-
ские линии»), при пересечении которых фазовый состав (структура) сплавов
обязательно изменяется.
Умение анализировать диаграммы состояния является важной частью ос-
воения курса материаловедения. К сожалению, из-за ограниченности объема
«Опорного конспекта» нет возможности посвятить этому вопросу отдельную
тему, но рекомендуется самостоятельно проработать соответствующую тему
(см. [1…4, 8]). Это облегчит усвоение материала последующих тем, посвящен-
ных структуре и свойствам конкретных промышленных сплавов.
Внимание!
Тема 1.3 – небольшая по объему и достаточно простая для восприятия,
однако она содержит ряд новых понятий, для усвоения которых требуются
определенные усилия, поэтому…
 2014-02-24
2014-02-24 562
562








