Тема 3 Обмен веществ и энергии растительной клетки
Раздел 1 Основы физиологии и биохимии растительной клетки
Вопросы к ЛК 3
1. Какой из названных ниже видов электромагнитного излучения обладает наибольшей частотой?
· Инфракрасное
· Видимый свет
· Ультрафиолетовое
· Рентгеновское
· Радиоволны
2. Какой из названных ниже видов электромагнитного излучения обладает наименьшей частотой?
· Видимый свет
· Ультрафиолет
· ИК
· Рентгеновское
· Радиоволны
3. Какое из трех типов ядерных излучений: альфа-излучение, бета-излучение, гамма-излучение, является электромагнитным излучением?
4. Какая из представленных последовательностей соответствует росту частоты ЭМИ?
· рентгеновское, гамма, УКВ – радиоволны
· инфракрасное излучение, видимое, у/ф
· радиоволны, рентеновские, видимый свет
· гамма-излучение, рентгеновское, видимое излучение
5. Назовите природные источники ЭМИ.
6. Назовите искусственные источники ЭМИ.
7. Охарактеризуйте волновую модель ЭМИ.
8. В чем отличие пассивных методов ДЗ от активных?
1. Внешний обмен и метаболизм клетки. Клеточная энергетика
2. Строение, функции и классификация ферментов
3. Биосинтез белка в клетке
4. Регуляция процессов на уровне клетки
Все живые существа состоят из клеток. Клетка является не только его структурной, но и функциональной единицей. Живая клетка состоит из тех же химических элементов, что и неживая природа. Процессы, происходящие в клетке, подчиняются общим законам физики и химии. Согласно первому закону термодинамики энергия для клеточной работы не может создаваться из ничего и исчезать бесследно. Согласно второму закону термодинамики в клетке последовательно возрастает энтропия и происходит «разупорядочение» структуры. По сравнению с неживыми структурами скорость возрастания энтропии в живых системах минимальная.
Живые организмы представляют собой открытые системы, которые обмениваются с окружающей средой энергией, веществом и информацией.
Фотосинтезирующие клетки растений потребляют солнечную энергию и превращают ее в химическую форму. Универсальной клеточной «валютой» служат молекулы АТФ, обеспечивающие важнейшие процессы жизнедеятельности, прежде всего – биосинтезы. Часть энергии АТФ затрачивается на механическую работу (например, движение цитоплазмы), другая часть идет на активный транспорт веществ против физико-химических градиентов. Большую роль играют в клетке механизмы, обеспечивающие сигналы о быстрых изменениях окружающей среды. При этом часть энергии АТФ превращается в электрическую (биопотенциалы) или световую (биохемилюминесценция), которые вновь высвобождаются в окружающую среду. Образованные при фотосинтезе органические вещества участвуют в другом важнейшем процессе - дыхании. Окислительный распад дыхательных субстратов приводит к освобождению заключенной в них энергии - часть ее вновь локализуется в молекулах АТФ и может затем использоваться по перечисленным направлениям. Более половины энергии окисления превращается в теплоту и в этой форме выделяется в окружающую среду. Таким образом осуществляется обмен энергией между клеткой и средой.
Обмен веществом включает процесс поглощения из окружающей среды диоксида углерода, воды, минеральных веществ, участвующих в клетке в многочисленных биохимических реакциях. В результате этих процессов клетка строит и поддерживает свои структуры, а продукты распада и отходы жизнедеятельности выходят в окружающую среду, где они подвергаются превращениям.
Обмен информацией начинается с восприятия клеткой сигналов от внешних раздражителей. Возникающее в клетке возбуждение приводит к изменению функциональной активности клетки. Сигналы о происшедших переменах клетка посылает в окружающую среду.
Компартментация клетки. Все клетки имеют много общих черт: они ограничены от внешней среды цитоплазматической мембраной, содержат системы хранения и реализации генетической информации, системы получения и преобразования энергии, системы обеспечения клетки необходимыми веществами и компонентами, системы восприятия внешних сигналов, их анализа и организации адекватного ответа. Различия между клетками связаны с их специализацией (дифференцировкой), позволяющей максимально эффективно выполнить конкретную функцию, «заданную» организмом. Наиболее существенны различия между клетками организмов, принадлежащих к различным царствам. Прокариотическая клетка не имеет оформленного ядра и не содержит внутренних перегородок. Эукариотическая клетка разделена мембранами на несколько отсеков (компартментов). Компартменты эукариотической клетки называют органеллами. Органеллы специализируются на выполнении различных функций. Разделение клетки на компартменты, возможно, является следствием ее больших размеров (современная эукариотическая клетка больше бактериальной в 10-30 раз). При этом увеличение объема клетки сопровождается существенно меньшим увеличением поверхности ее плазматической мембраны, где протекают многие важнейшие метаболические процессы. Кроме того, с увеличением объема клетки затрудняется координация ее метаболизма (например, «доставка» нужных веществ в нужное место). Формирование компартментов позволяет пространственно разделить блоки метаболизма.
Все живые организмы не могут оставаться живыми и поддерживать высокий уровень организации без постоянного притока энергии извне. При этом они могут использовать только две формы внешней энергии - световую и химическую. Именно по способу получения энергии организмы делят на фототрофы и хемотрофы. Растения получают энергию в виде электромагнитного излучения Солнца, а животные используют энергию, заключенную в ковалентных связях органических молекул, которые поступают в организм с пищей. Полагают, что первые организмы древней Земли располагали избытком органических соединений, образующихся в ходе геохимических процессов. Они извлекали энергию, окисляя органические соединения в процессах, видимо, сходных с различными видами брожения. Эту способность сохранили клетки всех ныне живущих организмов, способные получать энергию при анаэробном распаде глюкозы в процессе гликолиза. Однако по мере исчерпания запасов органики эволюционное развитие получили фототрофы, использующие энергию света в процессе фотосинтеза и способные синтезировать углеводы из атмосферного СО2 и воды. Фотосинтез сопровождался образованием молекулярного кислорода. Насыщение атмосферы кислородом привело к возникновению и эволюционному доминированию аэробных форм жизни, которые научились получать необходимую им энергию в результате окислении углеводов кислородом в процессе дыхания. Дальнейшая эволюция разделила живых существ на прокариоты и эукариоты, одноклеточные и многоклеточные, на растения и животные, но возникшие на ранних этапах эволюции механизмы использования клеткой энергии остались в своей основе неизменными.
При всем разнообразии живых существ и условий среды, в которых они обитают, для получения энергии ими используются три основных процесса - гликолиз, дыхание и фотосинтез. При этом, несмотря на все различия в метаболизме растений, животных и бактерий, способы преобразования внешней энергии, будь то энергия света или энергия субстратов дыхания, в клеточные формы энергии базируются на общих фундаментальных принципах и подчиняются общим законам. Основой этих законов является прежде всего то, что все процессы в живой клетке подчиняются законам физики и химии и могут быть описаны с позиций термодинамики.
Первый закон термодинамики - закон о сохранении энергии, согласно которому энергия не может появляться или исчезать и переходит из одной формы в другую. Живая клетка как раз и представляет собой систему, в которой постоянно происходит преобразование, или трансформация, одних форм энергии в другие, и прежде всего энергии внешних источников во внутренние энергетические ресурсы самой клетки.
Второй закон термодинамики утверждает, что в изолированной системе самопроизвольно могут идти только те процессы, в результате которых степень неупорядоченности, или энтропия, возрастает, и система переходит из менее вероятного в более вероятное состояние.
В то же время очевидно, что все живые системы организованы сложным образом - множество атомов собраны в чрезвычайно сложные молекулы, а молекулы - в исключительно точные структуры. При этом живая клетка демонстрирует удивительную стабильность и, поддерживая свой внутренний порядок, координирует в пространстве и во времени множество реакций и процессов.
С термодинамической точки зрения поддержание внутренней организации возможно благодаря постоянному поступлению в клетку энергии извне, часть которой выделяется в окружающее пространство в виде тепла. Тепловая энергия усиливает хаотичное движение молекул. Выделяя тепло, клетка тем самым компенсирует внутреннюю упорядоченность, повышая энтропию окружающей среды. Постоянная потеря тепла требует ввода в клетку энергии, отличной от тепловой. Растения используют для этой цели поглощенную световую энергию, а животные - энергию, выделяемую при окислении органических молекул.
Все реакции, протекающие в клетке, можно разделить на экзергонические и эндергонические. Первые идут с выделением энергии, которая может быть рассеяна в виде тепла в окружающую среду. Вторые требуют энергетических затрат и, как правило, способствуют созданию сложной организации и поддержанию внутреннего порядка.
Для интеграции метаболизма в единое целое вся поступающая в клетку энергия, будь то световая энергия или энергия субстратов дыхания, сначала преобразуется и запасается в форме универсальных энергетических и восстановительных эквивалентов. Универсальными, или конвертируемыми, формами клеточной энергии в растительной клетке является: трансмембранный градиент электрохимического потенциала ионов водорода, или электрохимический протонный градиент ΔμН+ и АТФ. Важнейшими восстановительными эквивалентами являются никотинамидадениндинуклеотид (НАДН) и никотинамидадениндинуклеотидфосфат (НАДФН). В фотосинтезе поглощение света сопровождается восстановлением НАДФН и синтезом АТФ в хлоропластах. В процессе дыхания, который имеет место в клетках растений и животных, восстановленный НАДН и АТФ образуются в митохондриях. В обоих случаях синтез АТФ опосредован образованием на тилакоидной или митохондриальной мембране электрохимического протонного градиента ΔμН+.
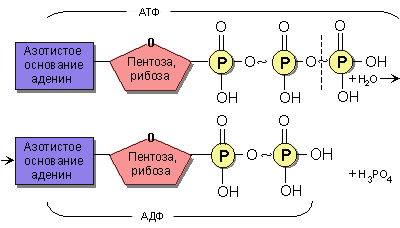
АТФ представляет собой универсальное макроэргическое соединение, реакция гидролиза которого сопряжена со множеством энергозависимых процессов. Сопряжение осуществляется через образование общего для двух реакций промежуточного продукта: отщепляемый от АТФ фосфат временно переносится на молекулу одного из реагирующих веществ. В результате такого фос-форилирования энергия молекулы повышается, и это дает возможность пройти энергетически невыгодной реакции. Помимо АТФ в клетке есть и другие соединения с макроэргической связью и высокими значениями свободной энергии гидролиза, однако, именно АТФ является наиболее общим и прямым источником энергии в клетке. В то же время следует заметить, что роль АТФ в метаболизме гораздо шире - это универсальный донор фосфатных групп в реакциях фосфорилирования, катализируемых ферментами киназами. Такие реакции важны не только для синтеза новых соединений, но и для регуляции ферментативной активности, а также играют важную роль в процессах, связанных с клеточной сигнализацией.
Расход АТФ на обеспечение энергозависимых реакций должен восполняться ее синтезом, который требует адекватных энергетических затрат. Каким же образом происходит синтез АТФ в клетке и каким образом используется для этого энергия внешних ресурсов?
Небольшая часть АТФ может быть образована при анаэробном разложении глюкозы в биохимических реакциях гликолиза. Основная же часть АТФ в клетках растений, животных и многих бактерий образуется в процессах фотосинтеза или дыхания. В основе трансформации энергии (будь то энергия света или субстратов дыхания) в энергию молекулы АТФ лежит общий и единый механизм, который получил название хемиосмотического сопряжения. Впервые хемиосмотическая теория была постулирована в 1960 г. английским биохимиком Питером Митчеллом. Однако идеи Митчелла были столь необычны, что стали общепризнанными лишь спустя некоторое время, когда получили неопровержимые экспериментальные подтверждения. Впоследствии П. Митчелл получил за свое открытие Нобелевскую премию (1978). Рассмотрим в общих чертах, в чем смысл хемиосмотического сопряжения и какие события лежат на пути преобразования энергии в клетке.
В системах трансформации энергии ключевая роль принадлежит замкнутой, сопрягающей мембране, непроницаемой для ионов. К сопрягающим относятся тилакоидная мембрана хлоропластов, внутренняя мембрана митохондрий и плазматические мембраны бактериальных клеток. Как правило, сопрягающая мембрана обогащена белком и биохимически отличается от других мембран клетки, так как содержит уникальный фосфолипид - кардиолипин, который делает мембрану более жидкой и более непроницаемой для ионов.
Энергопреобразующие мембраны содержат электрон-транспортные цепи (ЭТЦ). В процессах фотосинтеза и дыхания реализация энергии света или окисляемых субстратов в тилакоидной или митохондриальной мембране связана с возникновением электронного транспорта в ЭТЦ. Перенос электрона в фотосинтетической или дыхательной цепи неразрывно связан с векторной транслокацией иона Н+ через мембрану против сил электрического поля и в направлении большей концентрации. В фотосинтезе действие ЭТЦ сопряжено с накоплением протонов внутри тилакоидного пространства. Дыхательная цепь перекачивает протоны из матрикса в межмембранное пространство митохондрий. Процесс транслокации протона сопровождается энергизацией мембраны, т.е. возникновением на ней трансмембранной разности, или градиента электрохимического потенциала ионов водорода (ΔμН+) или протондвижущей силы Δρ. Генерируемый на мембране ΔμН+ представляет собой форму энергии, запасенную на мембране. Он используется для синтеза АТФ в процессах фотофосфорилирования и окислительного фосфорилирования. Синтез АТФ катализируется ферментом АТФ-синтазой, также локализованным в сопрягающих мембранах хлоропластов, митохондрий или бактерий.
Таким образом, система трансформации энергии включает следующие основные компоненты:
· замкнутая сопрягающая мембрана;
· локализованная в мембране ЭТЦ;
· трансмембранный электрохимический протонный градиент ΔμН+, генерируемый работой цепи;
· АТФ-синтаза, катализирующая синтез АТФ из АДФ иФн за счет энергии ΔμН+.
Так выглядит общая схема преобразования энергии на мембране.
АТФ-синтазы разного происхождения - из митохондрий, хлоропластов или бактериальных мембран - имеют в целом схожее строение, что говорит о несомненно древнем эволюционном происхождении фермента. На снимках, полученных при помощи электронной микроскопии, АТФ-синтазы выглядят как локализованные в мембранах грибовидные структуры. Хорошо видно, что фермент состоит из двух частей - двух белковых комплексов, которые обозначают как фактор F1 и фактор F0 (CF1 и СF0 - для АТФ-синтазы хлоропластов). Фактор, или комплекс, F1 расположен вне мембраны и на снимках представляет собой «шляпку» гриба высотой 8 нм и шириной 10 нм. Этот гидрофильный сферический комплекс представляет собой каталитический центр, на котором осуществляется синтез АТФ. Гидрофобный F0-фактор интегрально встроен в мембрану и формирует канал, по которому ионы Н+ могут пересекать мембрану, двигаясь по градиенту своего потенциала (рисунок).
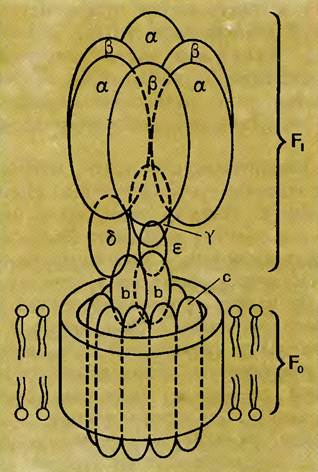
Комплекс F1 состоит из пяти разных субъединиц в определенном соотношении: αβγδε. Основу его структуры составляют гомологичные субъединицы α и β, чередующиеся друг с другом. Места связывания для нуклеотидов есть на обеих субъединицах, но три активных центра, где происходит синтез АТФ, расположены в основном на субъединицах β. Субъединицы α и β расположены поочередно вокруг γ-субъединицы, которая представляет собой стержень (9 нм) и, как втулка, проходит через каталитический центр, связывая факторы F1 и F0. Субъединица δ, расположенная на внешней стороне одной из δ-субъединиц, служит сайтом прикрепления двух b-субъединиц, которые заякоривают комплекс F1 в мембране. Функции ε-субъединицы связаны с регуляцией: ε-субъ-единица избирательно препятствует гидролизу АТФ. Фактор F1 легко диссоци-ирует от F0 и проявляет in vitro АТФазную активность, гидролизуя АТФ.
Комплекс F0 состоит из трех типов белковых субъединиц в следующем соотношении: a1b2c9-12. Он обеспечивает связывание F1 с мембраной и перенос протона. Небольшие, очень гидрофобные c-субъединицы, имеющие по два трансмембранных участка, формируют проводящий протоны канал, который обеспечивает прохождение H+ через всю мембрану. Интересно отметить, что такой сложный ферментный комплекс, как АТФ-синтаза, находится под двойным генетическим контролем: три субъединицы F0-фактора и α-субъединицы фактора F1 кодируются геномом митохондрий или хлоропластов, тогда как синтез остальных субъединиц контролируется ядерными генами.
Организация ЭТЦ в мембране. Электрон-транспортные цепи фотосинтеза и дыхания организованы в мембране сложным образом и представляют собой встроенные в нее суперкомплексы, состоящие из многих субъединиц белка. В их составе обязательно присутствуют трансмембранные белки, закрепляющие весь комплекс в мембране. Каждый суперкомплекс содержит, как правило, несколько активных центров: на белках в качестве простетических групп или за счет нековалентных взаимодействий удерживаются соединения, которые участвуют в переносе электрона. Некоторые комплексы из тилакоидных и митохондриальных мембран удалось выделить с помощью детергентов и получить в кристаллизованном состоянии.
Это позволило изучить их молекулярную организацию методом рентгеноструктурного анализа. Связь между комплексами осуществляют подвижные переносчики, которые могут перемещаться либо в липидной фазе мембраны (хиноны), либо в водной фазе вблизи мембраны. Реакции в ЭТЦ идут с большими скоростями, измеряемыми в интервалах 10-4 – 10-9с.
Организация электронного транспорта такова, что перенос электрона по цепи неразрывно связан с направленной транслокацией ионов Н+ через мембрану и генерацией ΔμH+. В тилакоидной мембране протоны переносятся внутрь тилакоидного пространства, а в митохондриях - из матрикса в межмембранное пространство. Механизмы транслокации Н+ через мембрану могут быть разными и в ряде случаев пока остаются неясными. Общим случаем является перенос протона через мембрану при участии подвижных переносчиков - хинонов.
Если в процессе электронного транспорта на мембране возникает ΔμH+, который используется на синтез АТФ, то транспорт называется сопряженным. Однако могут быть ситуации, когда работа цепи не сопряжена с генерацией ΔμH+ и синтезом АТФ. Тогда электронный транспорт называется разобщенным. Разобщение электронного транспорта с фосфорилированием имеет место in vitro, при этом энергия электронного потока преобразуется (диссипирует) в тепло. Разобщение имеет место в митохондриях животных и растений и представляет особый механизм регуляции метаболизма.
Некоторые переносчики электронов являются общими для ЭТЦ всех типов. Никотинамидадениндинуклеотид (НАД(Н)) и никотинамидадениндинук-леотидфосфат (НАДФ(Н)) - это близкие по структуре растворимые соединения, функциональной частью которых является ароматическое кольцо. НАД(Н) и НАДФ(Н) являются коферментами НАД (Ф)-зависимых дегидрогеназ. Эти ферменты катализируют реакции, связанные с отнятием или присоединением двух атомов водорода, при этом коферменты переносят гидрид-ион, а недостающий протон захватывается или отдается в водную фазу:
AH2 + НАД(Ф)+ ↔ А + НАД(Ф)Н + Н+
Большая часть НАД(Н) и НАДФ(Н) растворена в водной фазе, так как их связи с ферментными белками непрочные и возникают только в момент ферментативной реакции. Окисленные формы НАД+ и НАДФ+ имеют полосу поглощения при 260 нм, а при их восстановлении появляется полоса поглощения при 340 нм. Это позволяет регистрировать редокс-состояние коферментов в ходе реакций. Стандартный Е° этих соединений равен -0,32 В. Роль НАД(Н) и НАДФ(Н) в клетке очень велика. Принимая участие во многих реакциях в качестве доноров или акцепторов электронов, они обеспечивают взаимодействие разных процессов и в целом контролируют редокс-статус клетки.
Флавопротеиды. Компонентами ЭТЦ являются флавопротеиды - белки, содержащие в качестве прочно связанной простетической группы флавинмо-нонуклеотид (ФМН) и флавинадениндинуклеотид (ФАД). Функциональная часть этих соединений представлена системой ароматических колец, в состав которых входит остаток рибофлавина (витамина В2). Окисление – восстановление флавопротеидов связано с переносом двух атомов водорода. Окисленные формы флавинов имеют два максимума поглощения - при 375 и 450 нм, которые исчезают при восстановлении. Редокс-потенциалы флавопротеидов варьируют в широких пределах (от -0,49 до +0,19 В) в зависимости от структуры апобелка.


ФМН ФАД
Цитохромы. Обязательными компонентами ЭТЦ являются цитохромы - железосодержащие белки, в составе которых присутствует гем. Основой структуры гема является порфириновое кольцо, образованное из четырех пиррольных колец, в центре которого расположен атом железа. В редокс-превраще-ниях цитохромы функционируют как одноэлектронные переносчики, при этом железо меняет свою валентность, переходя из состояния Fe2+ в состояние Fe3+. Восстановленные формы цитохромов имеют три характерных полосы поглощения в областях 545-600, 520-535, 415-445 нм.
Железосерные белки. Железосерные белки, или Fe-S-белки, содержат так называемые Fe-S-кластеры, или центры. Центры состоят из двух или четырех атомов железа, комплексно связанных с атомами неорганической серы или серы в остатках цистеина в структуре белка. В основе классификации железо-серных белков лежит структура кластера; в зависимости от этого различают 2Fe-2S- или 4Fe-4S-белки.
В состав центра входят несколько атомов железа, но каждый из центров способен принимать или отдавать только один электрон. Восстановление железосерных белков сопровождается исчезновением в спектре полосы 450 нм и появлением сигнала ЭПР (метод электронного парамагнитного резонанса), что указывает на появление свободного радикала. Для этой группы соединений диапазон значений Е° также достаточно широк: от -0,42 В до +0,35 В.
Хиноны. В качестве подвижных переносчиков, действующих в липидной фазе мембраны, функционируют хиноны, обозначаемые буквой Q (от англ. quinon), пластохинон в ЭТЦ фотосинтеза и убихинон в ЭТЦ дыхания. Хиноны состоят из ароматического кольца и боковой липофильной цепи, в составе которой может содержаться 9 (пластохинон) или 10 (убихинон) изопреноидных остатков. Свободно диффундирующие в мембране хиноны осуществляют связь между белковыми комплексами и могут переносить два атома водорода. Хиноны обладают двумя свойствами, исключительно важными для работы ЭТЦ по переносу протонов через мембрану. Во-первых, в ходе редокс-реакций хиноны могут захватывать или освобождать 2Н+ на границе раздела двух фаз - липид/вода с любой стороны мембраны. Во-вторых, в ходе электронного транспорта хиноны могут принимать или отдавать только один электрон, при этом находясь в течение какого-то времени в форме свободного анион-радикала - семихинона (Q·). Спектры поглощения хинонов находятся в УФ-области и маскируются поглощением других соединений, поэтому их окислительно-восстановительные состояния отслеживают, как правило, методом ЭПР. Редокс-потенциалы хинонов близки к нулю или имеют низкие положительные значения.
Итак, живые организмы используют энергию света и химическую энергию органических соединений в процессах фотосинтеза и дыхания. И в том и другом случае клетка превращает внешние энергетические ресурсы в конвертируемые формы клеточной энергии - АТФ и трансмембранный электрохимический протонный градиент. Преобразование энергии в процессах фотосинтеза и дыхания основано на общем механизме хемиосмотического сопряжения. Oбщим принципом клеточной биоэнергетики является взаимопревращение на мембранах двух форм клеточной энергии - энергии ионных градиентов и АТФ. Благодаря этим превращениям клетка обеспечивает энергией разнообразные процессы, протекающие как в растворе, так и на мембранах.
 2014-02-10
2014-02-10 3330
3330