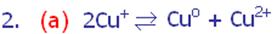1. Определение. Это тип окислительно-восстановительных реакций, при которых соединение с промежуточной степенью окисления превращается в два другие: одно – с более низкой, а другое – с более высокой степенью окисления.
|
Ka = 2 × 10 36
а) влево за счет образования малорастворимых солей Cu X или комплексных соединений [Cu X2 ]- (X=Cl,Br,CN)
б) вправо- за счет образования комплексных соединений Cu2+ с Н2О, этилендиамином H2N–CH=CН–NH2.
4. Важны для понимания природы катализа (реакции окисления оксидазы в организме человека), механизма высокотемпературной проводимости.
§ 6. Свойства Сu(I)
1.Получение:CuCl2 + Cu 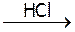 2CuCl (бесцв.) ® H[CuCl2]
2CuCl (бесцв.) ® H[CuCl2]
H[CuCl2] 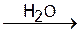 CuCl¯
CuCl¯
 2014-02-09
2014-02-09 292
292