Наиболее типичны для алкенов реакции присоединения (А) по схеме:

π-Связь легко поляризуется. Её атакуют электрофилы и радикалы (нуклеофилы - редко).
1. Реакции электрофильного присоединения (АЕ).
а) Наиболее часто используются реакции присоединения воды и галогеноводородов. В первом случае продуктами реакции являются спирты, во втором – галогенопроизводные.
Реакция проходит в сильно кислой среде, ион Н+ является атакующим электрофилом.
Механизм реакции:
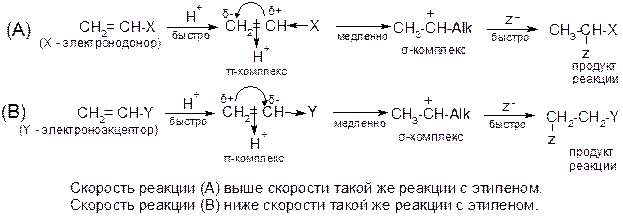
Правило Марковникова:
При присоединении воды или галогеноводорода к алкенам водород присоединяется к наиболее гидрогенизированному атому углерода.
Правило Марковникова соблюдается для углеводородов и для тех производных, которые имеют у двойной связи электронодонорный заместитель. Например:
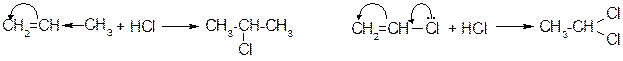
Для соединений, имеющих у двойной связи электроноакцепторный заместитель, реакция идет против правила Марковникова.
Например:

б) присоединение серной кислоты
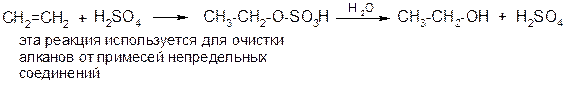
в) присоединение галогенов.
Реакция с фтором из-за слишком большой его активности проходит с разрывом С-С-связей и разрушением цепи. Лучше всего присоединяются хлор и бром. Реакция с иодом идет медленно и равновесно.

г) присоединение хлорноватистой кислоты.

Сравнительная реакционная способность алкенов в реакциях АЕ:
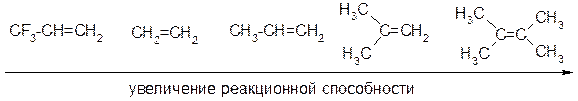
2. Реакции радикального присоединения (АR).
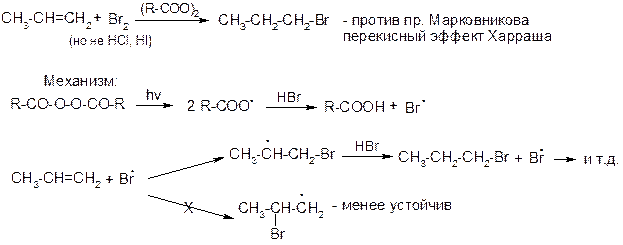
3. Реакции аллильного замещения
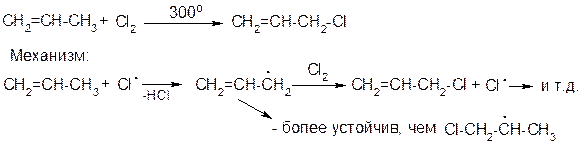
4. Окисление
а) эпоксидирование
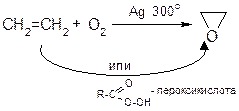
б) гидроксилирование (реакция Вагнера)

в) озонолиз
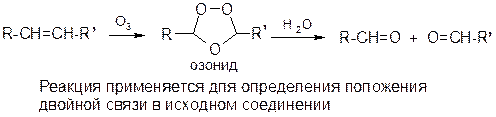
г) жесткое окисление
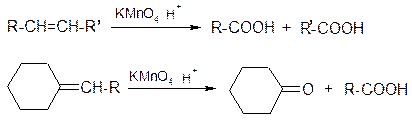
5. Восстановление
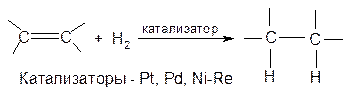
Отдельные представители алкенов – см. учебник.
 2014-02-12
2014-02-12 705
705








