Пример 10.1. Золь иодида серебра получен при добавлении к раствору AgNO3 избытка KI. Определить заряд частиц полученного золя и написать формулу его мицеллы.
Решение. При смешивании растворов AgNO3 и KI протекает реакция
AgNO3 + KI (изб.) = AgI + KNO3.
Ядро коллоидной частицы золя иодида серебра состоит из агрегата молекул (mAgI) и зарядообразующих ионов I‾, которые находятся в растворе в избытке и обеспечивают коллоидным частицам отрицательный заряд. Противоионами являются гидратированные ионы калия. Формула мицеллы иодида серебра имеет вид {[(m AgI)· n I‾·(n-x)К+· y H2O] x − + x К+? z H2O}0.
Пример 10.2. Золь кремневой кислоты был получен при взаимодействии растворов K2SiO3 и HCl. Написать формулу мицеллы золя и определить, какой из электролитов был взят в избытке, если противоионы в электрическом поле движутся к катоду.
Решение. Образование золя кремневой кислоты происходит по реакции
K2SiO3 + 2HCl = H2SiO3 + 2KCl.
Чтобы двигаться к катоду (отрицательному электроду) противоионы должны иметь положительный заряд, а коллоидные частицы золя должны быть заряжены отрицательно. На электронейтральном агрегате частиц (mH2SiO3) адсорбируются ионы элемента, входящего в состав ядра.
Таковыми являются ионы HSiO3‾, которые образуются в результате гидролиза соли K2SiO3:
K2SiO3 + H2O 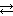 KHSiO3 + KOH или в ионной форме
KHSiO3 + KOH или в ионной форме
SiO32− + H2O 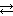 HSiO3‾ + OH‾.
HSiO3‾ + OH‾.
Ионы HSiO3‾, адсорбируясь на поверхности частиц золя кремниевой кислоты, сообщают им отрицательный заряд. Противоионами являются гидратированные ионы водорода H+.
Формула мицеллы золя кремневой кислоты:
{[(m H2SiO3) · n HSiO3‾·(n-x)H+? y H2O] x − + x H+? z H2O}.
Так как коллоидные частицы золя кремневой кислоты заряжены отрицательно за счет ионов HSiO3‾, то, следовательно, в избытке был взят K2SiO3.
Пример 10.3. Какого из веществ, K2SO4 или KCl, потребуется меньше, чтобы вызвать коагуляцию коллоидного раствора гидроксида железа (II), полученного по реакции FeCl2 + 2NaOH = Fe(OH)2 + 2NaCl?
Решение. Из формулы коллоидной частицы золя гидроксида железа (II) [(m Fe(OH)2· n Fe2+ 2(n-x)Cl‾?yH2O]2 x + видно, что частицы золя имеют положительный заряд. Коагуляцию золя вызывает тот из ионов прибавленного электролита, заряд которого противоположен заряду коллоидной частицы. В данной задаче – это ионы SO42− и Cl‾. Коагулирующая способность иона определяется его зарядом – чем больше заряд иона, тем больше его коагулирующая способность. Заряд иона SO42− больше заряда иона Cl‾, поэтому, чтобы вызвать коагуляцию коллоидного раствора гидроксида железа (II), раствора K2SO4 потребуется меньше, чем раствора KCl.
Пример 10.4. Составить схему строения мицеллы золя гидроксида меди (II) в растворе хлорида меди.
Решение. В состав мицеллы гидроксида меди входят: агрегат молекул (mCu(OH)2), адсорбированный слой, состоящий из зарядообразующих ионов меди Cu2+ и гидратированных противоионов хлора, и диффузный слой гидратированных противоионов хлора. Схема строения мицеллы гидроксида меди {[(m Cu(OH)2·nCu2+ 2(n-x)Cl‾? y H2O]2 x + + 2 x Cl‾? z H2O}.
 2014-09-04
2014-09-04 28846
28846
