2.
Активность человека невозможно понять, не выяснив источники, побудительные силы, мотивы этого явления.
Активность личности достигает высшей эффективности, когда она оптимально организована и целенаправленна, что обеспечивается принципом доминанты, иерархией мотивов активности личности.
Е.П. Ильин считает, что мотивацией не следует считать любое побуждение, любую детерминацию, он полагает, что при этом нужно отсечь побуждения, связанные с безусловно - и условно-рефлекторным реагированием на внешние стимулы.
Активность человека, по его мнению, следует связывать лишь с волей (участвует она в инициации активности или нет, противоречит активность воле субъекта или не противоречит). Не случайно мотив и волю часто понимают как синонимы.
Таким образом, можно сказать, что мотивом следует считать такую причинную обусловленность поведения, которая связана с внутренними побуждениями человека.
Вместе с тем до настоящего времени существует терминологическая неясность в определении мотивации и мотива. Эти термины порой используются как синонимы.
Так, А.Б. Орлов (1989) под мотивацией понимает процессы детерминации активности человека и животных или формирование побуждений к действию или деятельности.
В.А. Иванников (1985, 1991) мотивацию связывает с потребностями и мотивами, мировоззрениями человека и особенностями его представлений о себе, личностными особенностями и функциональными состояниями, с переживаниями, знаниями о среде и прогнозом ее изменения, с ожидаемыми последствиями и оценками других людей.
Леонтьев писал, что работы по проблеме мотивации почти не поддаются систематизации.
В зарубежной психологии имеется около 50 терминов мотивации. В связи с таким положением В.К. Вилюнас (1990) высказывает сомнение в целесообразности обсуждения вопроса что такое «мотив». Вместо этого он предлагает сосредоточить внимание на более отчетливом обозначении и описании отдельных феноменов, принимаемых в качестве побудителей активности.
По мнению В.А. Иванникова (1985), термин «мотив» нужно закрепить за устойчивыми образованиями мотивационной сферы в виде определенных потребностей, а для обозначения ситуаций, инициирующих деятельность, использовать термин «побуждение».
В ряде работ мотив рассматривается только как интеллектуальный продукт.
Так, Ж. Годфруа (1994) пишет, что мотив — это соображение, по которому субъект должен действовать. По X. Хекхаузену (1985), мотив — это лишь «конструкт мышления», теоретическое построение, а не реально существующий психологический феномен. За мотив он принимает либо:
1) потребность (потребность во властвовании, называемая им «мотивом власти», потребность в достижении — «мотив достижения»; либо
2) личностные диспозиции (тревожность и др.; либо
3) внешние и внутренние причины того или иного поведения (оказание помощи, проявление агрессии).
А.Н. Леонтьев писал в 1956 г., что мотив побуждает отдельное, частное действие, в более поздних работах он утверждал, что термин относится только к деятельности. Это утверждение можно считать правомерным, так как каждое действие в составе какой-то деятельности не имеет собственного мотива, хотя это не значит, что эти действия немотивированны. Однако цели деятельности и каждого действия в ней не совпадают.
Согласно же представлениям Р.А. Пилояна (1984), мотив, наоборот, относится к действиям, деятельность же он рассматривает в контексте понятия «мотивация». В этом он солидарен с М.Ш. Магомед-Эминовым (1987), который связывает мотивацию не только с подготовкой детальности, но и ее осуществлением.
Таким образом, проблема мотивации и мотивов остается остродискуссионной, трудноизучаемой экспериментально, а так как мотивационная сфера является ядром личности, то изучение мотивации человеческого поведения становится насущной задачей науки. Тем более без понимания того, чем же мотивировано поведение потребителя в каждом конкретном случае обращения в сервисные службы, деятельность профессионала в сфере продаж вряд ли будет достаточно успешной и целенаправленной.
В «Словаре русского языка» СИ. Ожегова говорится, что цель — это то, к чему стремятся, то, что надо осуществить, т.е. целью могут быть предмет, объект, действия.
С.Л. Рубинштейн предмет удовлетворения потребности тоже рассматривает как цель, он говорит, что предметы становятся объектами желаний — возможными целями субъекта, когда он включает их в практическое осознание своего отношения к потребности.
Леонтьев и его последователи отделяют мотив от цели, принимая в качестве последней только действие по удовлетворению потребности или вообще не уточняя ее. Мотив у него — это то объектное, в чем потребность концентрируется в данных условиях и на что направлена деятельность. Воспринимаемый (мыслимый) предмет, приобретая свою побудительную функцию, становится мотивом. «Опредмечивание потребности» придает побуждению смысл, побудителем деятельности выступает не сам предмет, а его значение для субъекта. Он приписывает мотиву смыслообразующую функцию, когда побуждает к действию не желание чем-либо завладеть, а интерес к нему, получение от него удовольствия (например, творческая деятельность — снятие психологического напряжения личности, а значит, получение удовольствия).
Манукян поддерживает Леонтьева и считает ошибочной точку зрения философов-материалистов Древней Греции — Аристотеля, Лукренция Кара (в наше время — Л.И. Божович и др.), что нужда заставляет человека создавать предметы удовлетворения потребностей. По мнению Манукяна, потребности с конкретным предметным содержанием порождают определенные предметы и явления. Он полагает, что не потребность вызывает деятельность, а предмет потребности или его образ. Так, он считает, что биологические потребности вначале выступают как психологическое состояние напряжения, при котором человек не знает, чего ему хочется, и лишь встречаясь с объектом, могущим снять напряжение, человек начинает действовать, стремясь к этому объекту. При этом автор оказывается на позиции бихевиоризма, который рассматривает детерминацию поведения по типу стимул-реакция (S-R), когда потребность как бы совсем и не нужна.
Более справедливо высказывание И.М. Соченова: «...жизненные потребности родят хотения, и уже эти ведут за собой действия, хотения будут тогда мотивом или целью, а движения — действием или средством достижения цели... Без хотения как мотива или импульса движение было бы вообще бессмысленно» (1952). Предметы могут обладать силой привлекательности, но это, скорее, характеристика стимула, а не мотива. В связи с представлением о мотиве как о предмете говорят, о роли мотива в формировании потребностей, а не о роли потребностей в формировании мотива, т.е. процесс мотивации ставится с ног на голову.
Еще с прошлого века так трактовался мотив многими психологами, поэтому говорить о «побудительных» мотивах — все равно, что сказать «масло масляное»: мотив всегда побуждает что-либо делать или не делать. Следует обратить внимание на то, что не строгость в терминах привела к тому, что мотив стал пониматься как любая причина, вызывающая побуждение, т.е. мотивами стали стимулы, а «побудитель» и «побуждение» стали синонимами.
Биологи, физиологи и психологи-бихевиористы за мотив в основном принимали внешний стимул. Олпорт справедливо отмечает, что в качестве объектов, побуждающих деятельность человека, могут выступать и отсутствующие (представляемые) объекты. То есть побудителей поведения может быть много, но не все они могут быть отнесены к мотивам. При этом возникает вопрос, что может служить критерием различения мотивационных и немотивационных детерминант.
В западной психологии решением этого вопроса является различение способа (как) и причины (почему) поведения: к мотивации относят только причины. При этом считается, что мотивация отвечает за стратегическую направленность поведения на цель, а способ поведения, его тактическая реализация определяется не причиной, а опытом, научением. Вместе с тем, как отмечал В.К. Вилюнас (1990), отдельные механизмы мотивации отвечают именно за способ поведения, т.е. за то, как делается. С.Л. Рубинштейн писал: «Мотивация — через психику реализующаяся детерминация. Большинство отечественных и зарубежных психологов считают, что мотив — это не любое возникшее в организме человека побуждение (понимаемое как состояние), а внутреннее осознанное побуждение, отражающее готовность человека к действию или поступку. Таким образом, стимул вызывает (побуждает) действие или поступок — внутреннее осознанное побуждение, принимаемое многими психологами в качестве мотива. В то же время ряд психологов (в частности А.А. Файзуллаев, 1985,1987, 1989) не сводят мотив к побуждению и даже, более того, отделяют мотив от побуждения.
Ограниченность этих схем очевидна, так как если оторвать побуждение от мотива, то он теряет побудительную силу. Но в то же время свести мотив только к побуждению также нет достаточных оснований.
Во-первых, побудительностью обладает и потребность, причем побуждения можно рассматривать как состояние внутреннего (потребностного) напряжения — состояние, одинаковое для разных мотивов.
Во-вторых, побуждение не раскрывает содержательную сторону мотива, не объясняет причину и смысл проявляемой человеком активности (если, конечно, не принимать, как В.И. Ковалев, за побуждение сам мотив). Например, побуждение к занятиям спортом может быть сначала обусловлено необходимостью укрепления здоровья, затем получением удовольствия от процесса, потом — стремлением достигнуть высот в спорте (так и стремление к отдыху может быть обусловлено желанием, потребностью в сохранении и укреплении здоровья, с одной стороны, а с другой — приобретением новых знакомств, занятием любимыми увлечениями, т.е. получением удовольствия от общения, от реализации своих интересов, устремлений).
Таким образом, само побуждение не может дать ответа на вопросы — почему, для чего, из-за чего.
В-третьих, мешает принятию побуждения за мотив и то, что у человека имеются поступки, связанные с обоснованным (мотивированным) отказом что-либо делать, т.е. в соответствии с мотивом можно не только действовать, но и бездействовать. Такие мотивы называются отрицательными.
Признавая в большинстве случаев за мотивом побудительную силу, психологи различаются во взглядах на истоки побудительности.
Одни считают, что побуждение берется от потребности, другие — от предмета ее удовлетворения. Кроме того, сама роль побуждения рассматривается по-разному. У одних — это побуждение к действию, у других — то, что побуждает к постановке целей. В ряде случаев побуждение подменяется его причинами: идеалами, ценностными ориентациями, потребностями, целями, интересами.
Существуют также следующие точки зрения на мотив.
· Мотив как намерение (К. Левин, Л.И. Божович и др.). Отмечается, что намерения возникают на базе потребностей, которые не могут быть удовлетворены прямо, а требуют ряда промежуточных действий, не имеющих собственной побудительной силы, или же когда цель деятельности отдалена, ее достижение отсрочено. При этом намерение является результатом влияния потребности, с одной стороны, и интеллектуальной активности — с другой. Таким образом, признание за намерением побудительной силы указывает на его связь с мотивацией и мотивом.
Но намерение не раскрывает первопричину поступка или действия, а в ряде случаев, когда цель, выбираемая человеком, отдалена по времени, не содержит и побуждения.
· Мотив как устойчивые личностные проявления (М. Мадсен, 1959; Дж. Аткинсон, 1964; К.К. Платонов, B.C. Мерлин, М.Ш. Магомед-Эминов). Однако принятие свойств личности за мотив тоже не решает проблемы, так как многие личностные свойства скорее являются потребностями, например, стремление к деятельности, к наслаждению, к новым впечатлениям, к самосохранению, самоуважению, знаниям, творчеству.
· Мотив как состояние (Философский энциклопедический словарь — 1983; Р.А. Пилоян, 1984; Дж. Гилфорд, 1956). Е.Р. Хилгард (1957) прямо пишет, что мотивом является любое состояние организма, которое имеет влияние на начало или продолжение определенного поведения.
Е.П. Ильин считает, что свести мотив к состоянию также неправомерно, как принять за мотив нужду.
· Мотив как формулировка (К. Обуховский, 1972). Он считает, что мотив — это формулировка цели и средств. Он сужает понятие мотива, не включая в него побудительные факторы, связанные с состоянием напряжения, возникающим при потребностях.
В случае биологических потребностей личности этапы формирования мотива следующие:
I -й этап — формирование первичного (абстрактного) мотива.
Этот этап состоит из формирования потребности и побуждения к поисковой активности. Для того чтобы нужда превратилась в потребность личности, надо, чтобы человек сделал значимой для себя ее ликвидацию.
2-й этап — поисковая активность.
При этом:
а) нужда должна быть осознанна (т.е. чтобы появилось чувство голода, жажды и т.п.);
б) чтобы это чувство по интенсивности достигло порога, за которым начинается беспокойство, т.е. чувство переживается как неприятное;
в) переживание порождает состояние напряжения и аффективное стремление избавиться от него, восстановить равновесие.
Причем вначале у человека появляется лишь обобщенный образ удовлетворения потребности, т.е. абстрактная цель, без ее конкретизации (хочу пить, есть, не задумываясь, что конкретно хочу пить или есть).
Поисковая активность может быть внешней или внутренней.
· Внешняя осуществляется человеком, если он попадает в незнакомую обстановку, не обладает необходимой для принятия решения информацией и должен заняться поиском во внешней среде реального объекта, который мог бы удовлетворить имеющуюся потребность.
· Внутренняя поисковая активность связана с мысленным анализом и выбором конкретных предметов удовлетворения потребностей. Аристотель писал: «Движет то, чего хочется, и благодаря этому приводит в движение рассудок, так как желаемое представляет исходную точку для практического ума». С.Л. Рубинштейн писал, что мотив формируется по мере того, как человек учитывает, оценивает, взвешивает обстоятельства, в которых он находится, и осознает цель; из отношения к ним и рождается мотив в его конкретной содержательности, необходимой для реального действия.
Задачи второго этапа мотивационного процесса в случае удовлетворения личностных потребностей:
1) определение субъективной вероятности достижения успеха при различных способах поведения и деятельности;
2) предвидение (прогнозирование) последствий выбираемого для достижения цели пути.
При этом могут учитываться реакции других людей на ваши действия, нравственные критерии поступков. В мотивации может быть несколько причин, побуждений, поэтому ее правильнее рассматривать как совокупность и последовательность ряда причин.
3-й этап — выбор конкретной цели и формирование намерений. В случае, когда конкретная цель не поставлена, мотивы называют недейственными (А.Н. Леонтьев). Ильин с этим не согласен, по его мнению, первичный мотив действенен потому, что вызывает у человека поисковую активность.
Безусловно, первопричиной деятельности человека, его поступков являются потребности (правда, люди не всегда это понимают). Но вместе с тем нельзя отрицать и роль мышления в активности человека, ведь именно она, по существу, определяет, будет удовлетворяться потребность или нет, т.е. роль потребности велика в придании энергии мотиву, в осознании нужды, но в направлении энергии по определенному руслу большее значение имеют мышление и воля человека. То есть третья стадия формирования мотива — выбор конкретной цели и формирование намерения ее достичь.
После рассмотрения различных вариантов удовлетворения потребности человек должен на чем-то остановиться, выбрать конкретную цель и способ ее достижения.
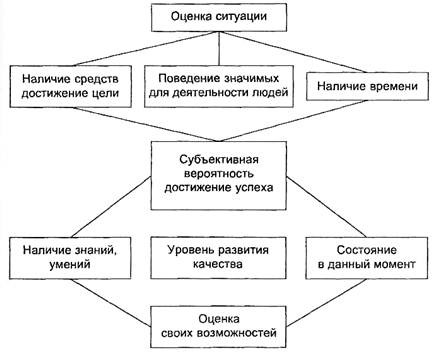
Рис. 1. Факторы, учитываемые субъектом при определении вероятности достижения успеха
О цели говорят как о структурном психологическом образовании (Ф. Хоппе), как об осознанном образе будущих результатов (O.K. Тихомиров, 1977), как о сложном многокомпонентном образе того, что человек хочет достичь. Цель характеризуется не только содержанием (чего хочу), но и уровнем качества (какой результат нужен — высокий, низкий). Поэтому ее выбор определяется имеющимся у человека уровнем притязаний. Субъективная трудность достижения цели определяет степень мобилизации человека, его старания, терпеливость, настойчивость. Уровень притязаний определяется имеющейся у человека установкой (потребностью в достижении успеха или избегания неудач). При этом важно учитывать тип решимости человека. У. Джемс выделяет:
· 1-й тип, связанный со страхом и печалью, парализующими легкомысленные фантазии и побуждающими к серьезным поступкам;
· 2-й тип, когда у человека нет разумного основания к действию, и оно побуждается усилием воли.
Лица с первым типом правильнее оценивают свои возможности, обладают адекватным уровнем притязания. Люди второго типа имеют завышенную или заниженную самооценку, обладают неадекватным, завышенным или заниженным уровнем притязаний.
Таким образом, на третьей стадии формирования мотива возникает намерение достичь цели, побуждения воли, выражающееся в сознательном, преднамеренном побуждении к действию. С формированием этого побуждение заканчивается формирование конкретного мотива. То есть побуждение - лишь часть мотива.
Мотив — это системное образование, а побуждение — это его энергетическая сторона, состояние готовности начать действия. Дж. Роттер (1954) обозначает его как потенцию действия, а Л. Фестингер (1957) как мотивационное давление. В мотиве происходит сознательное отражение будущего на основании использования опыта прошлого.
Однако намерение и побуждение — не одно и то же. Намерение — это замысел, предположение сделать что-нибудь. Намерение может быть и без побуждения, например, когда человек намерен что-то не делать, или же при наличии намерения у человека может не хватить решимости осуществить задуманное, т.е. он не сможет проявить силу воли.
Итак, мы изучили взгляды ученых на мотивированность поведения человека в реализации его потребностей. Далее рассмотрим существующие подходы к классификации потребностей.
Вопросы и задания для самопроверки:
1. Охарактеризуйте различия понятий: индивид, личность, индивидуальность.
2. Раскройте общие характеристики индивида.
3. Осветите понятие роли и ее разновидностей.
4. Охарактеризуйте понятие личности как социального субъекта.
5. Охарактеризуйте взгляд на современного человека с позиции рыночной типологии. Проведите сравнительную характеристику позитивных и негативных сторон личности.
6. Охарактеризуйте различия понятий «потребность» и «мотив».
7. Дайте характеристику мотиву как намерению, как состоянию, как устойчивому личностному проявлению.
8. Разноплановость в толковании мотива у В.А.Иванникова, А.Б.Орлова, А.Н.Леонтьева.
9. Охарактеризуйте факторы, учитываемые субъектом при достижении успеха.
Раство́р – гомогенная (однородная) смесь, состоящая из частиц растворённого вещества, растворителя и продуктов их взаимодействия. "Гомогенный" – значит, каждый из компонентов распределён в массе другого в виде своих частиц, то есть атомов, молекул или ионов.
Раствор – однофазная система переменного, или гетерогенного, состава, состоящая из двух или более компонентов.
Растворитель – компонент, агрегатное состояние которого не изменяется при образовании раствора. В случае же растворов, образующихся при смешении газа с газом, жидкости с жидкостью, твёрдого вещества с твёрдым, растворителем считается компонент, количество которого в растворе преобладает.
Образование того или иного типа раствора обусловливается интенсивностью межмолекулярного, межатомного, межионного или другого вида взаимодействия, то есть, теми же силами, которые определяют возникновение того или иного агрегатного состояния. Отличия: образование раствора зависит от характера и интенсивности взаимодействия частиц разных веществ.
По сравнению с индивидуальными веществами по структуре растворы сложнее.
Растворы бывают газовыми, жидкими и твёрдыми.
Чаще под раствором подразумевается жидкое вещество, например раствор соли или спирта в воде (или даже раствор золота в ртути — амальгама).
Существуют также растворы газов в жидкостях, газов в газах и жидкостей в жидкостях, в последнем случае растворителем считается вода, или же компонент, которого больше.
В химической практике обычно под растворами понимают гомогенные системы, растворитель может быть жидким, твёрдым (твёрдый раствор), газообразным. Однако нередко допускается и микрогетерогенность – золи.
«Раствором» именуют и смесь цемента с водой, песком и так далее. Хотя это и не является раствором в химическом смысле этого слова.
Коллоидные и истинные растворы (изучением коллоидных систем занимается коллоидная химия) отличаются главным образом размерами частиц.
В истинных растворах размер частиц менее 1·10−9 м, частицы в таких растворах невозможно обнаружить оптическими методами; в то время как в коллоидных растворах размер частиц 1·10−9 м – 10·10−7 м, частицы в таких растворах можно обнаружить при помощи ультрамикроскопа.
Растворение – переход молекул вещества из одной фазы в другую (раствор, растворенное состояние). Происходит в результате взаимодействия атомов (молекул) растворителя и растворённого вещества и сопровождается увеличением энтропии при растворении твёрдых веществ и её уменьшением при растворении газов. При растворении межфазная граница исчезает, при этом многие физические свойства раствора (например, плотность, вязкость, иногда цвет, и другие) меняются.
В случае химического взаимодействия растворителя и растворённого вещества сильно меняются и химические свойства – например, при растворении газа хлороводорода в воде образуется жидкая соляная кислота.
Электролиты – вещества, проводящие в расплавах или водных растворах электрический ток. В расплавах или водных растворах они диссоциируют на ионы. Электролиты при растворении в подходящих растворителях (вода, другие полярные растворители) диссоциируют на ионы. Сильное физико-химическое взаимодействие при растворении приводит к сильному изменению свойств раствора (химическая теория растворов).
Неэлектролиты – вещества, водные растворы и расплавы которых не проводят электрический ток, так как их молекулы не диссоциируют на ионы. Вещества, которые в тех же условиях на ионы не распадаются и электрический ток не проводят, называются неэлектролитами.
К электролитам относятся кислоты, основания и почти все соли, к неэлектролитам – большинство органических соединений, а также вещества, в молекулах которых имеются только ковалентные неполярные или малополярные связи.
Растворы высокомолекулярных веществ ВМС – белков, углеводов и др. обладают одновременно многими свойствами истинных и коллоидных растворов.
В зависимости от цели для описания концентрации растворов используются разные физические величины.
Насыщенный раствор – раствор, в котором растворённое вещество при данных условиях достигло максимальной концентрации и больше не растворяется. Осадок данного вещества находится в равновесном состоянии с веществом в растворе.
Ненасыщенный раствор – раствор, в котором концентрация растворенного вещества меньше, чем в насыщенном растворе, и в котором при данных условиях можно растворить еще некоторое его количество.
Пересыщенный раствор – раствор, содержащий при данных условиях больше растворённого вещества, чем в насыщенном растворе, избыток вещества легко выпадает в осадок. Обычно пересыщенный раствор получают охлаждением раствора, насыщенного при более высокой температуре (пересыщение).
Концентрированный раствор – раствор с высоким содержанием растворённого вещества в противоположность разбавленному раствору, содержащему малое количество растворённого вещества. Деление растворов на концентрированные и разбавленные не связано с делением на насыщенные и ненасыщенные. Так насыщенный 0,0000134М раствор хлорида серебра является очень разбавленным, а 4М раствор бромида калия, будучи очень концентрированным, не является насыщенным.
Разбавленный раствор – раствор с низким содержанием растворённого вещества. Отметим, что не всегда разбавленный раствор является ненасыщенным – например, насыщенный 0,0000134М раствор практически нерастворимого хлорида серебра является очень разбавленным. Граница между разбавленным и концентрированным растворами весьма условна.
РАСТВОРЫ – однофазные системы, состоящие из двух или более компонентов. По своему агрегатному состоянию растворы могут быть твердыми, жидкими или газообразными. Так, воздух – это газообразный раствор, гомогенная смесь газов; водка – жидкий раствор, смесь нескольких веществ, образующих одну жидкую фазу; морская вода – жидкий раствор, смесь твердого (соль) и жидкого (вода) веществ, образующих одну жидкую фазу; латунь – твердый раствор, смесь двух твердых веществ (меди и цинка), образующих одну твердую фазу. Смесь бензина и воды не является раствором, поскольку эти жидкости не растворяются друг в друге, оставаясь в виде двух жидких фаз с границей раздела. Компоненты растворов сохраняют свои уникальные свойства и не вступают в химические реакции между собой с образованием новых соединений. Так, при смешивании двух объемов водорода с одним объемом кислорода получается газообразный раствор. Если эту газовую смесь поджечь, то образуется новое вещество – вода, которая сама по себе раствором не является. Компонент, присутствующий в растворе в большем количестве, принято называть растворителем, остальные компоненты – растворенными веществами. Однако иногда бывает трудно провести грань между физическим перемешиванием веществ и их химическим взаимодействием. Например, при смешивании газообразного хлороводорода HCl с водой H2O образуются ионы H3O+ и Cl-. Они притягивают к себе соседние молекулы воды, образуя гидраты. Таким образом, исходные компоненты – HCl и H2O – после смешивания претерпевают существенные изменения. Тем не менее, ионизация и гидратация (в общем случае – сольватация) рассматриваются как физические процессы, происходящие при образовании растворов. Одним из важнейших типов смесей, представляющих собой гомогенную фазу, являются коллоидные растворы: гели, золи, эмульсии и аэрозоли. Размер частиц в коллоидных растворах составляет 1-1000 нм, в истинных растворах
0,1 нм (порядка размера молекул).
Основные понятия. Два вещества, растворяющиеся друг в друге в любых пропорциях с образованием истинных растворов, называют полностью взаиморастворимыми. Такими веществами являются все газы, многие жидкости (например, этиловый спирт – вода, глицерин – вода, бензол – бензин), некоторые твердые вещества (например, серебро – золото). Для получения твердых растворов необходимо сначала расплавить исходные вещества, затем смешать их и дать затвердеть. При их полной взаиморастворимости образуется одна твердая фаза; если же растворимость частичная, то в образовавшемся твердом веществе сохраняются мелкие кристаллы одного из исходных компонентов. Если два компонента образуют одну фазу при смешивании только в определенных пропорциях, а в других случаях возникают две фазы, то они называются частично взаиморастворимыми. Таковы, например, вода и бензол: истинные растворы получаются из них только при добавлении незначительного количества воды к большому объему бензола или незначительного количества бензола к большому объему воды. Если же смешать равные количества воды и бензола, то образуется двухфазная жидкая система. Нижний ее слой – это вода с небольшим количеством бензола, а верхний – бензол с малой примесью воды. Известны также вещества, совсем не растворяющиеся одно в другом, например, вода и ртуть. Если два вещества лишь частично взаиморастворимы, то при данных температуре и давлении существует предельное количество одного вещества, которое способно образовать истинный раствор с другим в равновесных условиях. Раствор с предельной концентрацией растворенного вещества называют насыщенным. Можно приготовить и так называемый пересыщенный раствор, в котором концентрация растворенного вещества даже больше, чем в насыщенном. Однако пересыщенные растворы неустойчивы, и при малейшем изменении условий, например при перемешивании, попадании частичек пыли или добавлении кристалликов растворяемого вещества, избыток растворенного вещества выпадает в осадок. Всякая жидкость начинает кипеть при той температуре, при которой давление ее насыщенного пара достигает величины внешнего давления. Например, вода под давлением 101,3 кПа кипит при 100° С потому, что при этой температуре давление водяного пара как раз равно 101,3 кПа. Если же растворить в воде какое-нибудь нелетучее вещество, то давление ее пара понизится. Чтобы довести давление пара полученного раствора до 101,3 кПа, нужно нагреть раствор выше 100° С. Отсюда следует, что температура кипения раствора всегда выше температуры кипения чистого растворителя. Аналогично объясняется и понижение температуры замерзания растворов.
Закон Рауля. В 1887 французский физик Ф.Рауль, изучая растворы различных нелетучих жидкостей и твердых веществ, установил закон, связывающий понижение давления пара над разбавленными растворами неэлектролитов с концентрацией: относительное понижение давления насыщенного пара растворителя над раствором равно мольной доле растворенного вещества. Из закона Рауля следует, что повышение температуры кипения или понижение температуры замерзания разбавленного раствора по сравнению с чистым растворителем пропорционально молярной концентрации (или мольной доле) растворенного вещества и может быть использовано для определения его молекулярной массы. Раствор, поведение которого подчиняется закону Рауля, называется идеальным. Наиболее близки к идеальным растворы неполярных газов и жидкостей (молекулы которых не меняют ориентации в электрическом поле). В этом случае теплота растворения равна нулю, а свойства растворов можно прямо предсказать, зная свойства исходных компонентов и пропорции, в которых они смешиваются.
Для реальных растворов сделать такое предсказание нельзя. При образовании реальных растворов обычно выделяется или поглощается тепло. Процессы с выделением тепла называются экзотермическими, а с поглощением – эндотермическими. Те характеристики раствора, которые зависят в основном от его концентрации (числа молекул растворенного вещества на единицу объема или массы растворителя), а не от природы растворенного вещества, называют коллигативными. Например, температура кипения чистой воды при нормальном атмосферном давлении равна 100° С, а температура кипения раствора, содержащего 1 моль растворенного (недиссоциирующего) вещества в 1000 г воды, составляет уже 100,52° С независимо от природы этого вещества. Если же вещество диссоциирует, образуя ионы, то температура кипения увеличивается пропорционально росту общего числа частиц растворенного вещества, которое благодаря диссоциации превышает число молекул вещества, добавленных в раствор. Другими важными коллигативными величинами являются температура замерзания раствора, осмотическое давление и парциальное давление паров растворителя.
Концентрация раствора – это величина, отражающая пропорции между растворенным веществом и растворителем. Такие качественные понятия, как "разбавленный" и "концентрированный", говорят только о том, что раствор содержит мало или много растворенного вещества. Для количественного выражения концентрации растворов часто используют проценты (массовые или объемные), а в научной литературе – число молей или химических эквивалентов растворенного вещества на единицу массы или объема растворителя либо раствора. Чтобы не возникало путаницы, следует всегда точно указывать единицы измерения концентрации. Рассмотрим следующий пример. Раствор, состоящий из 90 г воды (ее объем равен 90 мл, поскольку плотность воды равна 1 г/мл) и 10 г этилового спирта (его объем равен 12,6 мл, поскольку плотность спирта равна 0,794 г/мл), имеет массу 100 г, но объем этого раствора равен 101,6 мл (а был бы равен 102,6 мл, если бы при смешивании воды и спирта их объемы просто складывались). Процентную концентрацию раствора можно рассчитать по-разному:

или


или


Единицы концентраций, используемые в научной литературе, основаны на таких понятиях, как моль и эквивалент, поскольку все химические расчеты и уравнения химических реакций должны основываться на том, что вещества вступают в реакции между собой в определенных соотношениях. Например, 1 экв. NaCl, равный 58,5 г, взаимодействует с 1 экв. AgNO3, равным 170 г. Ясно, что растворы, содержащие по 1 экв. этих веществ, имеют совершенно разные процентные концентрации. Молярность (M или моль/л) – число молей растворенного веществ, содержащихся в 1 л раствора. Моляльность (м или моль/1000 г) – число молей растворенного вещества, содержащихся в 1000 г растворителя. Нормальность (н. или моль/л) – число химических эквивалентов растворенного вещества, содержащихся в 1 л раствора. Мольная доля (безразмерная величина) – число молей данного компонента, отнесенное к общему числу молей растворенного вещества и растворителя. Мольный процент – мольная доля, умноженная на 100.) Наиболее распространенная единица – молярность, но при ее расчете следует учитывать некоторые неоднозначности. Например, чтобы получить 1M раствор данного вещества, растворяют в заведомо небольшом количестве воды точную его навеску, равную мол. массе в граммах, и доводят объем раствора до 1 л. Количество воды, необходимое для приготовления данного раствора, может слегка различаться в зависимости от температуры и давления. Поэтому два одномолярных раствора, приготовленных в разных условиях, в действительности имеют не совсем одинаковые концентрации. Моляльность вычисляется исходя из определенной массы растворителя (1000 г), которая не зависит от температуры и давления. В лабораторной практике гораздо удобнее отмеривать определенные объемы жидкостей (для этого существуют бюретки, пипетки, мерные колбы), чем взвешивать их, поэтому в научной литературе концентрации чаще выражают в молярностях, а моляльность обычно применяют только при особо точных измерениях. Нормальность используется для упрощения расчетов. Как мы уже говорили, вещества взаимодействуют друг с другом в количествах, соответствующих их эквивалентам. Приготовив растворы разных веществ одинаковой нормальности и взяв равные их объемы, мы можем быть уверены в том, что они содержат одно и то же количество эквивалентов. В тех случаях, когда трудно (или нет необходимости) делать различие между растворителем и растворенным веществом, концентрацию измеряют в мольных долях. Мольные доли, как и моляльности, не зависят от температуры и давления. Зная плотности растворенного вещества и раствора, можно пересчитать одну концентрацию в другую: молярность в моляльность, мольную долю и наоборот. Для разбавленных растворов данного растворенного вещества и растворителя эти три величины пропорциональны друг другу.
О каких бы особенностях раствора ни шла речь, первой его характеристикой будет концентрация, потому что именно от концентрации зависит большинство свойств раствора. Концентрацию соли в рассоле либо сахара в стакане чая можно определить по вкусу. Но в остальных случаях, концентрацию раствора приходится выражать более объективными показателями. Хотя бы с помощью процентов, т.е. через количество граммов растворенного вещества, приходящееся на 100 г раствора. Способ этот часто применяется в быту (в аптеке продается 3%-ная перекись водорода, в продуктовом магазине - 6%-ная уксусная кислота, в молочном магазине - 20%-ные сливки). Для примера посчитаем концентрацию сахара (сахарозы) в кружке чая. Обычная (не большая, не маленькая) кружка вмещает в себя 300 мл чая, из этих 300 мл часть приходится на молекулы сахара, если добавлено 2 чайные ложки (2 х 9 г = 18 г), то на долю растворенного сахара приходится 8 мл (определенно экспериментально), тогда на долю воды приходится 300 мл - 8 мл = 292 мл. 292 мл воды - это примерно 292 г, 2 чайные ложки сахара - 18 г сахара. Получается 5,8%-ный раствор сахара:
| 18 г | • 100% = 5,8% |
| 292 г + 18 г |
В физике же и химии к процентному способу выражения концентрации прибегают редко. Причина ясна: взаимодействуют друг с другом не граммы, а атомы. Если сопоставить два раствора различных веществ и одинаковой процентной концентрации, то их одинаковые объемы содержат различное количество молекул.
Молярная концентрация (молярность). Для химиков и физиков удобнее выражать концентрацию растворов через число молей в каком либо объеме (обычно в литре). В одном моле любого вещества содержится 6,022•1023 молекул (6,022•1023 - это число Авогадро - NA). Пользоваться молярной концентрацией значительно удобнее, чем процентной: два различных раствора характеризующихся одинаковой молярной концентрацией, в равных объемах содержат одинаковое число молей и, значит, молекул растворенных веществ. Посмотрим какая молярная концентрация у уже приготовленного чая. Формула сахара (сахарозы) C12H22O11, используя атомные массы из таблицы Менделеева считаем массу одного моля сахарозы:
12•12 + 1•22 + 16•11 = 342 г/моль
Наш чай содержит 18 г сахара, получается 18(г)/342(г/моль) = 0,053 моль. Общий объем чая 300 мл, или 0,3 л, тогда концентрация, отнесенная к одному литру, будет:
| 0,053 моль | = 0,177 моль/л |
| 0,3 л |
При использовании молярной концентрации, сразу можно сказать какой объем раствора необходим для какой либо реакции. Например, есть раствор азотной кислоты концентрацией 0,01 моль/л который нужно нейтрализовать раствором гидроксида натрия концентрацией 0,1 моль/л, реакция нейтрализации имеет следующий вид:
HNO3 + NaOH → NaNO3 + H2O
Из реакции видно, что на 1 моль кислоты необходим 1 моль основания (столько же, сколько кислоты), то есть если в 0,5 л 0,01 молярного раствора кислоты содержится 0,005 моль кислоты, для её нейтрализации необходимо добавить столько же молей основания - 0,005 моль. Столько молей основания содержит 50 мл 0,1 молярного раствора (0,005(моль)/0,1(моль/л) = 0,05 л = 50 мл). Если необходимо нейтрализовать 0,01 молярный раствор серной кислоты:
H2SO4 + 2NaOH → Na2SO4 + 2H2O
Для нейтрализации 1 моля кислоты необходимо 2 моля основания (в два раза больше). Тогда для нейтрализации 0,5 л 0,01 молярного раствора, содержащего 0,005 моль кислоты, необходим 0,01 моль основания. Столько молей основания содержится в 100 мл 0,1 молярного раствора (0,01(моль)/0,1(моль/л)=0,1л=100мл).
Недостатком такого выражения концентрации (как и любого выражения концентрации отталкивающегося от объема раствора) является зависимость от температуры, т.к. при изменении температуры изменяется объем. Кроме того, при приготовлении концентрированных растворов приходится учитывать увеличение объема после добавление значительного количества вещества, как это было сделано при расчете молярной концентрации сахара в чае (однако для концентрированных растворов молярная концентрация обычно не используется).
Моляльность. Количество молей растворенного вещества, приходящееся на 1 кг растворителя. Моляльность в отличие молярности не зависит от объема раствора, и в этом главное преимущество моляльности над молярностью. Вернемся к нашему чаю, посчитаем его моляльность. Количество молей сахара мы уже посчитали (0,053 моль). Масса используемой воды равна 0,292 кг. Получается:
| 0,053 моль | = 0,182 моль/кг |
| 0,292 кг |
У разбавленного водного раствора молярность и моляльность будут почти равны. Это потому, что 1000 г воды примерно соответствует 1 л (объем зависит от температуры), а добавление к 1000 г воды незначительного количества вещества почти не влияет на объем получившегося раствора. Однако в случаи концентрированных растворов, когда добавление вещества к 1 л воды приводит к увеличению объема раствора, или когда физические условия (температура, давление) существенно влияют на объем раствора, молярность и моляльность будут отличаться.
Мольно-долевое выражение концентрации. В данном случае концентрацию выражают через отношение числа молей растворенного вещества к сумме молей растворенного вещества и растворителя. Так, если количество молей растворенного вещества составляет m, а количество молей растворителя ms, то мольная доля растворенного вещества N будет равна:
| N = | m |
| m + ms |
Понятно, что мольно-долевая концентрация всегда меньше 1. Существенно важно и то, что, в отличие от предыдущих способов выражения концентрации, мольно-долевая концентрация - величина безразмерная. Посчитаем для чая, число молей сахара уже известно (0,053 моль), количество молей используемой воды считаем также как и количество молей сахара, сначала используя таблицу Менделеева считаем массу одного моля воды (H2O):
1•2 + 16 = 18 г/моль
Далее считаем сколько молей в 292 мл (292 г) воды: 292(г)/18(г/моль) = 16,222 моль (умножив эту цифру на число Авогадро можно узнать сколько ориентировочно молекул воды выпивается с кружкой чая).
Теперь можно посчитать мольно-долевую концентрацию:
| 0,053 моль | = 0,0033 |
| 0,053 моль + 16,222 моль |
Много, очень много различных способов выражения концентрации растворов - размерных и безразмерных, объективных и не очень, простых и сложных придумали люди, и, конечно, всех их не перечислить. Например, при оценке загрязненности водоёмов, концентрацию загрязняющих веществ выражают в долях от предельно допустимой концентрации (ПДК), так если концентрация меди в воде 0,005 мг/л при ПДК для меди 0,01 мг/л, от концентрацию меди можно представить как 0,5 ПДК (0,005(мг/л)/0,01(мг/л)), а если концентрация 0,02 мг/л, то это 2 ПДК (0,02(мг/л)/0,01(мг/л)).
Растворимость данного вещества – это его способность образовывать растворы с другими веществами. Количественно растворимость газа, жидкости или твердого тела измеряется концентрацией их насыщенного раствора при данной температуре. Это важная характеристика вещества, помогающая понять его природу, а также влиять на ход реакций, в которых это вещество участвует.
Газы. В отсутствие химического взаимодействия газы смешиваются друг с другом в любых пропорциях, и в этом случае говорить о насыщении нет смысла. Однако при растворении газа в жидкости существует некая предельная концентрация, зависящая от давления и температуры. Растворимость газов в некоторых жидкостях коррелирует с их способностью к сжижению. Наиболее легко сжижаемые газы, например NH3, HCl, SO2, более растворимы, чем трудно сжижаемые газы, например O2, H2 и He. При наличии химического взаимодействия между растворителем и газом (например, между водой и NH3 или HCl) растворимость увеличивается. Растворимость данного газа изменяется с природой растворителя, однако порядок, в котором располагаются газы в соответствии с увеличением их растворимости, остается примерно одинаковым для разных растворителей. Процесс растворения подчиняется принципу Ле Шателье (1884): если на систему, находящуюся в равновесии, оказывается какое-либо воздействие, то в результате протекающих в ней процессов равновесие сместится в таком направлении, что оказанное воздействие уменьшится. Растворение газов в жидкостях обычно сопровождается выделением тепла. При этом, в соответствии с принципом Ле Шателье, растворимость газов уменьшается. Это уменьшение тем заметнее, чем выше растворимость газов: такие газы имеют и большую теплоту растворения. "Мягкий" вкус кипяченой или дистиллированной воды объясняется отсутствием в ней воздуха, поскольку его растворимость при высокой температуре весьма мала. С ростом давления растворимость газов увеличивается. Согласно закону Генри (1803), масса газа, который может раствориться в данном объеме жидкости при постоянной температуре, пропорциональна его давлению. Это свойство используется для приготовления газированных напитков. Углекислый газ растворяют в жидкости при давлении 3-4 атм.; в этих условиях в данном объеме может раствориться в 3-4 раза больше газа (по массе), чем при 1 атм. Когда емкость с такой жидкостью открывают, давление в ней падает, и часть растворенного газа выделяется в виде пузырьков. Аналогичный эффект наблюдается при открывании бутылки шампанского или выходе на поверхность подземных вод, насыщенных на большой глубине углекислым газом. При растворении в одной жидкости смеси газов растворимость каждого из них остается такой же, как и в отсутствие других компонентов при таком же давлении, как в случае смеси (закон Дальтона).
Жидкости. Взаимная растворимость двух жидкостей определяется тем, насколько сходно строение их молекул ("подобное растворяется в подобном"). Для неполярных жидкостей, например углеводородов, характерны слабые межмолекулярные взаимодействия, поэтому молекулы одной жидкости легко проникают между молекулами другой, т.е. жидкости хорошо смешиваются. Напротив, полярные и неполярные жидкости, например вода и углеводороды, смешиваются друг с другом плохо. Каждой молекуле воды нужно сначала вырваться из окружения других таких же молекул, сильно притягивающими ее к себе, и проникнуть между молекулами углеводорода, притягивающими ее слабо. И наоборот, молекулы углеводорода, чтобы раствориться в воде, должны протиснуться между молекулами воды, преодолевая их сильное взаимное притяжение, а для этого нужна энергия. При повышении температуры кинетическая энергия молекул возрастает, межмолекулярное взаимодействие ослабевает и растворимость воды и углеводородов увеличивается. При значительном повышении температуры можно добиться их полной взаимной растворимости. Такую температуру называют верхней критической температурой растворения (ВКТР). В некоторых случаях взаимная растворимость двух частично смешивающихся жидкостей увеличивается при понижении температуры. Этот эффект наблюдается в том случае, когда при смешивании выделяется тепло, обычно в результате химической реакции. При значительном понижении температуры, но не ниже точки замерзания, можно достичь нижней критической температуры растворения (НКТР). Можно предположить, что все системы, имеющие НКТР, имеют и ВКТР (обратное не обязательно). Однако в большинстве случаев одна из смешивающихся жидкостей кипит при температуре ниже ВКТР. У системы никотин – вода НКТР равна 61 °С, а ВКТР составляет 208 °C. В интервале
61–208 °C эти жидкости ограниченно растворимы, а вне этого интервала обладают полной взаимной растворимостью.
Твердые вещества. Все твердые вещества проявляют ограниченную растворимость в жидкостях. Их насыщенные растворы имеют при данной температуре определенный состав, который зависит от природы растворенного вещества и растворителя. Так, растворимость хлорида натрия в воде в несколько миллионов раз выше растворимости нафталина в воде, а при растворении их в бензоле наблюдается обратная картина. Этот пример иллюстрирует общее правило, согласно которому твердое вещество легко растворяется в жидкости, имеющей с ним сходные химические и физические свойства, но не растворяется в жидкости с противоположными свойствами. Соли обычно легко растворяются в воде и хуже - в других полярных растворителях, например в спирте и жидком аммиаке. Однако растворимость солей тоже существенно различается: например, нитрат аммония обладает в миллионы раз большей растворимостью в воде, чем хлорид серебра. Растворение твердых веществ в жидкостях обычно сопровождается поглощением тепла, и в соответствии с принципом Ле Шателье их растворимость должна увеличиваться при нагревании. Этот эффект можно использовать для очистки веществ методом перекристаллизации. Для этого их растворяют при высокой температуре до получения насыщенного раствора, затем раствор охлаждают и после выпадения растворенного вещества в осадок профильтровывают. Есть вещества (например, гидроксид, сульфат и ацетат кальция), растворимость которых в воде с ростом температуры уменьшается. Твердые вещества, как и жидкости, тоже могут растворяться друг в друге полностью, образуя гомогенную смесь - истинный твердый раствор, аналогичный жидкому раствору. Частично растворимые друг в друге вещества образуют два равновесных сопряженных твердых раствора, составы которых изменяются с температурой.
Коэффициент распределения. Если к равновесной системе двух несмешивающихся или частично смешивающихся жидкостей добавить раствор какого-либо вещества, то оно распределяется между жидкостями в определенной пропорции, не зависящей от общего количества вещества, в отсутствие химических взаимодействий в системе. Это правило получило название закона распределения, а отношение концентраций растворенного вещества в жидкостях - коэффициента распределения. Коэффициент распределения примерно равен отношению растворимостей данного вещества в двух жидкостях, т.е. вещество распределяется между жидкостями соответственно его растворимостям. Это свойство используется для экстракции данного вещества из его раствора в одном растворителе с помощью другого растворителя. Еще одним примером его применения является процесс экстракции серебра из руд, в состав которых оно часто входит вместе со свинцом. Для этого в расплавленную руду добавляют цинк, который не смешивается со свинцом. Серебро распределяется между расплавленным свинцом и цинком, преимущественно в верхнем слое последнего. Этот слой собирают и отделяют серебро дистилляцией цинка.
Произведение растворимости (ПР). Между избытком (осадком) твердого вещества M x B y и его насыщенным раствором устанавливается динамическое равновесие, описываемое уравнением

Константа равновесия этой реакции равна

и называется произведением растворимости. Она постоянна при данных температуре и давлении и является величиной, на основании которой рассчитывают растворимость осадка и изменяют ее. Если в раствор добавить соединение, диссоциирующее на ионы, одноименные с ионами малорастворимой соли, то в соответствии с выражением для ПР растворимость соли уменьшается. При добавлении же соединения, реагирующего с одним из ионов, она, напротив, увеличится.
 2014-02-02
2014-02-02 1260
1260