Собрать прибор как это показано на рис.1. Заполнить электролитические ячейки соответствующим раствором электролита. Подготовить рабочий электрод (обезжирить поверхность, промыть дистиллированной водой, высушить фильтровальной бумагой, взвесить с точностью до 0,0002 г). Провести электролиз (время электролиза и силу тока указывает преподаватель). Взвесить рабочий электрод после опыта с точностью до 0,0002 г, предварительно промыв его водой 





























|
|
|
|
|



 (–) (+)
(–) (+)
К(–) А(+) К(–) А(+) К(–) А(+) К(–) А(+) К(–) А(+)
Рис. 1 Прибор для проведения электролиза.
Результаты опыта записать в табл. 2.
Таблица 2. Результаты опыта.
| Название электролита | Масса электрода до опыта, г | Масса электрода после опыта, г | Время электролиза, с | Сила тока, А | Площадь покрытия, см2 |
| свинцевание | |||||
| блестящее меднение | |||||
| никелирование | |||||
| цинкование | |||||
| кулонометрия |
По данным табл. 2 произведите следующие расчеты:
1) Рассчитайте теоретическую силу тока в цепи (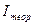 ), считая, что выход металла по току в кулонометрии равен 100 %:
), считая, что выход металла по току в кулонометрии равен 100 %:
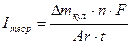 (7)
(7)
где 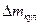 – изменение массы электрода в кулонометрии;
– изменение массы электрода в кулонометрии;
n – валентность меди;
F – постоянная Фарадея;
Ar – атомная масса меди;
t – время электролиза.
2) Определите ошибку амперметра, пользуясь соотношением:
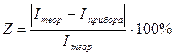 (8)
(8)
где 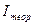 – сила тока в цепи, А;
– сила тока в цепи, А;
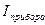 – сила тока, заданная по амперметру, А.
– сила тока, заданная по амперметру, А.
3) Используя формулы (4), (6), (9) и (10) вычислите теоретическую массу металла, восстановившегося на катоде; выход металла по току для всех случаев электролиза (кроме кулонометрии); плотность по току; толщину покрытия:
Плотность тока вычисляется по формуле:
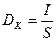 (9)
(9)
где I – сила тока, А;
S – площадь покрытия, см2
Толщина покрытия рассчитывается по формуле:
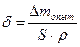 (10)
(10)
где 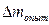 – изменение массы рабочего электрода в процессе электролиза, г;
– изменение массы рабочего электрода в процессе электролиза, г;
S – площадь покрытия, см2;
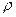 – плотность металла покрытия, г/см3.
– плотность металла покрытия, г/см3.
Исходя из проведенных расчетов, сформулируйте выводы.
 2015-01-07
2015-01-07 417
417








