Химически чистая вода обладает хотя и ничтожной, но измеримой электропроводностью, так как вода в незначительной степени диссоциирует на ионы. Так при комнатной температуре лишь примерно одна из 108 молекул воды находится в диссоциированной форме. Процесс электролитической диссоциации воды возможен благодаря достаточно высокой полярности связей О-Н и наличию между молекулами воды системы водородных связей. Уравнение диссоциации воды записывается так:
2H2O ↔ H3O+ + OH- ,
где H3O+ - катион гидроксония водорода.
Уравнение диссоциации воды можно записать в более простой форме:
H2O ↔ H+ + OH- .
Присутствие в воде ионов водорода и гидроксида придают ей специфические свойства амфолита, т.е. способность выполнять функции слабой кислоты и слабого основания. Константа диссоциации воды при температуре 220С:
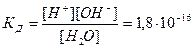 , (1)
, (1)
где [H+] и [OH-] – равновесные концентрации в г-ион/л соответственно катионов водорода и гидроксо-анионов, а [H2O] – равновесная концентрация воды в моль/л. Учитывая, что степень диссоциации воды чрезвычайно мала, равновесную концентрацию недиссоциированных молекул воды вполне можно приравнять к общему количеству воды, заключающемуся в 1 л ее:
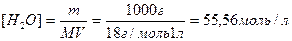 . (2)
. (2)
Теперь выражение (1) можно записать в следующем виде:
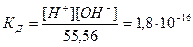 , (3)
, (3)
отсюда [H+] [OH-] = (1,8 10-16) 55,56 = 10-14 г-ион2/л2.
Произведение концентраций ионов водорода и гидроксо-ионов является константой не только для воды, но и для водных растворов солей, кислот и щелочей. Эта величина называется ионным произведением воды или константой воды. Следовательно: КН2О = [H+][OH-] = 10-14 г-ион2/л2.
Для нейтральных сред [H+] = [OH-] = 10-7 г-ион/л. В кислых средах [H+] > [OH-], а в щелочных [H+] < [OH-]. При этом в любых средах произведение концентраций ионов водорода и гидроксо-ионов при данной температуре остается постоянным и равным 10-14 г-ион2/л2. Таким образом, пользуясь ионным произведением воды, любую реакцию среды (нейтральную, кислую или щелочную) можно количественно выразить при помощи концентрации водородных ионов.
 2015-01-07
2015-01-07 831
831








