Фазовые переходы подчиняются определённым закономерностям, в основе которых лежит понятие равновесия фаз. Равновесие фаз характеризуется константой равновесия, которая зависит от температуры и давления.
Константа фазового равновесия i-го компонента характеризуется отношением мольной доли компонента в газовой фазе (уi или Nyi) к мольной доле этого компонента в жидкой фазе (хi или Nxi), находящейся в равновесном состоянии с газовой фазой:
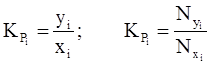 . (4.1)
. (4.1)
Для определения равновесного состояния газожидкостных смесей используются законы Дальтона и Рауля.
Согласно закону Дальтона каждый компонент, входящий в газовую фазу имеет своё парциальное давление Pi, а общее давление в газовой системе равно сумме парциальных давлений:
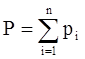 (4.2)
(4.2)
Согласно закону Рауля, парциальное давление компонента над жидкостью (нефтью) равно давлению насыщенного пара (Рнас. пара) или упругости пара (Qi) и этого компонента, умноженному на его мольную долю в нефти:
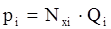 или
или 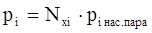 (4.3)
(4.3)
где Qi – упругость паров компонента;
Nxi – мольная доля компонента
piнас. пара – давление насыщенного пара i-го компонента.
В момент равновесия парциальное давление i-го компонента в газовой фазе равно парциальному давлению компонента над жидкостью. Отсюда следует закон Дальтона-Рауля для равновесного состояния газовой и нефтяной фазы:
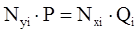 ; (4.4)
; (4.4)
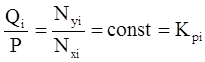 , (4.5)
, (4.5)
где Кi – константа равновесия i-го компонента при данной температуре и давлении смеси.
Уравнение материального баланса для одного моля нефтегазовой смеси:
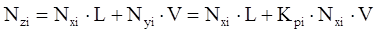 , (4.6)
, (4.6)
где L – мольная доля жидкой фазы;
V – мольная доля паровой фазы
Nzi – мольные доли компонентов в нефтегазовой смеси.
По условию сумма мольной доли жидкой и паровой фаз равна единице. Отсюда:
V=1–L. (4.7)
Используя уравнения (4.6) и (4.7) получим выражение для мольной доли компонента жидкой фазы:
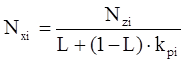 , (4.8)
, (4.8)
и для мольной доли компонента газовой фазы:
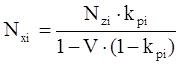 . (4.9)
. (4.9)
 2015-01-21
2015-01-21 712
712







