В результате протекания обменных реакций (14.1) образуются предварительные молекулы нерастворенных соединений, которые объединяются в агломераты постепенно с образованием критических зародышей.
Размер устойчивого критического зародыша r ~G/mxn; где:
· G – удельная поверхностная энергия образования кристалла. (G CaSO4 = 10-2 Дж/м2);
· mxn - разность химических потенциалов;
m xn = mкристалла- m растворителя.
Чем ниже G, тем труднее образуется зародыш; после образования Tкр. начинается его рост (рис. 3.2). Для описания роста кристалла используется модель с фронтальным перемещением зоны химической реакции.
Стадии гетерогенного процесса:
1. Внешняя диффузия (реакция 3.4);
2. Химическая поверхностная реакция (реакция 4.1).
Расчетная схема (рис. 14.1).
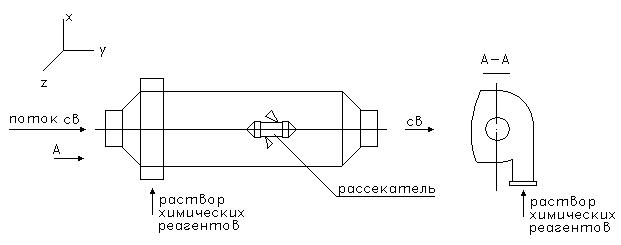
Особенностистатического реактора - отсутствие вращательных перемешивающих устройств.
Достоинства:
1. наличие рассекателя стационарного устройства понижает энергетические затраты на перемешивание (используются внутренние резервы кинетических потоков сточных вод) " поэтому статические смесители в случае осадкообразования имеют преимущество над динамическими.
Рис 14.2. Распределение поля концентраций в реакторе- смесителе.
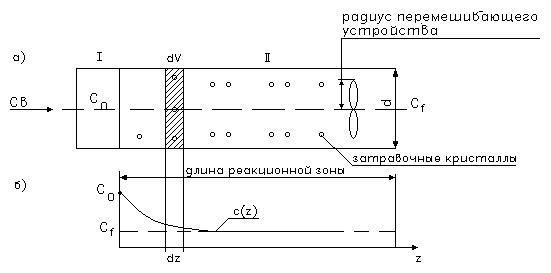
I - зона мгновенного смешивания (идеальное) сточных вод и химических реагентов.
· Время коагуляции – 2сек;
· Vсв/V хим.р-ции =103-104.
II- зона роста кристаллов и флокулообразования.
Скоростной градиент:
· dM/dz – должен плавно убывать, чтобы не разрушались флокулы;
· U – линейная скорость потока сточных вод, м/с.
В объеме реакционного пространства /V/ необходимо поддерживать определенную концентрацию затравочных кристаллов (CaCO3), т.е. необходимо создавать циркуляционные схемы с возвратом части очищенного потока в голову процесса
Основное уравнение массопередачи: dM/dt= k*CС*F
Затравочные кристаллы увеличивают удельную поверхность – f (м2/м3).
С(z) – изменение профиля по длине z.
 2015-02-27
2015-02-27 740
740








