Задача 1. Концентрация водородных ионов в растворе равна 10 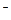 4 моль/л.
4 моль/л.
Найти рН раствора.
Решение: pH= - lg 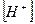 = - lg10
= - lg10 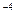 =-(-4) =4.
=-(-4) =4.
Ответ: 4
Задача 2. рН = 3. Найти концентрацию водородных ионов в растворе.
Решение: pH= -lg[H+]; lg[H+] = -pH = -3,
[H+]=10-pH; [H+]= 10-3 моль/л.
Ответ: 10-3 моль/л.
Задача 3. Вычислить константу диссоциации кислоты, если рОН её 0,001 н раствора равен 8,3. 
Решение:
рH + рOH = 14; рH = 14 – 8,3 = 5,7 рH = – lg [H+]
lg [H+] = –5,7 = (–6 + 0,3) = 6,3, используя понятие антилогарифма, находим
[H+] = 2•10–6 моль /л.
[H+] = 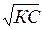 ; [H+]2 = KC;
; [H+]2 = KC;
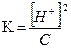
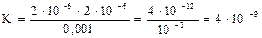
Ответ: 4•10–9
Задача 4. Вычислить ионную силу для 0,4 М раствора Al2(SO4)3 и раствора KCl той же молярности.
Решение:

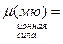
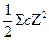 Al2 (SO4)3 ↔ 2Al3+ + 3SO42-
Al2 (SO4)3 ↔ 2Al3+ + 3SO42-

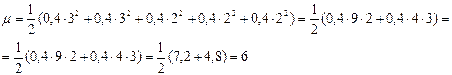
 Для раствора KCl:
Для раствора KCl: 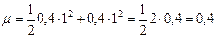 .
.
Ответ: 0,4
 2015-02-04
2015-02-04 1370
1370