В прошлом столетии Гиббс ввел в практику тепловых расчетов новую функцию - энтальпию.
Определение: Энтальпия это сумма внутренней энергии тела и произведения давления на объем;
I = U + PV; [кДж]
где: I – энтальпия; U –внутренняя энергия; P – давление; V -объем.
С каждым состоянием термодинамической системы связано одно вполне определенно значение энтальпии, и поскольку энтальпия является функцией состояния, то она может быть представлена в виде функции двух любых других параметров состояния:
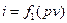 ,
, 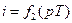 ,
, 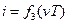
Удельная энтальпия i [кДж/кг] это отношение энтальпии тела к его массе. Удельная энтальпия это параметр состояния. Значение удельной энтальпии пара и воды при определенном давлении и температуре можно найти в справочнике. Пользуясь этими данными, можно определить количество теплоты участвующее в процессе или работу процесса.
В изобарном процессе количество тепла определяется разностью конечной и начальной энтальпии q=i2-i1.
 2015-02-18
2015-02-18 1511
1511
