1 Вторичным амином является:
1) СН3; 2) СН3 - СН - СН2 - СН3;
ç ç
СН3-С- СН2-СН3 NH2
ç
NH2
3) CH3-CH2-CH2-NH2; 4) CH3-NH-CH3.
2 Количество первичных аминов с молекулярной формулой С4Н11N равно:
1) 2; 2) 3; 3) 4; 4) 5.
3 Количество изомерных аминов с молекулярной формулой С3Н9N равно:
1) 2; 2) 3; 3) 4; 4) 5.
4 Вторичный амин образуется в реакции:
1) R-NO2 + 3H2 ®; 2) RCONH2 + KBrO ®;
3) R-CN + 2H2 ®; 4) R-NC + 2H2 ®.
5 Продуктом превращений RCOOH 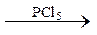 A
A 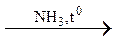 B
B 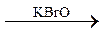 C
C
является:
1) первичный амин; 2) вторичный амин;
3) амид кислоты; 4) аминокислота.
6 Гидролизом белков получают:
1) первичные амины; 2) вторичный амины;
3) a- аминокислоты; 4) b-аминокислоты.
7 Оптические изомеры имеет соединение:
1) 2-амино-2-метилпропановая кислота;
2) амид пропановой кислоты;
3) 2-аминопропановая кислота;
4) 3-аминопропановая кислота.
8 Продуктом взаимодействия пропиламина с азотистой кислотой является:
1) спирт; 2) нитрозамин;
3) соль; 4) третичный амин.
9 Продуктом взаимодействия метилэтиламина с азотистой кислотой является:
1) спирт; 2) нитрозамин;
3) соль; 4) третичный амин.
10 Качественной реакцией на первичные амины является взаимодействие с:
1) HNO3; 2) HNO2; 3) Cu(OH)2; 4) Ag(NH3)2OH.
11 Для аминокислот характерны свойства:
1) только кислотные;
2) только основные;
3) амфотерные.
12 Продуктом нагревания b-аминокислот являются:
1) лактамы; 2) дикетопиперазины;
3) непредельные кислоты; 4) полипептиды.
13 Наличие пептидной связи в белках подтверждается реакцией:
1) ксантопротеиновой; 2) биуретовой;
3) сульфгидрильной; 4) денатурации.
14 Трипептид аланил-глицин-аланин имеет строение:
1) СH3-CH(NH2)-CO-NH-CH(CH3)-CO-NH-CH2COOH;
2) H2N-CH2-CO-NH-CH2-CO-NH-CH(CH3)-COOH;
3) CH3-CH(NH2)-CO-NH2–CH2-CO-NH-CH2-COOH;
4) CH3-CH(NH2)-CO-NH-CH2-CO-NH-CH(CH3)-COOH.
 2015-03-07
2015-03-07 1302
1302








