При изменении внешних условий скорости прямой и обратной реакций изменяются неодинаково: если в большей степени увеличивается vпр, то происходит сдвиг вправо; если vобр - сдвиг влево. Если vпр и vобр изменяются одинаково, значит, равновесие не нарушено. Таким образом, изменяя условия проведения реакции, можно смещать равновесие в нужную сторону, т.е. управлять течением химического процесса.
Смещение химического равновесия подчиняется принципу Ле-Шателье: при изменении внешних условий в равновесной системе происходит сдвиг равновесия, направленный в сторону той реакции, которая противодействует произведенному изменению. Так, благоприятными условиями для получения максимального выхода аммиака по реакции 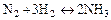 (DH=-80Дж/моль) являются: увеличение концентрации исходных компонентов N2 или H2, понижение температуры и повышение давления. (DH=-80Дж/моль) являются: увеличение концентрации исходных компонентов N2 или H2, понижение температуры и повышение давления.
|
 2015-04-01
2015-04-01 514
514








