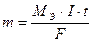 Для выделения на электроде 1 эквивалента любого вещества необходимо через электролит пропустить 96500 Кл электричества.
Для выделения на электроде 1 эквивалента любого вещества необходимо через электролит пропустить 96500 Кл электричества.
МЭ – эквивалентная масса, г/моль;
I - сила тока, А;
t – время проведения процесса, с;
F = 96500 Кл - число Фарадея.
1 F = 96500 Кл = 96500 А•с= 26,8 А•час
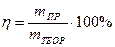 1Фарадей – это заряд, который несет на себе 1 моль электронов или 1 моль однозарядных ионов. Количественной характеристикой полноты использования тока является выход по току (η):
1Фарадей – это заряд, который несет на себе 1 моль электронов или 1 моль однозарядных ионов. Количественной характеристикой полноты использования тока является выход по току (η):
Применение электролиза
• Получение металлов – выделение в чистом виде алюминия и щелочных, щелочноземельных металлов производится электролизом расплавов, а остальных металлов – электролизом водных растворов.
• Очистка металлов – электролиз проводят с активным (растворимым) анодом.
• Получение различных химических веществ
• Зарядка аккумулятора – при разрядке аккумулятор работает как гальванический элемент, а зарядка -это процесс электролиза.
• Получение металлических покрытий – в декоративных целях, для защиты от коррозии, повышения твердости и электропроводности производят осаждение металла электролизом водного раствора соли, покрываемое изделие выполняет роль катода.
• Защита от коррозии – защита основана на электролизе, при котором защищаемый объект играет роль катода, на котором происходит восстановление воды.
 2015-04-12
2015-04-12 442
442








