Основы возникновения и развития пожара
ПОСОБИЕ ПО ВЫПОЛНЕНИЮ
КОНТРОЛЬНО-РАСЧЕТНОЙ РАБОТЫ
САНКТ-ПЕТЕРБУРГ
Содержание
1. Общие сведения. 3
2. Определение характеристик горения. 4
2.1 Характер свечения пламени. 5
2.2 Теоретический и практический расход водуха на горение. 10
2.3 Объем и состав продуктов полного сгорания. 21
2.4 Низшая теплота горения. 30
2.5 Стехиометрическая концентрация в паровоздушной смеси. 32
2.6 Расчет температуры горения. 33
2.7 Максимальное давление взрыва. 35
Общие сведения
По данным справочной литературы выписываются основные сведения о веществе:
Название вещества, структурная формула, область применения. Агрегатное состояние. Внешний вид, цвет и запах. Плотность. Относительная плотность пара по воздуху. Температура плавления. Температура кипения. Коэффициент молекулярной диффузии пара. Растворимость в воде. Химические свойства. Воздействие на человека.
Определение характеристик горения
Характер свечения пламени
Характер свечения пламени при горении веществ зависит от процентного содержания элементов в веществе, главным образом, углерода, водорода, кислорода и азота.
Свечение пламени связано с наличием несгоревших раскаленных твердых частиц углерода С, а также трехатомных молекул.
Если в горючем веществе при термическом разложении углерод не образуется, то вещество горит бесцветным пламенем как, например, в случае горения водорода Н2.
При термическом разложении веществ с массовой долей углерода менее 50 % и содержащих в своем составе кислород (более 30 %) несгоревших частиц углерода образуется очень мало, и в момент образования они успевают окислиться до СО.
СН3ОН 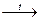 СО + 2Н2
СО + 2Н2
Такие вещества имеют голубоватые пламена (пламя угарного газа СО, метанола СН3ОН и этанола С2Н5ОН).
При горении веществ, содержащих более 75 % углерода (ацетилен С2Н2, бензол С6Н6), в зоне горения образуется настолько много частиц С, что поступающего путем диффузии воздуха не хватает для полного окисления всего углерода.
С6Н6 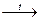 6С + 3Н2
6С + 3Н2
Не окислившийся в пламени углерод выделяется в виде копоти, и пламя при горении таких веществ будет ярким и коптящим.
Если кислород в веществе отсутствует или его содержание не превышает 30 %, но, в свою очередь, и массовая доля углерода не очень велика (менее 75 %), то при термическом разложении будет выделяться значительное количество частиц углерода, но при нормальном доступе воздуха в зону горения они успевают окислиться до СО2.
Возможная реакция при термическом разложении ацетона:
СН3СОСН3 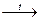 СО + 2С + 3Н2.
СО + 2С + 3Н2.
В подобных случаях пламя будет яркое, но не коптящее.
Сопоставляя значения процентного содержания углерода и кислорода в горючих веществах, можно приблизительно судить о характере свечения пламени (таблица 1.).
Таблица 1 Характер свечения пламени
| Содержание углерода в горючем веществе, w (С) % | Содержание кислорода в горючем веществе, w (О) % | Характер свечения пламени |
| < 50 | > 30 | пламя бесцветное или голубоватое |
| < 75 | отсутствует или < 30 | пламя яркое, не коптящее |
| > 75 | отсутствует или < 25 | пламя яркое, коптящее |
Цвет пламени горючих веществ, в основном, определяется присутствием в нем твердых частиц углерода. Если вместо углерода ввести в пламя другие твердые частицы, то пламя соответственно окрашивается. Так, например, если в бесцветное пламя метилового спирта ввести соли стронция, то пламя окрашивается в красный цвет, при введении солей бария - в зеленый, меди - в синий, натрия - в желтый. Вводимая в пламя соль при высокой температуре диссоциирует и образующиеся продукты диссоциации излучают характерные для них лучи. Так, например, хлористый барий при высокой температуре диссоциирует по уравнению:
2BaCl2 => 2BaCl + Cl2
Монохлорид ВаСl излучает в зеленой линии спектра. Это свойство солей некоторых металлов используется при изготовлении самых разнообразных пиротехнических составов.
Пример: Определить характер свечения пламени метаналя НСОН, фенола С6Н5ОН и пентанола С5Н11ОН.
1. Массовые доли углерода и кислорода в молекуле метаналя составляют:
Мr (НСОН) = 30
w (С) = 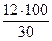 = 40 %; w (О) =
= 40 %; w (О) = 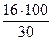 = 53 %
= 53 %
Массовая доля углерода < 50 %, а массовая доля кислорода > 30 %, следовательно, при горении метаналя наблюдается голубоватое пламя.
2. Массовые доли углерода и кислорода в молекуле фенола составляют:
Мr (С6Н5ОН) = 94
w (С) = 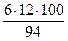 = 77 %; w (О) =
= 77 %; w (О) = 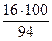 = 17 %
= 17 %
Массовая доля углерода > 50 %, а массовая доля кислорода < 25 %, следовательно, пламя при горении фенола яркое и коптящее.
3. Массовые доли углерода и кислорода в молекуле пентанола составляют:
Мr (С5Н11ОН) = 88
w (С) = 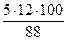 = 68 %; w (О) =
= 68 %; w (О) = 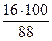 = 18 %
= 18 %
Массовая доля углерода < 75 %, а массовая доля кислорода < 30 %, следовательно, пламя при горении пентанола будет ярким, но не коптящим.
 2015-04-01
2015-04-01 6093
6093






