Стекло представляет собой изотропное твердое вещество, образующееся при охлаждении расплава компонентов, среди которых хотя бы один является стеклообразующим. Стеклообразующими являются оксиды SiО2, B2O3, Р2О5, GeО2, а также некоторые бескислородные соединения мышьяка, селена, теллура.
Основу стекла образует объемная сетка из однородных структурных элементов. В наиболее простом по составу кварцевом стекле такими элементами являются тетраэдры [SiO4], которые соединяются своими вершинами (рис. 3.6). Из таких же тетраэдров образована структура кристаллического кварца. Различие между двумя веществами одинакового химического состава объясняется тем, что в аморфных стёклах углы между связями Si-О лежат в пределах 120-180° − это больше, чем в кристаллическом кварце. Структура аморфного стекла возникает при охлаждении стеклянной массы, когда повышение её вязкости препятствует кристаллизации.
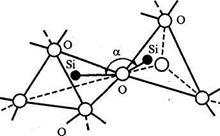 | Рис. 3.6. Расположение тетраэдров [SiO4] в стекле (α − угол между связями Si-O) |
Основную массу промышленных стекол составляют силикатные стекла с добавками других оксидов. По сравнению с кварцевым стеклом они размягчаются при более низких температурах и легче перерабатываются в изделия. В силикатных стеклах атомы соединяются ковалентно-ионными связями; в объемную сетку кроме кремния и кислорода входят также алюминий, титан, германий, бериллий; ионы щелочных и щелочноземельных металлов размещаются в ячейках этой сетки.
Усложнение химического состава силикатных стекол приводит к изменению их свойств, в том числе и цвета, и является причиной структурной неоднородности.
При охлаждении однофазный расплав расслаивается на две или несколько жидких фаз разного химического состава. Затвердевшее стекло имеет многофазную структуру. Расслоение силикатных стекол — характерная особенность их структуры.
При определенном соотношении содержания кремния, кислорода и других элементов очень трудно предупредить зарождение и рост кристаллов. Кристаллизация, или «расстекловывание » с образованием крупных кристаллов, отрицательно влияет на прочность и прозрачность стекла. Кристаллизацию предупреждают подбором химического состава стекла и условий его варки. Напряжения в стеклянных изделиях из-за различия плотности в разных участках устраняют нагревом, достаточным для перестройки элементов структуры и выравнивания плотности.
Из стекол специального состава при помощи контролируемой кристаллизации получают ситаллы, или стеклокристаллические материалы. Структура ситаллов представляет собой смесь очень мелких (0,01-1 мкм), беспорядочно ориентированных кристаллов (60 - 95 %) и остаточного стекла (5-40 %). Исходное стекло по химическому составу отличается от остаточного стекла, в котором накапливаются ионы, не входящие в состав кристаллов. Такая структура создается в стеклянных изделиях после двойного отжига (первый нужен для формирования центров кристаллизации, второй − для выращивания кристаллов на готовых центрах). Для образования кристаллов в стекла вводят Li2О, TiO2, AI2O3 и другие соединения.
В зависимости от условий образования центров кристаллизации ситаллы подразделяют на термоситаллы и фотоситаллы. В термоситаллах для образования центров кристаллизации используют оксиды или фториды ТiO2, Р2О5, NaF и др. (несколько процентов). При отжиге термоситалла получается высокая и однородная плотность кристаллов. В фотоситаллах используют малые добавки золота, серебра, платины или меди. Центры кристаллизации формируются под действием облучения ультрафиолетовым светом и отжига. Необлученные участки после отжига остаются аморфными.
Фотоситаллы применяются как фоточувствительные материалы. Термоситаллы имеют универсальное применение: как износостойкие материалы используются для деталей гидромашин, узлов трения, защитных эмалей; как прочные стабильные диэлектрики − для радиодеталей, плат и т.п.
 2015-04-01
2015-04-01 5151
5151
