Напомним, чтостепень диссоциации α - отношение числа молекул, распавшихся на ионы, к общему числу молекул, тогда для уравнения
КА K++A-
С∙ α – количество диссоциированных моль электролита КА,
(С-(С∙ α)) - количество недиссоциированных моль электролита КА.
Подставим эти значения в формулу выражения Кд:
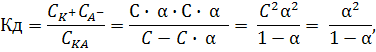
получим 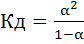 .
.
Это математическое выражение закона разбавления В. Оствальда (1888 г). Выражение можно упростить, если принять α→0. Величиной α в знаменателе пренебрегают и уравнение принимает вид:
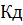 ≈ α2C, или α ≈
≈ α2C, или α ≈ 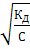
Формулировка закона разбавления В. Оствальда: «C разбавлением раствора слабого электролита степень диссоциации увеличивается».
 2015-04-01
2015-04-01 4026
4026








